| ADA | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Идентификаторы | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Псевдонимы | ADA, entrez: 100, Аденозиндезаминаза | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Внешние идентификаторы | OMIM: 608958 MGI: 87916 HomoloGene: 37249 GeneCard: ADA | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ортологи | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Виды | Человек | Мышь | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Entrez | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ensembl | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| UniProt | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| RefSeq (mRNA) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| RefSeq (белок) |
Аденозиндезаминаза (также известная как аденозинаминогидролаза или ADA ) представляет собой фермент (EC 3.5.4.4 ) участвует в метаболизме пуринов. Он необходим для расщепления аденозина с пищей и для обмена нуклеиновых кислот в тканях. Его основная функция у людей - развитие и поддержание иммунной системы. Однако полная физиологическая роль ADA еще не полностью изучена. Содержание
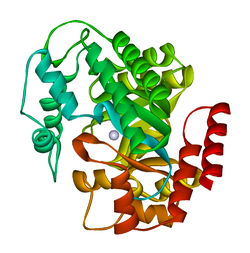
Структура ADA существует как в малой форме (в виде мономера) и крупная форма (в виде димер-комплекса). В мономерной форме фермент представляет собой полипептидную цепь, свернутую в восемь нитей параллельных α / β-бочек, которые окружают центральный глубокий карман, который является активным центром. Помимо восьми центральных β-бочек и восьми периферических α-спиралей, ADA также содержит пять дополнительных спиралей: остатки 19-76 складываются в три спирали, расположенные между β1 и α1 складками ; и две антипараллельные карбоксиконцевые спирали расположены поперек амино-конца β-цилиндра. Активный сайт ADA содержит ион цинка, который расположен в самом глубоком углублении активного центра и координируется пятью атомами His15, His17, His214, Asp295 и субстратом. Цинк - единственный кофактор, необходимый для деятельности. Субстрат, аденозин, стабилизирован и связан с активным центром девятью водородными связями. Карбоксильная группа Glu217, примерно копланарная пуриновому кольцу субстрата, может образовывать водородную связь с N1 субстрата. Карбоксильная группа Asp296, также копланарная пуриновому кольцу субстрата, образует водородную связь с N7 субстрата. Группа NH Gly184 может образовывать водородную связь с N3 субстрата. Asp296 образует связи как с ионом Zn, так и с 6-ОН субстрата. His238 также водородно связывается с субстратом 6-ОН. 3'-OH рибозы субстрата образует водородную связь с Asp19, а 5'-OH образует водородную связь с His17. Две дополнительные водородные связи образуются с молекулами воды при открытии активного центра с помощью 2'-OH и 3'-OH субстрата. Из-за того, что активный центр находится внутри фермента, после связывания субстрат почти полностью изолируется от растворителя. Воздействие на поверхность подложки связанного растворителя составляет 0,5% от воздействия на поверхность подложки в свободном состоянии. Реакции ADA необратимо дезаминирует аденозин, превращая его в родственный нуклеозид инозин заменой амино группой кетогруппой.  Аденозин Аденозин 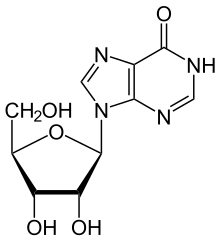 Инозин Инозин Инозин затем может быть дерибозилирован (удален из рибозы ) другим ферментом, называемым пуриновой нуклеозидфосфорилазой (PNP), превращая его в гипоксантин. Механизм катализа Предлагаемый механизм дезаминирования, катализируемого ADA, представляет собой стереоспецифическое присоединение-элиминирование через тетраэдрический промежуточный продукт. По любому механизму Zn как сильный электрофил активирует молекулу воды, которая депротонируется основным Asp295 с образованием атакующего гидроксида. His238 ориентирует молекулу воды и стабилизирует заряд атакующего гидроксида. Glu217 протонируется, чтобы отдать протон N1 субстрата. Реакция стереоспецифична из-за расположения остатков цинка, Asp295 и His238, которые все обращены к B-стороне пуринового кольца субстрата. Конкурентное ингибирование наблюдалось для ADA, когда продукт инозин действует как конкурентный ингибитор ферментативной активности. Функция ADA считается одним из ключевых ферментов метаболизма пуринов. Фермент был обнаружен у бактерий, растений, беспозвоночных, позвоночных и млекопитающих с высокой степенью сохранности аминокислотной последовательности. Высокая степень сохранения аминокислотной последовательности предполагает решающую природу ADA в пути спасения пуринов. В первую очередь, ADA у человека участвует в развитии и поддержании иммунной системы. Однако ассоциация ADA также наблюдалась с дифференцировкой эпителиальных клеток, нейротрансмиссией и сохранением беременности. Также было высказано предположение, что ADA, помимо расщепления аденозина, стимулирует высвобождение возбуждающих аминокислот и необходим для связывания аденозиновых рецепторов A1 и гетеротримерных G-белков. Дефицит аденозиндезаминазы приводит к фиброзу легких, предполагая, что хроническое воздействие высоких уровней аденозина может усугубить воспалительные реакции, а не подавить их. Также было обнаружено, что белок и активность аденозиндезаминазы активируются в сердцах мышей, которые сверхэкспрессируют HIF-1 альфа, что частично объясняет ослабленные уровни аденозина в сердцах, экспрессирующих HIF-1 альфа во время ишемии. стресс. Патология Некоторые мутации в гене аденозиндезаминазы приводят к тому, что он не экспрессируется. Возникающий в результате дефицит является одной из причин тяжелого комбинированного иммунодефицита (SCID), особенно аутосомно-рецессивного наследования. Недостаточный уровень ADA также был связан с воспалением легких, гибелью клеток тимуса и нарушением передачи сигналов рецепторами Т-клеток. И наоборот, мутации, вызывающие сверхэкспрессию этого фермента, являются одной из причин гемолитической анемии. Есть некоторые свидетельства того, что другой аллель (ADA2) может приводить к аутизму. Повышенный уровень ADA также был связан с СПИДом. изоформами Существует 2 изоформы ADA: ADA1 и ADA2.
Клиническая значимость ADA2 является преобладающей формой, присутствующей в плазме крови человека, и ее содержание во многих заболевания, особенно связанные с иммунной системой: например, ревматоидный артрит, псориаз и саркоидоз. Изоформа ADA2 в плазме также увеличивается при большинстве видов рака. ADA2 не является повсеместным, но сосуществует с ADA1 только в моноцитах-макрофагах. Общий ADA в плазме можно измерить с помощью высокоэффективной жидкостной хроматографии или ферментативных или колориметрических методов. Возможно, самая простая система - это измерение аммиака, высвобождаемого из аденозина при расщеплении до инозина. После инкубации плазмы с забуференным раствором аденозина аммиак реагирует с реагентом Бертло, образуя синий цвет, который пропорционален степени активности фермента. Для измерения ADA2 перед инкубацией добавляют эритро-9- (2-гидрокси-3-нонил) аденин (EHNA), чтобы ингибировать ферментативную активность ADA1. Отсутствие ADA1 вызывает SCID. ADA также может использоваться при лечении лимфоцитарных плевральных выпотов или перитонеального асцита в том смысле, что такие образцы с низким ADA по существу исключает туберкулез. Туберкулез плевральный выпот теперь можно точно диагностировать по повышенному уровню аденозиндезаминазы в плевральной жидкости, превышающему 40 Ед на литр. кладрибин и пентостатин представляют собой противоопухолевые агенты, используемые при лечении волосатоклеточного лейкоза ; их механизм действия - ингибирование аденозиндезаминазы. См. Также Ссылки Дополнительная литература Внешние ссылки
Последняя правка сделана 2021-06-10 00:38:29
Содержание доступно по лицензии CC BY-SA 3.0 (если не указано иное). | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||