 | |
 . __ Li __ N __ O . __ Li __ N __ O | |
 | |
| Идентификаторы | |
|---|---|
| Номер CAS | |
| 3D-модель (JSmol ) | |
| ChemSpider | |
| ECHA InfoCard | 100.029.290 |
| PubChem С ID | |
| номер RTECS |
|
| UNII | |
| CompTox Dashboard (EPA ) | |
InChI
| |
УЛЫБАЕТСЯ
| |
| Свойства | |
| Химическая формула | LiNO 3 |
| Молярная масса | 68,946 г / моль |
| Внешний вид | Твердое вещество от белого до светло-желтого |
| Плотность | 2,38 г / см |
| Температура плавления | 255 ° C (491 ° F; 528 K) |
| Температура кипения | 600 ° C (1112 ° F; 873 K) (разлагается) |
| Растворимость в воде | 52,2 г / 100 мл (20 ° C). 90 г / 100 мл (28 ° C). 234 г / 100 мл (100 ° C) |
| Растворимость | растворим в этаноле, метаноле, пиридине, аммиак, ацетон |
| Магнитная восприимчивость (χ) | -62,0 · 10 см / моль (+3 H 2 O) |
| Показатель преломления (nD) | 1,735 |
| Термохимия | |
| Теплоемкость (C) | 64 Дж / моль K |
| Стандартная молярная. энтропия (S 298) | 105 Дж / моль K |
| Стандартная энтальпия образования. (ΔfH298) | -7,007 кДж / г или -482,3 кДж / моль |
| свободная энергия Гиббса (ΔfG˚) | -389,5 кДж / моль |
| Стандартная энтальпия. горения (ΔcH298) | 25,5 кДж / моль |
| Опасности | |
| Основные опасности | Окислитель, раздражитель |
| NFPA 704 (огненный алмаз) |  0 1 0 OX 0 1 0 OX |
| Температура вспышки | Невоспламеняющийся |
| Смертельная доза или концентрация (LD, LC): | |
| LD50(средняя доза ) | 1426 мг / кг (перорально, крыса) |
| Родственные соединения | |
| Прочие катионы | Нитрат натрия. Нитр калия ели. нитрат рубидия. нитрат цезия |
| Родственные соединения | сульфат лития. хлорид лития |
| Если не указано иное, данные приведены для материалов в их стандартном состоянии ( при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки в ink | |
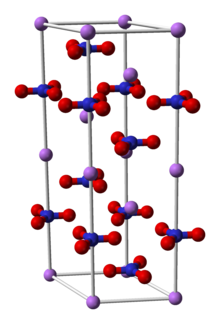
Нитрат лития представляет собой неорганическое соединение формулой LiNO 3. Это литиевая соль азотной кислоты (нитрат щелочного металла ). Соль расплывается, абсорбирует воду с образованием гидратированной формы, тригидрата нитрата лития. Его эвтектика представляет интерес для теплоносителей.
Его получают путем обработки карбоната лития или гидроксида лития с помощью азотной кислоты.
Эта жидкая бесцветная соль окислитель, используемый при производстве красных фейерверков и вспышек.
гидратированная форма, тригидрат нитрата лития, имеет чрезвычайно высокую удельную теплоту плавления, 287 (± 7) Дж / г, и, следовательно, может использоваться для хранения тепловой энергии при температуре его плавления 303,3 К.
Нитрат лития был предложен в качестве среды для хранения тепла, собираемого от солнца для приготовления пищи. Линза Френеля будет использоваться для плавления твердого нитрата лития, который затем будет функционировать как «солнечная батарея», позволяя позже перераспределять тепло за счет конвекции.
Нитрат лития можно синтезировать путем взаимодействия азотной кислоты и карбоната лития.
Обычно при образовании LiNO 3, Индикатор pH используется для определения того, когда вся кислота нейтрализована. Однако эту нейтрализацию можно также распознать по потере производства диоксида углерода. Чтобы избавить конечный продукт от лишней воды, образец нагревают.
Нитрат лития может быть токсичным для организма при приеме внутрь, поражая центральную нервную систему, щитовидную железу, почки и сердечно-сосудистую систему. При контакте с кожей, глазами и слизистыми оболочками нитрат лития может вызвать раздражение этих областей.
| HNO 3 | He | ||||||||||||||||
| LiNO 3 | Be (NO 3)2 | B (NO. 3). 4 | RONO 2 | NO. 3. NH4NO3 | HOONO 2 | FNO 3 | Ne | ||||||||||
| NaNO 3 | Mg (NO 3)2 | Al (NO 3)3 | Si | P | S | ClONO 2 | Ar | ||||||||||
| KNO 3 | Ca (NO 3)2 | Sc (NO 3)3 | Ti (NO 3)4 | VO (NO 3)3 | Cr ( NO 3)3 | Mn (NO 3)2 | . Fe (NO 3)3 | Co (NO 3)2. Co (NO 3)3 | Ni (NO 3)2 | CuNO 3. Cu (NO 3)2 | Zn (NO 3)2 | Ga (NO 3)3 | Ge | As | Se | Br | Kr |
| RbNO 3 | Sr (NO 3)2 | Y ( NO 3)3 | Zr (NO 3)4 | Nb | Mo | Tc | Pd (NO 3)2. | AgNO 3. | Cd (NO 3)2 | In | Sn | Te | I | Xe (NO 3)2 | |||
| CsNO 3 | Ba (NO 3)2 | Hf | Ta | W | Re | Os | Ir | . | Hg2(NO 3)2. Hg (NO 3)2 | . Tl (NO 3)3 | Pb (NO 3)2 | Bi (NO 3)3. BiO (NO 3) | At | Rn | |||
| Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og | |||
| ↓ | |||||||||||||||||
| Ce (NO 3)3. Ce (NO 3)4 | Nd (NO 3)3 | Eu (NO 3)3 | Gd (NO 3)3 | Tb (NO 3)3 | |||||||||||||
| Th (NO 3)4 | UO2) (NO 3)2 | Bk | Cf | Es | Fm | Md | № | Lr | |||||||||