| Глицерин-3-фосфатдегидрогеназа (NAD) | |||||||||
|---|---|---|---|---|---|---|---|---|---|
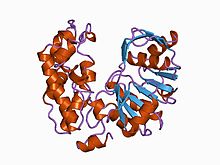
 Кристаллографическая структура глицерин-3-фосфатдегидрогеназы 1 человека. Кристаллографическая структура глицерин-3-фосфатдегидрогеназы 1 человека. | |||||||||
| Идентификаторы | |||||||||
| Номер EC | 1.1.1.8 | ||||||||
| Номер CAS | 9075-65-4 | ||||||||
| Базы данных | |||||||||
| IntEnz | IntEnz view | ||||||||
| BRENDA | BRENDA запись | ||||||||
| ExPASy | NiceZyme view | ||||||||
| KEGG | запись KEGG | ||||||||
| MetaCyc | метаболический путь | ||||||||
| PRIAM | профиль | ||||||||
| PDB структуры | RCSB PDB PDBe PDBsum | ||||||||
| Генная онтология | AmiGO / QuickGO | ||||||||
| |||||||||
| Глицерин-3-фосфатдегидрогеназа (хинон) | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Идентификаторы | |||||||||
| Номер ЕС | 1.1.5.3 | ||||||||
| Номер CAS | 9001-49-4 | ||||||||
| Базы данных | |||||||||
| IntEnz | IntEnz view | ||||||||
| BRENDA | BRENDA entry | ||||||||
| ExPASy | NiceZyme view | ||||||||
| KEGG | KEGG entry | ||||||||
| MetaCyc | метаболический путь | ||||||||
| PRIAM | профиль | ||||||||
| PDB структуры | RCSB PDB PDBe PDBsum | ||||||||
| |||||||||
| NAD-зависимый N-конец глицерин-3-фосфатдегидрогеназы | |||||||||
|---|---|---|---|---|---|---|---|---|---|
 кристаллическая структура n- (1-d-карбоксилэтил) -1-норвалиндегидрогеназы из Arthrobacter sp. штамм 1c кристаллическая структура n- (1-d-карбоксилэтил) -1-норвалиндегидрогеназы из Arthrobacter sp. штамм 1c | |||||||||
| Идентификаторы | |||||||||
| Символ | NAD_Gly3P_dh_N | ||||||||
| Pfam | PF01210 | ||||||||
| Pfam клан | CL0063 | ||||||||
| InterPro | IPR011128 | ||||||||
| PROSITE | PDOC00740 | ||||||||
| SCOPe | 1m66 / SUPFAM | ||||||||
| |||||||||
| НАД-зависимая глицерин-3-фосфатдегидрогеназа С-конец | |||||||||
|---|---|---|---|---|---|---|---|---|---|
 структура глицерин-3-фосфатдегидрогеназы из archaeoglobus fulgidus структура глицерин-3-фосфатдегидрогеназы из archaeoglobus fulgidus | |||||||||
| Идентификаторы | |||||||||
| Символ | NAD_Gly3P_dh_C | ||||||||
| Pfam | PF07479 | ||||||||
| Pfam клан | CL0106 | ||||||||
| InterPro | IPR006109 | ||||||||
| PROSITE | PDOC00740 <28380>SCOPe 1m66 / SUPFAM | ||||||||
| |||||||||
Глицерин-3-фосфатдегидрогеназа (GPDH ) - это фермент, который катализирует обратимое окислительно-восстановительное превращение дигидроксиацетонфосфат (также известный как глицеронфосфат, устаревший) на sn- глицерин-3-фосфат.
Глицерин-3-фосфатдегидрогеназа служит основным звеном между метаболизмом углеводов и липидный обмен. Он также является основным источником электронов в цепи переноса электронов в митохондриях.
Более старые термины для глицерин-3-фосфатдегидрогеназы включают альфа-глицерин-3-фосфатдегидрогеназу (альфаGPDH) и глицеринфосфат. дегидрогеназа (GPDH). Однако глицерин-3-фосфатдегидрогеназа отличается от глицеральдегид-3-фосфатдегидрогеназы (GAPDH), субстратом которой является альдегид, а не спирт.
GPDH играет важную роль в биосинтезе липидов . Посредством восстановления дигидроксиацетонфосфата в глицерин-3-фосфат GPDH обеспечивает быстрое дефосфорилирование глицерин-3-фосфата в глицерин. Кроме того, GPDH является одним из ферментов, участвующих в поддержании окислительно-восстановительного потенциала на внутренней митохондриальной мембране.
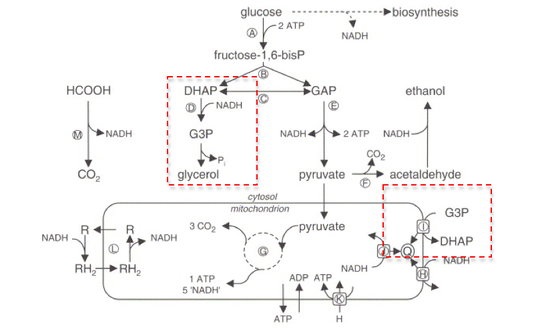 (рис. 1. Схематический обзор ферментативного и окислительного метаболизма глюкозы Saccharomyces cerevisiae. (A) верхняя часть гликолиза, которая включает две реакции фосфорилирования сахара. (B) фруктозо-1,6-бисфосфатальдолаза, расщепляющая молекулу C6 на два триозофосфата (C) триозофосфат-изомеразу, взаимопревращающую DHAP и GAP. (D) глицериновый путь, восстанавливающий DHAP до глицерин-3-фосфата (G3P) с помощью G3P-дегидрогеназы с последующим дефосфорилированием до глицерина с помощью G3Pase. (E) Нижняя часть гликолиза преобразует GAP в пируват, генерируя 1 НАДН и 2 АТФ с помощью серии из 5 ферментов. (F) Алкогольное брожение; декарбоксилирование пирувата пируватдекарбоксилазой с последующим восстановлением ацетальдегида до этанола. (G) митохондриальная пируват-дегидрогеназа превращает пируват в ацетил-КоА, который входит в цикл трикарбоновых кислот. (H) внешние митохондриальные NADH дегидрогеназы. (I) митохондриальная G3P-дегидрогеназа. Электроны этих трех дегидрогеназ попадают в дыхательную цепь на уровне пула хинолов (Q). (J) внутренняя митохондриальная НАДН-дегидрогеназа. (K) АТФ-синтаза. (L) обобщенная схема шаттла NADH. (M) окисление формиата формиатдегидрогеназой.
(рис. 1. Схематический обзор ферментативного и окислительного метаболизма глюкозы Saccharomyces cerevisiae. (A) верхняя часть гликолиза, которая включает две реакции фосфорилирования сахара. (B) фруктозо-1,6-бисфосфатальдолаза, расщепляющая молекулу C6 на два триозофосфата (C) триозофосфат-изомеразу, взаимопревращающую DHAP и GAP. (D) глицериновый путь, восстанавливающий DHAP до глицерин-3-фосфата (G3P) с помощью G3P-дегидрогеназы с последующим дефосфорилированием до глицерина с помощью G3Pase. (E) Нижняя часть гликолиза преобразует GAP в пируват, генерируя 1 НАДН и 2 АТФ с помощью серии из 5 ферментов. (F) Алкогольное брожение; декарбоксилирование пирувата пируватдекарбоксилазой с последующим восстановлением ацетальдегида до этанола. (G) митохондриальная пируват-дегидрогеназа превращает пируват в ацетил-КоА, который входит в цикл трикарбоновых кислот. (H) внешние митохондриальные NADH дегидрогеназы. (I) митохондриальная G3P-дегидрогеназа. Электроны этих трех дегидрогеназ попадают в дыхательную цепь на уровне пула хинолов (Q). (J) внутренняя митохондриальная НАДН-дегидрогеназа. (K) АТФ-синтаза. (L) обобщенная схема шаттла NADH. (M) окисление формиата формиатдегидрогеназой. Пара NAD+ /NADH кофермент действует как резервуар электронов для метаболических окислительно-восстановительные реакции, переносящие электроны от одной реакции к другой. Большинство этих метаболических реакций происходит в митохондриях. Чтобы регенерировать NAD + для дальнейшего использования, пулы NADH в цитозоле должны быть повторно окислены. Поскольку внутренняя мембрана митохондрий непроницаема как для НАДН, так и для НАД +, они не могут свободно обмениваться между цитозолем и митохондриями. матрица.
Один из способов переноса этого восстанавливающего эквивалента через мембрану - это глицерин-3-фосфатный челнок, который использует две формы GPDH:
Реакции, катализируемые цитозольным (растворимым) и митохондриальным GPDH, следующие:
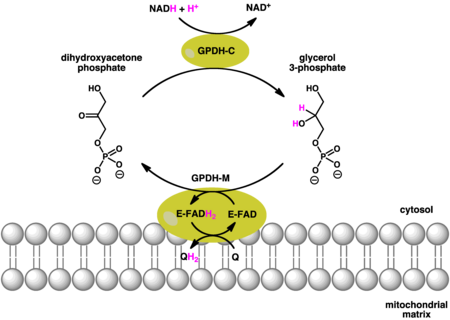 Сопряженные реакции, катализируемые цитозольным (GPDH-C) и митохондриальным (GPDH-M)) формы глицерин-3-фосфатдегидрогеназы. GPDH-C и GPDH-M используют NADH и хинол (QH) в качестве доноров электронов соответственно. GPDH-M дополнительно использует FAD в качестве кофактора. Сопряженные реакции, катализируемые цитозольным (GPDH-C) и митохондриальным (GPDH-M)) формы глицерин-3-фосфатдегидрогеназы. GPDH-C и GPDH-M используют NADH и хинол (QH) в качестве доноров электронов соответственно. GPDH-M дополнительно использует FAD в качестве кофактора. |
.
Есть две формы GPDH:
| Фермент | Белок | Ген | |||||
|---|---|---|---|---|---|---|---|
| Номер EC | Имя | Донор / Акцептор | Имя | Субклеточное расположение | Аббревиатура | Имя | Символ |
| 1.1.1.8 | глицерин-3-фосфатдегидрогеназа | НАДН / НАД | Глицерин-3-фосфатдегидрогеназа [NAD] | цитоплазматический | GPDH-C | глицерин-3-фосфатдегидрогеназа 1 (растворимый) | GPD1 |
| 1.1.5.3 | глицерин-3-фосфатдегидрогеназа | хинол / хинон | Глицерин-3-фосфатдегидрогеназа | митохондриальная | GPDH-M | глицерин-3-фосфатдегидрогеназа 2 (митохондриальная) | GPD2 |
Следующие гены человека кодируют белки с ферментативной активностью GPDH:
|
| ||||||||||||||||||||||||||||||||||||||||||||
Цитозольная глицерин-3-фосфатдегидрогеназа (GPD1) - это NAD + -зависимый фермент, который восстанавливает дигидроксиацетонфосфат на глицерин-3-фосфат. Одновременно NADH окисляется до NAD + в следующей реакции:
 Механизм реакции GPD1
Механизм реакции GPD1 В результате NAD + регенерируется для дальнейшей метаболической активности..
GPD1 состоит из двух субъединиц и реагирует с дигидроксиацетонфосфатом и NAD + посредством следующего взаимодействия:
Фиг.4. Предполагаемый активный сайт. Фосфатная группа DHAP наполовину окружена боковой цепью Arg269 и взаимодействует с Arg269 и Gly268 непосредственно за счет водородных связей (не показаны). Консервативные остатки Lys204, Asn205, Asp260 и Thr264 образуют стабильную сеть водородных связей. Другая сеть водородных связей включает остатки Lys120 и Asp260, а также упорядоченную молекулу воды (с B-фактором 16,4 Å2), которая связывается водородом с Gly149 и Asn151 (не показано). В этих двух электростатических сетях только группа ε-NH 3 Lys204 является ближайшей к атому C2 DHAP (3,4 Å).
Митохондриальный глицерин -3-фосфатдегидрогеназа (GPD2), катализирует необратимое окисление глицерин-3-фосфата до дигидроксиацетонфосфата и одновременно переносит два электрона с FAD на электронная транспортная цепь. GPD2 состоит из 4 идентичных субъединиц.
 Механизм реакции GPD2
Механизм реакции GPD2 Цитозоль вместе с митохондриальным глицерином -3-фосфатдегидрогеназа действуют согласованно. Окисление цитоплазматического НАДН цитозольной формой фермента приводит к образованию глицерин-3-фосфата из дигидроксиацетонфосфата. После того, как глицерин-3-фосфат прошел через внешнюю митохондриальную мембрану, он может быть окислен отдельной изоформой глицерин-3-фосфатдегидрогеназы, которая использует хинон в качестве окислителя и FAD в качестве кофактора. В результате возникает чистая потеря энергии, сравнимая с одной молекулой АТФ.
Совместное действие этих ферментов поддерживает соотношение НАД + / НАДН, которое обеспечивает непрерывную работу метаболизма.
Фундаментальная роль GDPH в поддержании потенциала NAD + / NADH, а также его роль в липидах метаболизм, делает GDPH фактором заболеваний липидного дисбаланса, таких как ожирение.
Считается, что митохондриальная изоформа G3P-дегидрогеназы ингибируется метформином, препаратом первой линии для диабета 2 типа.
Sarcophaga barbata использовалась для изучения окисления L-3-глицерофосфата в митохондриях. Установлено, что L-3-глицерофосфат не проникает в матрикс митохондрий, в отличие от пирувата. Это помогает найти L-3-глицерофосфат-флавопротеин оксидоредуктазу, которая находится на внутренней мембране митохондрий.
Глицерин-3-фосфатдегидрогеназа состоит из двух белковых доменов. N-концевой домен представляет собой NAD -связывающий домен, а C-конец действует как субстрат-связывающий домен. Однако димерные и тетрамерные интерфейсные остатки участвуют в связывании GAPDH-РНК, поскольку GAPDH может проявлять несколько подработок, включая модуляцию связывания и / или стабильности РНК.