 Основные структуры уплотнения ДНК: ДНК, нуклеосома, волокно «бусинки на нити» 10 нм, волокно хроматина 30 нм и метафаза хромосома.
Основные структуры уплотнения ДНК: ДНК, нуклеосома, волокно «бусинки на нити» 10 нм, волокно хроматина 30 нм и метафаза хромосома.Хроматин представляет собой комплекс ДНК и белок обнаружены в эукариотических клетках. Его основная функция - упаковка длинных молекул ДНК в более компактные и плотные структуры. Это предотвращает спутывание цепей, а также играет важную роль в укреплении ДНК во время деления клетки, предотвращении повреждения ДНК и регулировании экспрессии генов и Репликация ДНК. Во время митоза и мейоза хроматин способствует правильной сегрегации хромосом в анафазе ; характерные формы хромосом, видимые на этой стадии, являются результатом свертывания ДНК в сильно конденсированный хроматин.
Первичные белковые компоненты хроматина - это гистоны, которые связываются с ДНК и действуют как «якоря», вокруг которых наматываются нити. В общем, существует три уровня организации хроматина:
Однако многие организмы не следуют этой схеме организации. Например, сперматозоиды и avian красные кровяные тельца имеют более плотно упакованный хроматин, чем большинство эукариотических клеток, а трипаносоматиды простейшие вообще не конденсируют свой хроматин в видимые хромосомы. Прокариотические клетки имеют совершенно разные структуры для организации своей ДНК (эквивалент прокариотической хромосомы называется генофором и находится в области нуклеоида).
Общая структура хроматиновой сети дополнительно зависит от стадии клеточного цикла. Во время интерфазы хроматин структурно рыхлый, чтобы обеспечить доступ к РНК и ДНК-полимеразам, которые транскрибируют и реплицируют ДНК. Локальная структура хроматина во время интерфазы зависит от конкретных генов, присутствующих в ДНК. Активно транскрибируемые («включенные») участки ДНК, содержащие гены, менее плотно уплотнены и тесно связаны с РНК-полимеразами в структуре, известной как эухроматин, в то время как области, содержащие неактивные гены («выключены»), являются как правило, более конденсированы и связаны со структурными белками в гетерохроматине. Эпигенетическая модификация структурных белков хроматина посредством метилирования и ацетилирования также изменяет локальные структура хроматина и, следовательно, экспрессия генов. Структура хроматиновых сетей в настоящее время плохо изучена и остается активной областью исследований в молекулярной биологии.
 Основные единицы структуры хроматина
Основные единицы структуры хроматина Хроматин претерпевает различные структурные изменения в течение клеточного цикла. Белки гистонов являются основным упаковщиком и организатором хроматина и могут быть модифицированы с помощью различных посттрансляционных модификаций для изменения упаковки хроматина (модификация гистона ). Большинство модификаций происходит на гистоновом хвосте. Последствия с точки зрения доступности и уплотнения хроматина зависят как от модифицированной аминокислоты, так и от типа модификации. Например, ацетилирование гистонов приводит к разрыхлению и повышенной доступности хроматина для репликации и транскрипции. Три-метилирование лизина может коррелировать либо с транскрипционной активностью (триметилирование гистона H3, лизин 4), либо с репрессией транскрипции и уплотнением хроматина (три-метилирование гистона H3, лизина 9 или 27). Несколько исследований показали, что разные модификации могут происходить одновременно. Например, было высказано предположение, что двухвалентная структура (с триметилированием лизина 4 и 27 на гистоне H3) участвовала в раннем развитии млекопитающих.
Белки группы Polycomb играют роль роль в регуляции генов посредством модуляции структуры хроматина.
Для получения дополнительной информации см. Модификации гистонов в регуляции хроматина и Контроль РНК-полимеразы структурой хроматина.
 Структуры A-, B- и Z-ДНК.
Структуры A-, B- и Z-ДНК. В природе ДНК может образовывать три структуры: A-, B- и Z-ДНК. A- и B-ДНК очень похожи, образуя правые спирали, тогда как Z-ДНК представляет собой левую спираль с зигзагообразным фосфатным остовом. Считается, что Z-ДНК играет особую роль в структуре хроматина и транскрипции из-за свойств соединения между B- и Z-ДНК.
На стыке B- и Z-ДНК одна пара оснований отрывается от нормального связывания. Они играют двойную роль: сайт узнавания многими белками и приемник торсионного стресса от РНК-полимеразы или связывания нуклеосом.
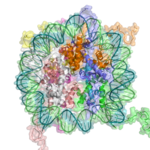 Рисунок нуклеосомы структура. Из PDB : 1KX5 .
Рисунок нуклеосомы структура. Из PDB : 1KX5 .Базовым повторяющимся элементом хроматина является нуклеосома, соединенная между собой участками линкерной ДНК, гораздо более короткое расположение, чем чистая ДНК в растворе.
В дополнение к коровым гистонам существует линкерный гистон H1, который контактирует с выходом / входом нити ДНК на нуклеосоме. Частица ядра нуклеосомы вместе с гистоном H1 известна как хроматосома. Нуклеосомы, содержащие примерно от 20 до 60 пар оснований линкерной ДНК, могут образовывать в нефизиологических условиях волокно размером примерно 10 нм «бусинки на нити». (Рис. 1-2)..
Нуклеосомы связывают ДНК неспецифически, как того требует их функция в общей упаковке ДНК. Однако существуют большие предпочтения последовательностей ДНК, которые определяют расположение нуклеосом. Это связано в первую очередь с различными физическими свойствами различных последовательностей ДНК: например, аденин и тимин более благоприятно сжаты во внутренних малых бороздках. Это означает, что нуклеосомы могут связываться преимущественно в одном положении примерно через каждые 10 пар оснований (спиральное повторение ДНК) - где ДНК поворачивается, чтобы максимизировать количество оснований A и T, которые будут находиться во внутренней малой бороздке. (См. механические свойства ДНК.)
 Две предложенные структуры 30-нанометрового хроматинового волокна.. Слева: 1 структура "соленоида" стартовой спирали.. Справа: 2 начала рыхлой спиральной структуры.. Примечание: гистоны на этой диаграмме опущены - показана только ДНК.
Две предложенные структуры 30-нанометрового хроматинового волокна.. Слева: 1 структура "соленоида" стартовой спирали.. Справа: 2 начала рыхлой спиральной структуры.. Примечание: гистоны на этой диаграмме опущены - показана только ДНК. С добавлением H1 структура бусинок на нити, в свою очередь, сворачивается в спиральную структуру диаметром 30 нм, известную как 30 нм волокно или нить. Точная структура хроматинового волокна в клетке подробно не известна, и до сих пор ведутся споры по этому поводу.
Считается, что этот уровень структуры хроматина представляет собой форму гетерохроматина, который содержит в основном транскрипционно молчащие гены. Исследования ЭМ (электронная микроскопия) продемонстрировали, что 30-нм волокно очень динамично, так что оно разворачивается в структуру 10-нм волокна («бусинки-на-нити») при пересечении РНК-полимеразой, участвующей в транскрипции.
 Четыре предложенных структуры филамента хроматина 30 нм с длиной повтора ДНК на нуклеосомы в диапазоне от 177 до 207 п.н.. Линкерная ДНК желтого цвета и нуклеосомная ДНК розового.
Четыре предложенных структуры филамента хроматина 30 нм с длиной повтора ДНК на нуклеосомы в диапазоне от 177 до 207 п.н.. Линкерная ДНК желтого цвета и нуклеосомная ДНК розового. Существующие модели обычно допускают, что нуклеосомы лежат перпендикулярно оси волокна, а линкерные гистоны расположены внутри. Стабильное 30-нм волокно основано на регулярном расположении нуклеосом вдоль ДНК. Линкерная ДНК относительно устойчива к изгибу и вращению. Это делает длину линкерной ДНК критической для стабильности волокна, требуя, чтобы нуклеосомы были разделены на длины, которые позволяют вращение и складывание в требуемую ориентацию без чрезмерной нагрузки на ДНК. С этой точки зрения, разная длина линкерной ДНК должна приводить к разным топологиям сворачивания хроматинового волокна. Недавняя теоретическая работа, основанная на изображениях реконструированных волокон с помощью электронной микроскопии, поддерживает эту точку зрения.
Пространственное расположение хроматина внутри ядра не случайно - специфические участки хроматина можно найти на определенных территориях. Территориями являются, например, lamina -ассоциированные домены (LAD) и топологически ассоциированные домены (TAD), которые связаны вместе белковыми комплексами. В настоящее время полимерные модели, такие как модель Strings Binders Switch (SBS) и модель Dynamic Loop (DL), используются для описания сворачивания хроматина внутри ядра.
 Кариограмма мужчины-человека с использованием окрашивания Гимза, демонстрирующая классическую метафазную структуру хроматина.
Кариограмма мужчины-человека с использованием окрашивания Гимза, демонстрирующая классическую метафазную структуру хроматина.  Конденсация и разрешение человеческого сестринские хроматиды в раннем митозе
Конденсация и разрешение человеческого сестринские хроматиды в раннем митозе Хроматин и его взаимодействие с ферментами были исследованы, а также Был сделан вывод, что это актуальный и важный фактор в экспрессии генов. Винсент Г. Олфри, профессор Университета Рокфеллера, заявил, что синтез РНК связан с ацетилированием гистонов. Аминокислота лизин, прикрепленная к концам гистонов, заряжена положительно. Ацетилирование этих хвостов сделает концы хроматина нейтральными, что обеспечит доступ ДНК.
Когда хроматин деконденсируется, ДНК открыта для проникновения молекулярных механизмов. Колебания между открытым и закрытым хроматином могут способствовать прерыванию транскрипции или взрыву транскрипции. Вероятно, вовлечены и другие факторы, такие как ассоциация и диссоциация комплексов факторов транскрипции с хроматином. Этот феномен, в отличие от простых вероятностных моделей транскрипции, может объяснить высокую вариабельность экспрессии генов, происходящую между клетками в изогенных популяциях.
Во время метазоа спермиогенез
Упаковка эукариотической ДНК в хроматин представляет собой барьер для всех Процессы на основе ДНК, которые требуют привлечения ферментов к участкам их действия. Чтобы разрешить критический клеточный процесс репарации ДНК, хроматин должен быть реконструирован. У эукариот АТФ-зависимые ремоделирующие хроматин комплексы и модифицирующие гистоны ферменты являются двумя преобладающими факторами, используемыми для осуществления этого процесса ремоделирования.
Релаксация хроматина происходит быстро в месте, где происходит восстановление повреждение ДНК. Этот процесс инициируется белком PARP1, который начинает появляться при повреждении ДНК менее чем за секунду, с половиной максимального накопления в течение 1,6 секунды после возникновения повреждения. Затем ремоделирующий хроматин Alc1 быстро присоединяется к продукту PARP1 и завершает прибытие к повреждению ДНК в течение 10 секунд после повреждения. Примерно половина максимальной релаксации хроматина, предположительно из-за действия Alc1, происходит через 10 секунд. Затем это позволяет задействовать фермент репарации ДНК MRE11, чтобы инициировать репарацию ДНК в течение 13 секунд.
γH2AX, фосфорилированная форма H2AX также участвует в первые шаги, ведущие к деконденсации хроматина после возникновения повреждения ДНК. Вариант гистона H2AX составляет около 10% гистонов H2A в хроматине человека. γH2AX (H2AX, фосфорилированный по серину 139) может быть обнаружен уже через 20 секунд после облучения клеток (с образованием двухцепочечного разрыва ДНК), а половина максимального накопления γH2AX происходит за одну минуту. Размер хроматина с фосфорилированным γH2AX составляет около двух миллионов пар оснований в месте двухцепочечного разрыва ДНК. γH2AX сам по себе не вызывает деконденсацию хроматина, но в течение 30 секунд после облучения белок RNF8 может быть обнаружен в ассоциации с γH2AX. RNF8 опосредует обширную деконденсацию хроматина посредством его последующего взаимодействия с CHD4, компонентом ремоделирования нуклеосом и деацетилазного комплекса NuRD.
После релаксации после повреждения ДНК с последующей репарацией ДНК хроматин восстанавливается до состояния уплотнения, близкого к уровню до повреждения, примерно через 20 мин.
Было загадкой, как деконденсированные интерфазные хромосомы остаются по существу незаузленными. Естественное ожидание состоит в том, что в присутствии топоизомераз ДНК типа II, которые допускают проходы двухцепочечных участков ДНК друг через друга, все хромосомы должны достичь состояния топологического равновесия. Топологическое равновесие в сильно переполненных интерфазных хромосомах, образующих хромосомные территории, должно приводить к образованию сильно узловатых волокон хроматина. Однако методы захвата конформации хромосом (3C) показали, что разрушение контактов с геномным расстоянием в интерфазных хромосомах практически такое же, как в смятом состоянии глобулы, которое образуется, когда длинные полимеры конденсируются без образования каких-либо узлов. Чтобы удалить узлы из сильно переполненного хроматина, потребуется активный процесс, который должен не только обеспечивать энергию для вывода системы из состояния топологического равновесия, но также направлять опосредованные топоизомеразой отрывки таким образом, чтобы узлы были эффективно развязаны вместо делая узлы еще более сложными. Было показано, что процесс экструзии петли хроматина идеально подходит для активного развязывания волокон хроматина в интерфазных хромосомах.
Термин, введенный Вальтером Флеммингом, имеет несколько значений:
Первое определение позволяет определять «хроматины» в других сферах жизни, таких как бактерии и археи, с использованием любых ДНК-связывающих белков, которые конденсируют молекулу. Эти белки обычно относят к ассоциированным с нуклеоидом белкам (NAP); примеры включают AsnC / LrpC с HU. Кроме того, некоторые археи действительно производят нуклеосомы из белков, гомологичных эукариотическим гистонам.
Следующие ученые были отмечены за свой вклад в исследования хроматина Нобелевскими премиями :
| Год | Who | Премия |
|---|---|---|
| 1910 | Альбрехт Коссель (Гейдельбергский университет) | Нобелевская премия по физиологии и медицине за открытие пяти ядерных основания: аденин, цитозин, гуанин, тимин и урацил. |
| 1933 | Thomas Hunt Morgan (Калифорнийский технологический институт) | Нобелевская премия по физиологии и медицине за открытия роли гена и хромосомы в наследственности, основанные на его исследованиях белоглазой мутации у плодовой мухи Drosophila. |
| 1962 | Фрэнсис Крик, Джеймс Уотсон и Морис Уилкинс (Лаборатория молекулярной биологии MRC, Гарвардский и Лондонский университет соответственно) | Нобелевская премия в физиологии ogy or Medicine за открытие двойной спиральной структуры ДНК и ее значение для передачи информации в живом материале. |
| 1982 | Аарон Клуг (Лаборатория молекулярной биологии MRC) | Нобелевская премия по химии «за разработку кристаллографической электронной микроскопии и структурное объяснение биологически важных комплексов нуклеиновая кислота-белок» |
| 1993 | Ричард Дж. Робертс и Филип А. Шарп | Нобелевская премия по физиологии «за независимые открытия расщепленных генов », в которых Участки ДНК, называемые экзонами, экспрессируют белки и прерываются участками ДНК, называемыми интронами, которые не экспрессируют белки. |
| 2006 | Роджер Корнберг (Стэнфордский университет) | Нобелевская премия по химии за открытие механизма, с помощью которого ДНК транскрибируется в информационную РНК. |