 | |
 | |
 | |
| Имена | |
|---|---|
| Предпочтительное название IUPAC N, N '-дициклогексилметандиимин | |
| Другие имена Дициклогексилметандиимин N, N '-Дициклогексилкарбодиимид DCC, DCCD, DCCI | |
| Идентификаторы | |
| Количество CAS | |
| 3D модель ( JSmol ) | |
| Ссылка на Beilstein | 610662 |
| ЧЭБИ | |
| ЧЭМБЛ | |
| ChemSpider | |
| ECHA InfoCard | 100.007.914 |
| Номер ЕС | |
| Ссылка на Гмелин | 51651 |
| PubChem CID | |
| Номер RTECS | |
| UNII | |
| Номер ООН | 2811 |
| Панель управления CompTox ( EPA) | |
ИнЧИ
| |
Улыбки
| |
| Характеристики | |
| Химическая формула | C 13 H 22 N 2 |
| Молярная масса | 206,333 г моль -1 |
| Появление | белый кристаллический порошок |
| Плотность | 1,325 г / см 3, твердый |
| Температура плавления | 34 ° С (93 ° F, 307 К) |
| Точка кипения | 122 ° С (252 ° F, 395 К) (при 6 мм рт. Ст.) |
| Растворимость в воде | не растворим |
| Опасности | |
| Пиктограммы GHS |    |
| Сигнальное слово GHS | Опасность |
| Формулировки опасности GHS | H302, H311, H317, H318 |
| Меры предосторожности GHS | Р261, Р264, Р270, P272, P280, P301 + 312, P302 + 352, P305 + 351 + 338, P310, P312, P321, P322, P330, P333 + 313, P361, P363, P405, P501 |
| NFPA 704 (огненный алмаз) |  3 1 3 1 |
| точка возгорания | 113 ° С (235 ° F, 386 К) |
| Родственные соединения | |
| Родственные карбодиимиды | DIC, EDC |
| Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| | |
| Ссылки на инфобоксы | |
N, N '-Дициклогексилкарбодиимид ( DCC или DCCD) представляет собой органическое соединение с химической формулой (C 6 H 11 N) 2 C. Это воскообразное белое твердое вещество со сладким запахом. Его основное использование - соединение аминокислот во время искусственного синтеза пептидов. Низкая температура плавления этого материала позволяет плавить его, что упрощает обращение с ним. Он хорошо растворяется в дихлорметане, тетрагидрофуране, ацетонитриле и диметилформамиде, но не растворяется в воде.
Ядро карбодиимидов CN = C = NC (N = C = N) является линейным и связано со структурой аллена. Молекула имеет идеализированную симметрию C 2.
Фрагмент N = C = N дает характерную ИК-спектроскопическую сигнатуру при 2117 см -1. В 15 Н ЯМР спектр показывает характерный сдвиг 275 м.д. Апфилд азотной кислоты и 13 C - ЯМР - спектр имеет пик при примерно 139 частей на миллион относительно тетраметилсилана TMS.
ДКК производится декарбоксилированием циклогексила изоцианата с использованием оксидов фосфина в качестве катализатора:
Альтернативные катализаторы этого превращения включают высоконуклеофильный OP (MeNCH 2 CH 2) 3 N.
Академический интерес, ацетат палладия, йод и кислород к паре циклогексиламина и циклогексил изоцианида. При использовании этого маршрута достигнута урожайность до 67%:
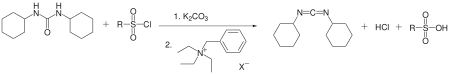
DCC также получали из дициклогексилмочевины с использованием катализатора межфазного переноса. Дизамещенная мочевина, аренсульфонилхлорид и карбонат калия реагируют в толуоле в присутствии бензилтриэтиламмонийхлорида с образованием DCC с выходом 50%.
DCC представляет собой дегидратирующий агент для получения амидов, кетонов и нитрилов. В этих реакциях DCC гидратируется с образованием дициклогексилмочевины (DCU), соединения, которое практически нерастворимо в большинстве органических растворителей и нерастворимо в воде. Таким образом, большая часть DCU легко удаляется фильтрацией, хотя последние следы трудно удалить из неполярных продуктов. DCC также можно использовать для обращения вторичных спиртов. При этерификации по Стеглиху спирты, включая даже некоторые третичные спирты, могут быть этерифицированы с использованием карбоновой кислоты в присутствии DCC и каталитического количества DMAP.
При синтезе белка (например, в твердотельных синтезаторах Fmoc ) N-конец часто используется в качестве сайта присоединения, к которому добавляются мономеры аминокислот. Для повышения электрофильность из карбоксилатной группы, отрицательно заряженный кислород должен первым быть «активирован» в более уходящую группу. Для этого используется DCC. Отрицательно заряженный кислород будет действовать как нуклеофил, атакуя центральный углерод в DCC. DCC временно присоединяется к бывшей карбоксилатной группе, образуя высокоэлектрофильный промежуточный продукт, что делает нуклеофильную атаку концевой аминогруппы на растущий пептид более эффективной.
В сочетании с диметилсульфоксидом (ДМСО) DCC вызывает окисление Пфицнера-Моффатта. Эта процедура используется для окисления спиртов до альдегидов и кетонов. В отличие от опосредованного металлами окисления, такого как окисление Джонса, условия реакции достаточно мягкие, чтобы избежать чрезмерного окисления альдегидов до карбоновых кислот. Обычно трем эквивалентам DCC и 0,5 эквивалента источника протонов в ДМСО дают возможность реагировать в течение ночи при комнатной температуре. Реакцию гасят кислотой.
DCC - классический ингибитор АТФ-синтазы. ДКК ингибирует АТФ - синтазы путем связывания с одним из гр субъединиц и вызывает пространственное затруднение вращения в F O субъединицей.
DCC - сильный аллерген и сенсибилизатор, часто вызывающий кожную сыпь.