 | |
 | |
| Клинические данные | |
|---|---|
| Торговые наименования | Mozobil |
| Другие названия | JM 3100, AMD3100 |
| AHFS / Drugs.com | Монография |
| MedlinePlus | a609018 |
| Данные лицензии |
|
| Беременность. категория |
|
| Способы введения. | Подкожная инъекция |
| Код ATC | |
| Правовой статус | |
| Правовой статус |
|
| Фармакокинетические данные | |
| Связывание с белками | До 58% |
| Метаболизм | Нет |
| Период полувыведения | 3-5 часов |
| Выведение | Почки |
| Идентификаторы | |
IUPAC имя
| |
| Номер CAS | |
| PubChem CID | |
| IUPHAR / BPS | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| ChEBI | |
| ChEMBL |
|
| CompTox Dashboard (EPA ) | |
| Химические и физические данные | |
| Формула | C28H54N8 |
| Молярная масса | 502,796 г · моль |
| 3D-модель (JSmol ) | |
УЛЫБКИ
| |
InChI
| |
| (что это?) | |
Plerixafor (INN и USAN, торговое наименование Mozobil ) является иммуностимулятор, используемый для мобилизации гемопоэтических стволовых клеток у онкологических больных в кровоток. Затем стволовые клетки извлекаются из крови и трансплантируются обратно пациенту. Препарат был разработан AnorMED, который впоследствии был куплен Genzyme.
Мобилизация стволовых клеток периферической крови, которая важна как источник гемопоэтические стволовые клетки для трансплантации, как правило, выполняется с использованием гранулоцитарного колониестимулирующего фактора (G-CSF), но неэффективен примерно у 15-20% пациентов. Комбинация G-CSF с Plerixafor увеличивает процент людей, которые реагируют на терапию и производят стволовые клетки в количестве, достаточном для трансплантации. Препарат разрешен для лечения пациентов с лимфомой и множественной миеломой.
Исследования на беременных животных показали тератогенное действие эффекты. Поэтому плериксафор противопоказан беременным женщинам, за исключением критических случаев. Фертильные женщины обязаны использовать противозачаточные средства. Неизвестно, выделяется ли препарат в грудное молоко. Во время терапии следует прекратить грудное вскармливание.
Тошнота, диарея и местные реакции наблюдались более чем у 10% пациентов. Другие проблемы с пищеварением и общие симптомы, такие как головокружение, головная боль и мышечная боль, также относительно распространены; они были обнаружены более чем у 1% пациентов. Аллергия возникает менее чем в 1% случаев. Большинство побочных эффектов в клинических испытаниях были легкими и преходящими.
Европейское агентство по лекарственным средствам перечислило ряд проблем безопасности, которые необходимо оценить на постмаркетинговой основе, в первую очередь теоретические возможности селезенка разрыв и мобилизация опухолевых клеток. Первая проблема возникла потому, что в исследованиях на животных наблюдалась спленомегалия, а в редких случаях G-CSF может вызывать разрыв селезенки. Мобилизация опухолевых клеток произошла у пациентов с лейкемией, получавших плериксафор.
Исследования взаимодействия не проводились. Тот факт, что плериксафор не взаимодействует с системой цитохрома, указывает на низкий потенциал взаимодействия с другими лекарственными средствами.
В виде комплекса цинка, plerixafor действует как антагонист (или, возможно, более точно частичный агонист ) альфа хемокинового рецептора CXCR4 и аллостерический агонист CXCR7. Рецептор CXCR4 альфа- хемокина и один из его лигандов, SDF-1, важны в гемопоэтических стволовых клетках, возвращающихся к костный мозг и в гемопоэтические стволовые клетки покой. Эффект in vivo плериксафора в отношении убиквитина, альтернативного эндогенного лиганда CXCR4, неизвестен. Было обнаружено, что плериксафор является сильным индуктором мобилизации гемопоэтических стволовых клеток из костного мозга в кровоток в виде стволовых клеток периферической крови. Кроме того, плериксафор подавляет экспрессию CD20 на В-клетках, влияя на ось CXCR4 / SDF1, которая регулирует его экспрессию.
После подкожной инъекции, Plerixafor быстро всасывается, и пиковые концентрации достигаются через 30-60 минут. До 58% связывается с белками плазмы, остальное в основном находится во внесосудистых отсеках. Препарат не метаболизируется в значительных количествах; не обнаружено взаимодействия с ферментами цитохрома P450 или P-гликопротеинами. Период полураспада в плазме составляет от 3 до 5 часов. Плериксафор выводится через почки, при этом 70% препарата выводится в течение 24 часов.
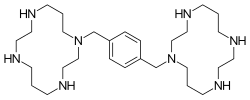
Плериксафор представляет собой макроциклическое соединение и производное би циклама, причем кольца циклама связаны по атомам азота амина через 1,4- ксилил спейсер. Это сильная база ; все восемь атомов азота легко принимают протоны. Два макроциклических кольца образуют хелатные комплексы с ионами двухвалентных металлов, особенно с цинком, медью и никелем, а также с кобальтом. и родий. Биологически активной формой плериксафора является его цинковый комплекс.
Три из четырех атомов азота макроциклациклама (1,4,8,11-тетраазациклотетрадекан) защищены с помощью тозильные группы. Продукт обрабатывают 1,4-бис (бромметил) бензолом и карбонатом калия в ацетонитриле. После отщепления тозильных групп с помощью бромистоводородной кислоты получают плериксафор октагидробромид.
Молекула была впервые синтезирована в 1987 году для проведения основных исследований редокс химия диметаллических координационных соединений. Затем, по счастливой случайности другим химиком было обнаружено, что такая молекула может иметь потенциальное применение для лечения ВИЧ из-за ее роли в блокировании CXCR4, рецептора хемокина, который действует как корецептор для определенные штаммы ВИЧ (наряду с основным клеточным рецептором вируса, CD4). Разработка этого показания была прекращена из-за недостаточной пероральной доступности и сердечных нарушений. Дальнейшие исследования привели к новому показанию для онкологических больных.
Plerixafor имеет статус орфанного препарата в США и Европейском Союзе для мобилизации гемопоэтические стволовые клетки. Он был одобрен Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) для этого показания 15 декабря 2008 г. В Европейском Союзе препарат был одобрен после положительного отзыва Комитета по лекарственным средствам для человека отчет об оценке 29 мая 2009 г. Препарат был одобрен для использования в Канаде Health Canada 8 декабря 2011 г.
В нескольких исследованиях было показано, что Plerixafor уменьшает метастазирование у мышей. Также было показано, что он снижает рецидив глиобластомы на мышиной модели после лучевой терапии. В этой модели раковые клетки, которые пережили облучение, критически зависели от клеток, полученных из костного мозга, для васкулогенеза, и рекрутирование последних опосредовано взаимодействиями SDF-1 CXCR4, которые блокируются плериксафором.
Исследователи Имперского колледжа продемонстрировали, что плериксафор в сочетании с фактором роста эндотелия сосудов (VEGF) может мобилизовать мезенхимальные стволовые клетки и эндотелиальные клетки-предшественники в периферическую кровь мышей.
В двойном слепом рандомизированном плацебо-контролируемом исследовании мобилизация стволовых клеток с помощью Plerixafor не улучшила заживление ишемических диабетических ран.
Блокада передачи сигналов CXCR4 с помощью плериксафора также неожиданно оказалась эффективной для противодействия индуцированной опиоидами гипералгезии, вызванной длительным лечением морфин, хотя пока проводились только исследования на животных.