| |||
 | |||
| Имена | |||
|---|---|---|---|
| Предпочтительное имя IUPAC Циклопента-1,3-диен | |||
| Другие имена 1,3-Циклопентадиен. Пиропентилен | |||
| Идентификаторы | |||
| Номер CAS | |||
| 3D-модель (JSmol ) | |||
| Аббревиатуры | CPD, HCp | ||
| Ссылка Beilstein | 471171 | ||
| ChEBI | |||
| ChemSpider | |||
| ECHA InfoCard | 100.008.033 | ||
| Номер EC |
| ||
| Справочник Гмелина | 1311 | ||
| MeSH | 1,3-циклопентадиен | ||
| PubChem CID | |||
| номер RTECS |
| ||
| UNII | |||
| Панель управления CompTox (EPA ) | |||
InChI
| |||
УЛЫБКИ
| |||
| Свойства | |||
| Химическая формула | C5H6 | ||
| Молярная масса | 66,103 г · моль | ||
| Внешний вид | Бесцветный жидкость | ||
| Запах | раздражающий, терпен -подобный | ||
| Плотность | 0,786 г см | ||
| Точка плавления | -90 ° C; -130 ° F; 183 K | ||
| Температура кипения | от 39 до 43 ° C; От 102 до 109 ° F; От 312 до 316 K | ||
| Растворимость в воде | нерастворимый | ||
| Давление пара | 400 мм рт. Ст. (53 кПа) | ||
| Кислотность (pK a) | 16 | ||
| Основание конъюгата | Циклопентадиенил анион | ||
| Магнитная восприимчивость (χ) | -44,5 × 10 см моль | ||
| Структура | |||
| Молекулярная форма | Планарная | ||
| Термохимия | |||
| Теплоемкость (C) | 115,3 Дж · К моль | ||
| Стандартная молярная. энтропия (S 298) | 182,7 Дж · К · моль | ||
| Опасности | |||
| Температура вспышки | 25 ° C (77 ° F; 298 K) | ||
| Смертельная доза или концентрация (LD, LC): | |||
| LC50(средняя концентрация ) | 14,182 частей на миллион (крыса, 2 часа). 5091 частей на миллион (мышь, 2 часа) | ||
| NIOSH (пределы воздействия на здоровье в США): | |||
| PEL (допустимо) | TWA 75 ppm (200 мг / м) | ||
| REL (рекомендуется) | TWA 75 ppm (200 мг / м) | ||
| IDLH (Непосредственная опасность) | 750 ppm | ||
| Родственные соединения | |||
| Родственные углеводороды | Бензол. Циклобутадиен. Циклопентен | ||
| Родственные соединения | Дициклопентадиен | ||
| Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки в ink | |||
Циклопентадиен представляет собой органическое соединение с формулой C5H6. Его часто обозначают сокращенно CpH, потому что циклопентадиенильный анион сокращенно обозначается Cp.
Эта бесцветная жидкость имеет сильный неприятный запах. При комнатной температуре этот циклический диен димеризуется в течение нескольких часов с образованием дициклопентадиена посредством реакции Дильса-Альдера. Этот димер может быть восстановлен путем нагревания с образованием мономера.
Соединение в основном используется для производства циклопентена и его производных. Он широко используется в качестве предшественника циклопентадиенильного аниона (Cp), важного лиганда в циклопентадиенильных комплексах в металлоорганической химии.
 Циклопентадиеновый мономер в ледяной бане
Циклопентадиеновый мономер в ледяной бане Производство циклопентадиена обычно не отличается от дициклопентадиена, поскольку они взаимно превращаются. Их получают из каменноугольной смолы (около 10–20 г / т) и парового крекинга нафты (около 14 кг / т). Чтобы получить циклопентадиеновый мономер, коммерческий дициклопентадиен крекируется при нагревании примерно до 180 ° C. Мономер собирают перегонкой и используют вскоре после этого.
Атомы водорода в циклопентадиене претерпевают быстрые [1,5] -сигматропные сдвиги, как показано Спектры ЯМР, записанные при различных температурах. Еще более текучими являются производные C 5H5E (CH 3)3(E = Si, Ge, Sn ), в которых более тяжелый элемент мигрирует от углерода к углероду с низким активационным барьером.
Циклопентадиен является высокореакционноспособным диеном в реакции Дильса – Альдера, поскольку для достижения геометрической формы оболочки требуется минимальное искажение диена переходное состояние по сравнению с другими диенами. Известно, что циклопентадиен димеризуется. Превращение происходит в течение часов при комнатной температуре, но мономер может храниться в течение нескольких дней при -20 ° C.
Соединение является необычно кислым (pK a = 16) для углеводорода, что объясняется высокой стабильностью ароматического циклопентадиенила анион, C. 5H. 5. Депротонирование может быть достигнуто с помощью различных оснований, обычно гидрида натрия, металлического натрия и бутиллития. Соли этого аниона коммерчески доступны, включая циклопентадиенид натрия и циклопентадиенид лития. Они используются для получения циклопентадиенильных комплексов.
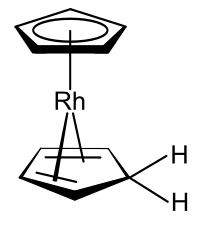 [(η-C 5H5) Rh (η-C 5H6)], 18-электронная смешанная- гаптичность производное родоцена, которое может образовываться при протонировании мономера родоцена.
[(η-C 5H5) Rh (η-C 5H6)], 18-электронная смешанная- гаптичность производное родоцена, которое может образовываться при протонировании мономера родоцена. Металлоцены и родственные циклопентадиенильные производные были тщательно исследованы и представляют собой краеугольный камень металлоорганической химии благодаря их высокой стабильности. Первый охарактеризованный металлоцен, ферроцен, был получен таким же образом, как и многие другие металлоцены: путем объединения производных щелочных металлов в форме MC 5H5с дигалогенидами переходных металлов : как обычно Например, никелоцен образуется при обработке хлорида никеля (II) циклопентадиенидом натрия в THF.
металлоорганические комплексы, которые включают как циклопентадиенильный анион, так и сам циклопентадиен, одним из примеров которых является производное родоцена, полученное из мономера родоцена в протонных растворителях.
Он был исходным материалом для Лео Пакета синтеза додекаэдрана в 1982 году. Первая стадия включала восстановительную димеризацию молекулы с образованием дигидрофулвалена, а не простое добавление для получения дициклопентадиена.
 Начало синтеза додекаэдрана Пакеттом в 1982 г. Обратите внимание на димеризацию циклопа энтадиен на стадии 1 в дигидрофулвален.
Начало синтеза додекаэдрана Пакеттом в 1982 г. Обратите внимание на димеризацию циклопа энтадиен на стадии 1 в дигидрофулвален. Помимо использования в качестве предшественника катализаторов на основе циклопентадиенила, основным коммерческим применением циклопентадиена является его использование в качестве предшественника сомономеров. Полугидрогенизация дает циклопентен. Реакция Дильса-Альдера с бутадиеном дает этилиденнорборнен, сомономер в производстве каучуков EPDM.
 Структура tBu 3C5H3, прототип объемный циклопентадиен.
Структура tBu 3C5H3, прототип объемный циклопентадиен.Циклопентадиен может замещать один или несколько атомов водорода, образуя производные с ковалентными связями:
Большинство этих замещенных циклопентадиенов могут также образовывать анионы и присоединяться к циклопентадиенильным комплексам.