| Атипичная тератоидная рабдоидная опухоль | |
|---|---|
 | |
| МРТ AT / RT | |
| Специальность | Онкология |
атипичная тератоидная рабдоидная опухоль (AT / RT ) - это редкая опухоль, обычно диагностируемая в детстве. Хотя обычно это опухоль головного мозга, AT / RT может возникать где угодно в центральной нервной системе (ЦНС), включая спинной мозг. Около 60% будет в задней черепной ямке (особенно в мозжечке ). Один обзор оценил 52% в задней черепной ямке, 39% - это супратенториальные примитивные нейроэктодермальные опухоли (sPNET), 5% - в пинеальной железе, 2% - спинномозговая, а 2% - мультифокальные.
В Соединенных Штатах ежегодно диагностируется трое детей на 1 000 000 или около 30 новых случаев AT / RT. AT / RT составляет около 3% детских раковых заболеваний ЦНС. Около 17% всех онкологических заболеваний у детей поражает ЦНС, что делает эти виды рака наиболее распространенной солидной опухолью у детей. Выживаемость при опухолях ЦНС составляет около 60%. Рак головного мозга у детей является второй по значимости причиной смерти от рака у детей сразу после лейкемии. Последние тенденции предполагают, что частота общей диагностики опухолей ЦНС увеличивается примерно на 2,7% в год. По мере того, как методы диагностики с использованием генетических маркеров улучшаются и используются все чаще, ожидается, что доля диагнозов AT / RT будет расти.
AT / RT была признана юридическим лицом только в 1996 году и добавлена к Всемирной организации здравоохранения Классификация опухолей головного мозга в 2000 году (степень IV). Относительно недавняя классификация и редкость способствовали первоначальному ошибочному диагнозу и неоптимальной терапии. Это привело к исторически плохому прогнозу.
Текущие исследования сосредоточены на использовании химиотерапевтических протоколов, эффективных против рабдомиосаркомы в сочетании с хирургическим вмешательством и лучевой терапией.
Недавние исследования с использованием мультимодальной терапии показали значительно улучшенные данные о выживаемости. В 2008 году Институт рака Дана-Фарбер в Бостоне сообщил о двухлетней общей выживаемости 53% и бессобытийной выживаемости 70% (средний возраст при постановке диагноза - 26 месяцев). В 2013 году Венский медицинский университет сообщил, что пятилетняя общая выживаемость составила 100%, а выживаемость без событий - 89% (средний возраст при постановке диагноза - 24 месяца).
Показатели выживаемости могут быть значительно улучшены, если Правильный генетический диагноз ставится в самом начале, после чего назначается специальное мультимодальное лечение.
Клинические признаки и симптомы зависят от местоположения опухоли.
Поскольку многие опухоли возникают в задней черепной ямке, они проявляются, как и другие опухоли задней черепной ямки, часто с головной болью, рвотой, летаргией и атаксией (шаткая походка). Сообщалось о случае семимесячного ребенка с первичной опухолью позвоночника, которая проявлялась прогрессирующей параплегией и ненормальным ощущением в ногах.
Генетическое сходство было обнаружено внутри рабдоидных опухолей. В частности, делеция хромосомы 22 очень распространена в AT / RT. Область хромосомы 22 содержит hSNF5 / INI1 ген, который, по-видимому, функционирует как классический ген-супрессор опухоли. Большинство рабдоидных опухолей имеют делеции INI1 независимо от того, происходят ли они в ЦНС, почках или где-либо еще. Эта мутация рассматривается как «первый удар», который предрасполагает детей к злокачественным новообразованиям. INI1 / hSNF5, компонент ремоделирующего хроматин комплекса SWI / SNF, является критическим опухолевым супрессором, биаллельно инактивированным в рабдоидных опухолях. Идентификация INI1 как опухолевого супрессора облегчила точную диагностику рабдоидных опухолей.
Скорость транскрипции для комплексов SWI / SNF и HDAC, по-видимому, регулируется геном INI1. Комплекс SWI / SNF играет роль в ремоделировании хроматина. AT / RT - первая опухоль головного мозга у детей, для которой был идентифицирован ген-супрессор опухоли. Мутация или делеция в гене INI1 / hSNF5 встречается в большинстве опухолей AT / RT. До 90% случаев AT / RT связаны с делецией 22 хромосомы. В основном это точечные мутации в гене hSNF5 / INI1 (т. Е. Можно диагностировать AT / RT без делеции 22 хромосомы в другом месте). Ген hSNF5 / INI1 регулирует около 15 белков в структуре хроматина. Кроме того, ген OPN имеет более высокую экспрессию в опухолях AT / RT. Считается, что все виды рака AT / RT не связаны с геном hSNF5 / INI1, поскольку 14 дополнительных белков в структуре хроматина контролируются другими генами. Существуют также некоторые новые мышиные модели рака AT / RT, а также экспериментальные клеточные линии, полученные из опухолей. Несмотря на эти достижения, функция гена еще не изучена. Недостаточно известно о функции INI1, будь то независимый модулятор экспрессии гена или его связь с комплексом SWI / SNF, чтобы можно было использовать конкретные целевые биологические агенты для лечения. Проспективные клинические и биологические исследования крайне необходимы для понимания эффективности терапевтических вмешательств, а также роли гена.
Атипичные тератоидные / рабдоидные опухоли очень редки, а абсолютный риск для братьев и сестер в литературе не описан. Однако существуют сообщения о том, что AT / RT присутствуют у двух членов одной семьи или у одного члена семьи с AT / RT, а у другого - почечной рабдоидной опухоли или другой опухоли ЦНС. Предполагается, что они возникли в результате генетических мутаций зародышевой линии у родителя, общего у затронутых братьев и сестер.
AT / RT и рабдоидный опухоль имеет термин «рабдоидная», потому что под микроскопом обе опухоли напоминают рабдомиосаркому.
 AT / RT Гистология с множеством рабдоидных опухолевых клеток
AT / RT Гистология с множеством рабдоидных опухолевых клеток 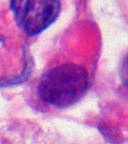 Рабдоидная опухолевая клетка - увеличение 400X
Рабдоидная опухолевая клетка - увеличение 400X Опухоль гистопатология состоит из мелких и крупных клеток. ткань этой опухоли содержит множество различных типов клеток, включая рабдоидные клетки, большие веретенообразные клетки, эпителиальные и мезенхимальные клетки, а также области, напоминающие примитивную нейроэктодермальную опухоль ( PNET). До 70% опухоли может состоять из PNET-подобных клеток. Ультраструктура характерные завитки промежуточных филаментов видны в рабдоидных опухолях (как и в случае рабдоидных опухолей в любой области тела). Хо и соавторы обнаружили серповидные охватывающие клетки, о чем ранее не сообщалось, во всех 11 случаях AT / RT.
 Иммуногистохимия для INI1, продукта гена SMARCB1, обычно дефектного в AT / RT: Обратите внимание на потерю коричневого окрашивания в ядрах опухолевых клеток с дефектным SMARCB1 по сравнению с сохраняющимся окрашиванием ядер сосудистых клеток (внутренний положительный контроль).
Иммуногистохимия для INI1, продукта гена SMARCB1, обычно дефектного в AT / RT: Обратите внимание на потерю коричневого окрашивания в ядрах опухолевых клеток с дефектным SMARCB1 по сравнению с сохраняющимся окрашиванием ядер сосудистых клеток (внутренний положительный контроль). Иммуногистохимическое окрашивание широко используется в диагностике и лечении рака. Специфические молекулярные маркеры характерны для определенных типов рака. Иммуногистохимия также широко используется в фундаментальных исследованиях для понимания распределения и локализации биомаркеров в различных частях ткани. Белки, обнаруженные в ATeratoid / RT:
Цитогенетика - исследование генетической структуры опухоли -вверх. Флуоресцентная гибридизация in situ может помочь найти мутацию или аномалию, которая может способствовать росту опухоли. Было показано, что этот метод полезен для идентификации некоторых опухолей и различения двух гистологически похожих опухолей друг от друга (таких как AT / RT и PNET). В частности, медуллобластмы / PNET могут быть цитогенетически дифференцированы от AT / RT, поскольку хромосомные делеции 17p относительно обычны для медуллобластомы, а аномалии 22q11.2 не наблюдаются. Однако делеции хромосомы 22 очень распространены при AT / RT.
Подчеркивается важность гена hSNF5 / INI1, расположенного на хромосомной полосе 22q11.2, поскольку наличие мутации достаточно для изменения диагноза с медуллобластомы или PNET на более агрессивную классификацию AT / RT. Однако в 100% случаев эта мутация отсутствует. Следовательно, если мутация не присутствует в классическом иммуногистохимическом и морфологическом паттерне AT / RT, тогда диагноз остается AT / RT.
Стандартное обследование при АТ / ЛТ включает:
Первоначальный диагноз опухоли ставится с помощью рентгенологического исследования (МРТ или CT -). Если сначала была проведена КТ, обычно выполняется МРТ, поскольку изображения часто более подробны и могут выявить ранее необнаруженные метастатические опухоли в других частях мозга. Кроме того, обычно выполняется МРТ позвоночника. Опухоль AT / RT часто распространяется на позвоночник. AT / RT сложно диагностировать только на основании рентгенологического исследования; Обычно патолог должен провести цитологический или генетический анализ.
Исследование спинномозговой жидкости важно (CSF), так как у одной трети пациентов будет внутричерепное диссеминация с вовлечением CSF. Крупные опухолевые клетки, эксцентриситет ядер и выступающие ядрышки - последовательные результаты. Обычно только небольшая часть биопсий AT / RT содержит рабдоидные клетки, что затрудняет диагностику. Все чаще рекомендуется проводить генетический анализ опухоли головного мозга, особенно для определения наличия делеции в гене INI1 / hSNF5 (по всей видимости, это составляет более 80% случаев). Правильный диагноз опухоли имеет решающее значение для любого протокола. Исследования показали, что от 8% до более 50% опухолей AT / RT диагностируются неправильно.
AT / RT может быть связана с злокачественной рабдоидной опухолью (MRT), который возникает вне ЦНС, обычно в почках. Обнаружение того, что AT / RT и MRT имеют делеции гена INI1, указывает на то, что рабдоидные опухоли почек и мозга, по крайней мере, тесно связаны. AT / RT и MRT также имеют схожую гистологию и сходные клинические и демографические особенности. Более того, 10–15% пациентов с МРТ имеют одновременные или последующие опухоли головного мозга, многие из которых являются вторичными или первичными.
Критическим шагом в планировании лечения является определение правильной гистологии опухоли. Неправильная идентификация гистологии опухоли может привести к ошибкам в лечении и прогнозе.
Атипичная тератоидная / рабоидная опухоль очень похожа на медуллобластому, примитивную нейроэктодермальную опухоль, карциному сосудистого сплетения и некоторые виды опухолей зародышевых клеток. Поскольку рабдоидные характеристики не являются единственным компонентом AT / RT, некоторые участки AT / RT могут напоминать другие опухоли. Эти характеристики могут присутствовать только в фокусных областях или могут быть менее выраженными.
Рассмотрение AT / RT при подозрении на медуллобластому или PNET важно, особенно у детей в возрасте до одного года. Цитогенетические исследования могут помочь дифференцировать MB / PNET от AT / RT. Некоторые виды опухолей зародышевых клеток выделяют опухолевые маркеры AFP или bHCG ; AT / RT - нет.
AT / RT может произойти в любом месте в ЦНС; однако около 60% находятся в задней ямке или области мозжечка. Исследование ASCO показало 52% задней черепной ямки; 39% sPNET; 5% шишковидная железа ; 2% спинномозговых и 2% мультифокальных.
Внешний вид опухолей на КТ и МРТ неспецифичен, имеет тенденцию к большим размерам, кальцификации, некроз (отмирание тканей) и кровоизлияние (кровотечение). Сами по себе радиологические исследования не могут идентифицировать AT / RT; патолог почти всегда должен оценить образец ткани мозга.
Повышенная клеточность опухоли может показаться на КТ без искажений с повышенным ослаблением. Солидные части опухоли часто усиливаются при контрастном обнаружении МРТ на T1 и T2 взвешенных изображениях. Предконтрастные T2-взвешенные изображения могут показывать изосигнал или слегка гиперсигнал. Твердые компоненты опухоли могут усиливаться контрастом, но не всегда. МРТ-исследования, по-видимому, более способны выявить метастатические очаги в других внутричерепных, а также внутриспинальных местах.
Предоперационные и последующие исследования необходимы для выявления метастазов.
Хирургия играет решающую роль в получении ткани для постановки точного диагноза. Сама по себе операция не лечит. Кроме того, 30% AT / RT расположены супратенториально, и существует склонность к мозжечковому углу, что затрудняет хирургическую резекцию. У одной трети или более детей на момент постановки диагноза будет диссеминированное заболевание. Тотальная или почти полная резекция часто невозможна.
Около 50% AT / RT дает временный ответ, но химиотерапия сама по себе редко бывает лечебной. Стандартное лечение AT / RT неизвестно. Различные химиотерапевтические агенты применялись против AT / RT, которые также используются против других опухолей ЦНС, включая цисплатин, карбоплатин, циклофосфамид, винкристин и этопозид. Некоторые режимы химиотерапии перечислены ниже:
Традиционная практика лечения опухолей головного мозга у детей заключалась в использовании химиотерапии и откладывании лучевой терапии до тех пор, пока ребенок не достигнет возраста трех лет. Эта стратегия основана на наблюдениях за детьми в возрасте до трех лет, у которых в результате облучения головного мозга наблюдаются серьезные долгосрочные осложнения. Однако отдаленные результаты ПТ / ЛТ настолько плохи, что некоторые протоколы требуют предварительной лучевой терапии, часто, несмотря на молодой возраст.
Доза и объем облучения не были стандартизированы, но радиация требует похоже, улучшают выживаемость. Использование излучения у детей младше трех лет ограничено из-за риска серьезных нейрокогнитивных нарушений. Чтобы вылечить эту опухоль, используются протоколы, использующие конформное локальное излучение у маленьких детей.
Внешний луч (конформное) излучение использует несколько лучей, которые пересекаются в месте расположения опухоли; нормальная ткань головного мозга получает меньше излучения, и когнитивные функции тем самым менее страдают.
Облучение протонным пучком предлагалось только в Массачусетской больнице общего профиля в Бостоне и в Лома Линда, Калифорния, с 2002 года. С 2003 года в США открылись еще три или четыре центра протонной терапии. Состояния. Детская исследовательская больница Св. Джуда находится в процессе строительства в Мемфисе, Теннесси. Некоторые центры с тех пор открылись в Европе. (Германия, Швейцария и Франция).
Этот протокол все еще проходит доклиническую оценку. Ингибиторы гистондеацетилазы представляют собой новый класс противораковых агентов, нацеленных непосредственно на ремоделирование хроматина. Эти агенты использовались при остром промиелоцитарном лейкозе, и было обнаружено, что они влияют на репрессию транскрипции, опосредованную HDAC. Понимания недостаточности INI1 недостаточно, чтобы предсказать, будут ли ингибиторы HDAC эффективны против AT / RT. Некоторые лабораторные результаты показывают, что он эффективен против определенных клеточных линий AT / RT.
Прогноз для AT / RT очень плохой, хотя существуют некоторые признаки того, что терапия на основе IRSIII может обеспечивают длительную выживаемость (от 60 до 72 месяцев). Двухлетняя выживаемость составляет менее 20%, средняя выживаемость после операции составляет 11 месяцев, и врачи часто рекомендуют паллиативную помощь, особенно детям младшего возраста из-за плохих результатов. Недавно протокол, использованный в многоцентровом исследовании, опубликованном в Журнале клинической онкологии, привел к 70% выживаемости через 2–3 года, при этом большинство рецидивов происходило в течение месяцев, что дает надежду на то, что существует точка, за которой пациенты могут считаться излеченными..
Пациенты с метастазами (диссеминированная опухоль), более крупными опухолями, опухолями, которые не удалось полностью удалить или рецидивом опухоли, и которые были моложе 36 месяцев, имели худшие результаты (т.е. меньшее время выживания).
Ретроспективный обзор 36 случаев AT / RT в St. Детская больница Джуд с 1984 по 2003 год показала, что двухлетняя бессобытийная выживаемость (EFS) для детей до трех лет составила 11%, а общая выживаемость (OS) - 17%. Для детей в возрасте 3 лет и старше EFS составил 78%, а OS - 89%. Ретроспективный регистр 42 пациентов с AT / RT в Детской больнице Кливленда показал, что среднее время выживания составляет 16,25 месяца, а коэффициент выживаемости составляет около 33%. В четверти этих случаев мутации в гене INI1 / hSNF5 не обнаружено.
Наиболее длительные выживания, о которых сообщается в литературе, следующие:
Лечение рака у выживших в течение длительного периода времени. Дети обычно вызывают серию негативных эффектов на физическое благополучие, фертильность, когнитивные способности и обучение.
Метастатическое распространение отмечается примерно в одной трети случаев AT / RT в время постановки диагноза, и опухоли могут возникать в любом месте ЦНС. Исследование ASCO 188 задокументированных случаев ПТ / ЛТ до 2004 г. показало, что 30% случаев имели метастазы на момент постановки диагноза. Метастатическое распространение в мозговые оболочки (лептоменигеальное распространение, иногда называемое сахарным налетом) часто встречается как вначале, так и при рецидивах. Средняя продолжительность жизни снижается при наличии метастазов. Первичные опухоли ЦНС обычно метастазируют только в ЦНС.
Сообщалось об одном случае метастазирования в брюшную полость через вентрикулоперитонеальный шунт при использовании AT / RT. Сообщалось о метастатическом распространении через этот механизм с другими опухолями головного мозга, включая герминомы, медуллобластомы, астроцитомы, глиобластомы, эпендимомы. и опухоли энтодермального синуса. Гулер и Сугита по отдельности сообщили о случаях метастазов в легкие без шунта.
По оценкам, 3% детских опухолей головного мозга являются AT / RT, хотя этот процент может увеличиваться с лучшей дифференциацией между PNET / опухоли медуллобластомы и AT / RT.
Как и в случае с другими опухолями ЦНС, у мужчин поражается больше, чем у женщин (соотношение 1,6: 1). Исследование ASCO показало соотношение мужчин и женщин 1,4: 1.
Атипичная тератоидная / рабдоидная опухоль была впервые описана как отдельная форма в 1987 году. До 1978 года, когда была описана рабдоидная опухоль, AT / RT, вероятно, был ошибочно диагностирован как медуллобластома. В некоторых ранних сообщениях опухоль была известна также как злокачественная рабдоидная опухоль (MRT) ЦНС . В период с 1978 по 1987 год AT / RT обычно ошибочно принимали за рабдоидную опухоль. Однако как ПТ / ЛТ, так и МРТ не ЦНС имеют худший прогноз, чем медуллобластома, и устойчивы к стандартным протоколам лечения медуллобластомы.
К 1995 году AT / RT стали рассматривать как новое определение агрессивных, биологически уникальный класс опухолей головного и спинного мозга, обычно поражающий младенцев и детей младшего возраста. В январе 2001 г. Национальный институт рака и Управление редких заболеваний США провели семинар по детским атипичным тератоидным / рабдоидным опухолям центральной нервной системы. Двадцать два участника из 14 учреждений собрались вместе, чтобы обсудить биологию, методы лечения и новые стратегии лечения этих опухолей. Консенсусный документ по биологии опухоли был опубликован в журнале Clinical Research. Признание, сделанное семинаром, что атипичные тератоидные / рабдоидные опухоли ЦНС (AT / RT) имеют делеции гена INI1, указывает на то, что рабдоидные опухоли почек и мозга являются идентичными или тесно связанными образованиями. Это наблюдение неудивительно, потому что рабдоидные опухоли в обоих местах обладают схожими гистологическими, клиническими и демографическими характеристиками.
Атипичная тератоидная рабдоидная опухоль встречается редко, и не было доказано, что ни терапия, обеспечивающая долгосрочное выживание, ни набор протоколов стали стандартными. Таким образом, большинство детей с AT / RT участвуют в клинических испытаниях, чтобы попытаться найти эффективное лекарство. Клинические испытания не являются стандартом лечения; это исследование. Некоторые клинические испытания сравнивают экспериментальное лечение со стандартным лечением, но только в том случае, если такое стандартное лечение существует.
Исследования в области трансплантации стволовых клеток продолжаются.
В 2011 году The New Yorker опубликовал статью Александра Хемона о битве дочери автора с AT / RT.
В августе 2011 года шестилетняя девочка по имени Аваланна Рут, которая сражалась с AT / RT в Институте рака Дана-Фарбер, была устроена мнимая свадьба со своим кумиром Джастином Бибером, врачи и медсестры предоставили картонный вырез в натуральную величину с изображением Бибера, гитариста, цветов и футболки с надписью «Будущая миссис Бибер». В феврале 2012 года она провела день лично со своим воображаемым мужем Джастином Бибером после кампании Facebook по встрече со своим кумиром. 26 сентября 2012 года она умерла после пяти с половиной лет борьбы с AT / RT.
Видеоигра That Dragon, Cancer основана на опыте воспитания Райана и Эми Грин. их сын Джоэл после того, как ему в 12 месяцев поставили диагноз атипичной тератоидной рабдоидной опухоли, и ему осталось жить всего около четырех месяцев. Джоэл продолжал выживать еще четыре года после того, как страдал от семи дополнительных опухолей и в конечном итоге скончался от рака 13 марта 2014 года. Райан Грин хотел представить опыт воспитания Джоэла в форме видеоигры, чтобы помочь игроку понять трудности и реалии, с которыми им пришлось иметь дело за это время. После смерти Джоэла игра была переработана, чтобы вместо этого служить данью уважения пяти коротким годам Райана и Эми с их третьим ребенком. Опыт семьи Грин также задокументирован в фильме Спасибо за игру.
| Классификация | D |
|---|---|
| Внешние ресурсы |