 | |||
| |||
| Имена | |||
|---|---|---|---|
Другие имена
| |||
| Идентификаторы | |||
| Номер CAS | |||
| 3D-модель (JSmol ) | |||
| ChemSpider | |||
| PubChem CID | |||
| UNII | |||
| Панель управления CompTox (EPA ) | |||
InChI
| |||
УЛЫБКА
| |||
| Свойства | |||
| Химическая формула | S. 4N. 4 | ||
| Молярная масса | 184,287 г моль | ||
| Внешний вид | Яркие оранжевые непрозрачные кристаллы | ||
| Температура плавления | 187 ° C ( 369 ° F; 460 K) | ||
| Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |||
| ссылки на информационное окно | |||
Тетранитрид тетрасеры представляет собой неорганическое соединение с формулой S4N4. Это твердое вещество золотисто-макового цвета является наиболее важным бинарным нитридом серы, который представляет собой соединения, содержащие только элементы серу и азот. Он является предшественником многих соединений S-N и вызвал широкий интерес благодаря своей необычной структуре и связям.
Азот и сера имеют схожие электроотрицательности. Когда свойства атомов настолько похожи, они часто образуют обширные семейства ковалентно связанных структур и соединений. Действительно, известно большое количество соединений S-N и S-NH, у которых S 4N4является их родительским.
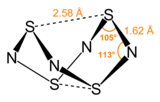
S4N4использует необычную конструкцию «экстремальной опоры» с точечной групповой симметрией D 2d. Его можно рассматривать как производное от гипотетического восьмичленного кольца чередующихся атомов серы и азота. Пары атомов серы в кольце разделены на 2,586 Å, в результате чего образуется структура в виде клетки, как определено с помощью дифракции рентгеновских лучей на монокристалле. Природа "трансаннулярных" S – S взаимодействий остается предметом исследования, поскольку она значительно короче суммы ван-дер-ваальских расстояний, но была объяснена в контексте теории молекулярных орбиталей. Связь в S 4N4считается делокализованной, на что указывает тот факт, что расстояния связи между соседними атомами серы и азота почти идентичны. Было показано, что S 4N4совместно кристаллизуется с бензолом и молекулой C60.
S4N4устойчив к воздуху. Однако он нестабилен в термодинамическом смысле с положительной энтальпией образования +460 кДж моль. Эта эндотермическая энтальпия образования возникает из-за разницы в энергии S 4N4по сравнению с его высокостабильными продуктами разложения:
Поскольку одним из продуктов разложения является газ, S 4N4можно использовать как взрывчатое вещество. Более чистые образцы имеют тенденцию быть более взрывоопасными. Небольшие образцы можно взорвать, ударив молотком. S 4N4представляет собой термохромный, меняющийся от бледно-желтого при температуре ниже -30 ° C до оранжевого при комнатной температуре и до темно-красного при температуре выше 100 ° C.
S. 4N. 4впервые был получен в 1835 году. М. Грегори путем взаимодействия дихлорида дисеры с аммиаком, процесса, который был оптимизирован:
Побочные продукты этой реакции включают имид гептасеры (S7NH) и элементарную серу. В родственном синтезе вместо этого используется монохлорид серы и NH 4 Cl:
Альтернативный синтез влечет за собой использование [(Me 3 Si) 2N]2S в качестве предшественника с предварительно сформированными связями S – N. [(Me 3 Si) 2N]2S получают реакцией бис (триметилсилил) амида лития и SCl 2.
[((CH 3)3Si) 2N]2S реагирует с комбинацией SCl 2 и SO2Cl2 с образованием S 4N4, триметилсилилхлорида и диоксида серы :
 S4N4· BF 3
S4N4· BF 3S4N4служит в качестве a основание Льюиса путем связывания через азот с сильно кислотными соединениями Льюиса, такими как SbCl 5 и SO3. Эти аддукты.
Реакция [Pt 2Cl4(PMe 2 Ph) 2 ] с S 4N4, как сообщается, с образованием комплекса, в котором сера образует дативную связь с металлом. Это соединение при стоянии изомеризуется в комплекс, в котором Атом азота образует дополнительную связь с металлическим центром.
Он протонирован HBF 4 с образованием тетрафторборатной соли:
Мягкая кислота Льюиса CuCl образует координационный полимер :
Разбавленный NaOH гидролизуется S 4N4следующим образом, с получением тиосульфата и тритионата :
Более концентрированное основание дает сульфит :
S4N4реагируют с комплексами металлов. В некоторых случаях клетка остается неповрежденной, но в других случаях она разрушена. S 4N4реагирует с комплексом Васьки ([Ir (Cl) (CO) (PPh 3)2] в реакции окислительного присоединения ) с образованием шестикоординированного иридия, где S 4N4связывается через два атома серы и один атом азота.
Многие соединения SN получают из S 4N4. Реакция с пиперидин образует [S 4N5]:
Родственный катион также известен, то есть [S 4N5]. Обработка тетраметиламмония азидом дает гетероцикл [S 3N3]:
Цикло- [S 3N3] имеет 10 пи-электроны: 2e / S плюс 1e / N плюс 1e для отрицательного заряда.
В очевидно связанной реакции использование PPN N3дает соль, содержащую синий [NS 4 ] анион:
Анион NS 4 имеет цепную структуру, описываемую с использованием резонанс [S = S = N – S – S] ↔ [S – S – N = S = S].
S4N4реагирует с бедными электронами алкинами.
Хлорирование S 4N4дает тиазилхлорид.
Пропускание газообразного S 4N4через металл серебро дает низкую температуру сверхпроводник политиазил или полисульфурнитрид (температура перехода (0,26 ± 0,03) К), часто называемый просто «(SN) x ». При превращении серебро сначала сульфидируется, и полученный Ag2S катализирует превращение S 4N4в четырехчленное кольцо S 2N2, которое легко полимеризуется.
Соединение селена Se 4N4известно и было предметом некоторых исследование. Кроме того, были выделены аддукты хлорида алюминия с Se 2N2; он образован из Se 4N4.
S4N4чувствительна к ударам. Более чистые образцы более чувствительны к удару, чем образцы, загрязненные элементарной серой.
| NH3. N2H4 | He (N 2)11 | ||||||||||||||||
| Li3N | Be3N2 | BN | β-C 3N4. gC 3N4. CxNy | N2 | NxOy | NF3 | Ne | ||||||||||
| Na3N | Mg3N2 | AlN | Si3N4 | PN. P3N5 | SxNy. SN. S4N4 | NCl 3 | Ar | ||||||||||
| Ca3N2 | ScN | TiN | VN | CrN. | FexNy | Zn3N2 | GaN | Ge3N4 | As | Se | NBr 3 | Kr | |||||
| Sr3N2 | YN | ZrN | NbN | Tc | Ru | Rh | Ag3N | InN | Sn | Sb | Te | NI3 | Xe | ||||
| TaN | WN | Re | Os | Ir | Pt | Au | Hg3N2 | Pb | Po | At | Rn | ||||||
| Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og | |||
| ↓ | |||||||||||||||||
| La | Pr | Nd | Pm | Sm | Eu | Tb | Dy | Ho | Er | Tm | Yb | Lu | |||||
| Ac | Th | Pa | UN | Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | Нет | Lr | |||