 | |||
| |||
| Имена | |||
|---|---|---|---|
| Название IUPAC Дихлорид дисеры | |||
| Систематическое название IUPAC Дихлордисульфан | |||
| Другие названия Бис [хлоридосера] (S– S). Димерный сульфенхлорид. Монохлорид серы | |||
| Идентификаторы | |||
| Номер CAS |
| ||
| 3D-модель (JSmol ) | |||
| ChemSpider | |||
| ECHA InfoCard | 100.030.021 | ||
| Номер EC |
| ||
| MeSH | Сера + монохлорид | ||
| PubChem CID | |||
| номер RTECS |
| ||
| UNII | |||
| Номер ООН | 3390 | ||
| Панель управления CompTox (EPA ) | |||
InChI
| |||
УЛЫБКИ
| |||
| Свойства | |||
| Химическая формула | S2Cl2 | ||
| Молярная масса | 135,04 г / моль | ||
| Внешний вид | От светло-желтого до желто-красного, маслянистая жидкость | ||
| Запах | резкий, тошнотворный, раздражающий | ||
| Плотность | 1,688 г / см | ||
| Точка плавления | -80 ° C (-112 ° F; 193 K) | ||
| Температура кипения | 137,1 ° C (278,8 ° F; 410,2 K) | ||
| Растворимость в воде | разлагается с потерей HCl | ||
| Растворимость | растворим в этанол, бензол, эфир, хлороформ, CCl 4 | ||
| Давление пара | 7 мм рт. Ст. (20 ° C) | ||
| Магнитная восприимчивость (χ) | -62,2 · 10 см / моль | ||
| Показатель преломления (nD) | 1,658 | ||
| Структура | |||
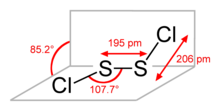
| Координационная геометрия | C2, гош | ||
| Дипольный момент | 1,60 D | ||
| Опасности | |||
| Паспорт безопасности | ICSC 0958 | ||
| Классификация ЕС (DSD) (устарело) | Токсично (T). Вредно (Xn). Коррозийный (C). Опасно для окружающей среды (N) | ||
| R-фразы (устаревшие) | R14, R20, R25, R29, R35, R50 | ||
| S-фразы (устаревшие) | (S1 / 2), S26, S36 / 37/39, S45, S61 | ||
| NFPA 704 (пожар алмаз) |  1 2 1 1 2 1 | ||
| Температура вспышки | 118,5 ° C (245,3 ° F; 391,6 K) | ||
| Самовоспламенение. температура | 234 ° C (453 ° F; 507 K) | ||
| Смертельная доза или концентрация (LD, LC): | |||
| LCLo(самый низкий опубликованный ) | 150 ppm (мышь, 1 мин) | ||
| NIOSH (пределы воздействия на здоровье США): | |||
| PEL (допустимое) | TWA 1 ppm (6 мг / м) | ||
| REL (рекомендуется) | C 1 ppm (6 мг / м) | ||
| IDLH (Непосредственная опасность) | 5 ppm | ||
| Родственные соединения | |||
| Родственные хлориды серы | Дихлорид серы. Тионилхлорид. Сульфурилхлорид | ||
| Родственные соединения | Дифторид дисеры. Дибромид дисеры | ||
| Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки в ink | |||
Дихлорид дисеры представляет собой неорганическое соединение серы и хлора с формулой S2Cl2.
Некоторые альтернативные названия этого соединения - монохлорид серы (название подразумевается его эмпирической формулой, SCl), дихлорид серы (британский английский правописание) и монохлорид серы (британский английский правописание). S 2Cl2имеет структуру, подразумеваемую формулой Cl-S-S-Cl, в которой угол между плоскостями Cl-S-S и S-S-Cl составляет 90 °. Эта структура называется гошей и похожа на структуру H2O2. Редкий изомер из S 2Cl2представляет собой S = SCl 2 ; этот изомер образуется временно, когда S 2Cl2подвергается воздействию УФ-излучения (см. тиосульфоксиды ).
Чистый дихлорид дисеры представляет собой жидкость желтого цвета, которая «дымится» во влажном воздухе из-за реакции с водой. Идеализированное (но сложное) уравнение:
Его получают частичное хлорирование элементарной серы. Реакция протекает с приемлемой скоростью при комнатной температуре. В лаборатории газообразный хлор направляют в колбу, содержащую элементарную серу. По мере образования дихлорида дисеры его содержимое становится золотисто-желтой жидкостью:
Избыточный хлор образует дихлорид серы, из-за которого жидкость становится менее желтой и более оранжево-красной:
Реакция обратима, и при стоянии SCl 2 выделяет хлор, который превращается в дихлорид дисеры. Дихлорид дисеры обладает способностью растворять большие количества серы, что частично отражает образование полисульфанов :
Дихлорид дисеры можно очистить перегонкой от избытка элементарных сера.
S2Cl2также возникает в результате хлорирования CS2, так как в синтезе тиофосгена.
S2Cl2гидролизует до диоксида серы и элементарной серы. При обработке сероводородом образуются полисульфаны, как показано в следующей идеализированной формуле:
Он реагирует с аммиаком. с образованием гептасульфуримида (S7NH) и родственных S-N-колец S 8-x (NH) x (x = 2, 3).
S2Cl2использовались для введения связей C-S. В присутствии хлорида алюминия (AlCl 3) S 2Cl2реагирует с бензолом с образованием дифенилсульфида:
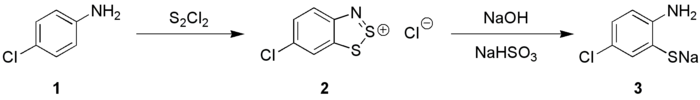
Анилины (1) реагируют с S 2Cl2в присутствии NaOH с образованием солей 1,2,3-бензодитиазолия (2) (реакция Герца ), которые могут быть преобразованы в орто-аминотиофеноляты (3), эти частицы являются предшественниками тиоиндиго красителей.
Он также используется для получения серного иприта, широко известного как «горчичный газ» в результате реакции с этиленом при 60 ° C (процесс Левинштейна):
Другие применения S 2Cl2включают производство серных красителей, инсектицидов и синтетических каучуков. Он также используется при холодной вулканизации каучуков, в качестве катализатора полимеризации растительных масел и для упрочнения древесины мягких пород.
Это вещество включено в Список 3, Часть B - Химические вещества-прекурсоры Конвенции о химическом оружии (КХО). Объекты, которые производят и / или обработка и / или потребление Списочные химические вещества могут подлежать контролю, механизмам отчетности и инспекции со стороны ОЗХО (Организации по запрещению химического оружия).
| На Викискладе есть материалы, связанные с дихлоридом дисеры. |