| ДНК-метилаза N-6 | |||||||||
|---|---|---|---|---|---|---|---|---|---|
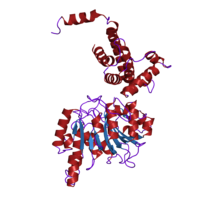 кристаллическая структура белка рестрикционного фермента типа i ecoki m (ec 2.1.1.72) (m.ecoki) кристаллическая структура белка рестрикционного фермента типа i ecoki m (ec 2.1.1.72) (m.ecoki) | |||||||||
| Идентификаторы | |||||||||
| Символ | N6_Mtase | ||||||||
| Pfam | PF02384 | ||||||||
| Pfam clan | CL0063 | ||||||||
| InterPro | IPR003356 | ||||||||
| PROSITE | PDOC00087 | ||||||||
| |||||||||
| N-концевой домен HsdM | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Идентификаторы | |||||||||
| Символ | HsdM_N | ||||||||
| Pfam | PF12161 | ||||||||
| |||||||||
| C-5 цитозин-специфическая ДНК-метилаза | |||||||||
|---|---|---|---|---|---|---|---|---|---|
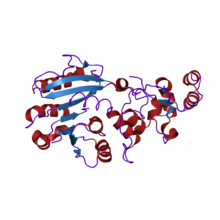 структура человеческого dnmt2, загадочного гомолога метилтрансферазы ДНК структура человеческого dnmt2, загадочного гомолога метилтрансферазы ДНК | |||||||||
| Идентификаторы | |||||||||
| Символ | ДНК_метилаза | ||||||||
| Pfam | PF00145 | ||||||||
| Pfam клан | CL0063 | ||||||||
| InterPro | IPR001525 | ||||||||
| PROSITE | PDOC00089 | ||||||||
| SCOPe | 1hmy / SUPFAM | ||||||||
| CDD | cd00315 | ||||||||
| |||||||||
| ДНК-метилаза | |||||||||
|---|---|---|---|---|---|---|---|---|---|
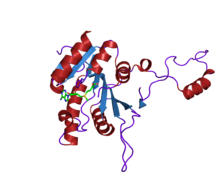 кристаллическая структура метилтрансферазы mboiia (moraxella bovis) кристаллическая структура метилтрансферазы mboiia (moraxella bovis) | |||||||||
| Идентификаторы | |||||||||
| Символ | N6_N4_Mtase | ||||||||
| Pfam | PF01555 | ||||||||
| Pfam клан | CL0063 | ||||||||
| InterPro | IPR002941 | ||||||||
| PROSITE | PDOC00088 | ||||||||
| SCOPe | 1boo / SUPFAM | ||||||||
| |||||||||
В биохимии ДНК-метилтрансфераза (ДНК-МТаза, DNMT ) семейство ферментов катализируют перенос метильной группы в ДНК. Метилирование ДНК выполняет широкий спектр биологических функций. Все известные ДНК-метилтрансферазы используют S-аденозилметионин (SAM) в качестве донора метила.
МТазы можно разделить на три разные группы на основе химических реакций, которые они катализируют:
m6A и m4C метилтрансферазы обнаруживаются в основном у прокариот (хотя недавние данные свидетельствуют о том, что m6A широко распространено у эукариот). Метилтрансферазы m5C обнаруживаются у некоторых низших эукариот, у большинства высших растений и у животных, начиная с иглокожих.
Метилтрансферазы m6A (N-6 аденин-специфическая ДНК-метилаза) (A-Mtase) представляют собой ферменты, которые специфически метилируют аминогруппу в положении C-6 аденинов в ДНК. Они обнаружены в трех существующих типах бактериальных систем рестрикции-модификации (в системе типа I А-Мтаза является продуктом гена hsdM, и в типе III это продукт гена mod). Эти ферменты отвечают за метилирование конкретных последовательностей ДНК , чтобы не дать хозяину переварить свой собственный геном через его рестрикционные ферменты. Эти метилазы имеют такую же специфичность последовательности, что и их соответствующие рестрикционные ферменты. Эти ферменты содержат консервативный мотив Asp / Asn - Pro -Pro- Tyr / Phe в их N-концевом участке, эта консервативная область может участвовать в связывании субстрата или в каталитических активность. Структура N6-MTase TaqI (M.TaqI) была преобразована в 2,4 A. Молекула укладывается на 2 домена, N-концевой каталитический домен, который содержит сайты связывания каталитического и кофактора, и включает центральный 9-нитевой бета-лист, окруженный 5 спиралями; и C-концевой домен узнавания ДНК, который образован 4 небольшими бета-листами и 8 альфа-спиралями. N- и C-концевые домены образуют щель, в которой находится ДНК субстрат. Была предложена классификация N-МТаз, основанная на расположении консервативного мотива (CM). Согласно этой классификации, N6-МТазы, которые имеют мотив DPPY (CM II), расположенный после мотива FxGxG (CM I), обозначаются как N6-аденин-МТазы класса D12. Система рестрикции и модификации типа I состоит из трех полипептидов R, M и S. Субъединицы M (hsdM) и S вместе образуют метилтрансферазу, которая метилирует два аденина остатка в комплементарных цепях двудольной ДНК узнаваемой последовательности. В присутствии субъединицы R комплекс может также действовать как эндонуклеаза, связываясь с той же целевой последовательностью, но разрезая ДНК на некотором расстоянии от этого сайта.. Будет ли ДНК разрезана или модифицирована, зависит от состояния метилирования целевой последовательности. Когда целевой сайт не изменяется, ДНК разрезается. Когда целевой сайт гемиметилирован, комплекс действует как поддерживающая метилтрансфераза, модифицируя ДНК так, что обе цепи становятся метилированными. hsdM содержит альфа-спиральный домен на N-конце, N-концевой домен HsdM.
Среди метилтрансфераз m6A (N -6 аденин-специфическая ДНК-метилаза) существует группа орфанных МТаз, которые не участвуют в бактериальной системе рестрикции / метилирования. Эти ферменты играют регулирующую роль в экспрессии генов и регуляции клеточного цикла. EcoDam из E. coli и CcrM из Caulobacter crescentus являются хорошо охарактеризованными членами этого семейства. Совсем недавно было показано, что CamA из Clostridioides difficile играет ключевую функциональную роль в споруляции, формировании биопленки и адаптации хозяина.
m4C метилтрансферазы (N-4-цитозин-специфичные метилазы ДНК) представляют собой ферменты, которые специфически метилируют аминогруппу в положении C-4 цитозинов в ДНК. Такие ферменты обнаруживаются как компоненты систем рестрикции-модификации типа II у прокариот. Такие ферменты распознают конкретную последовательность в ДНК и метилируют цитозин в этой последовательности. Этим действием они защищают ДНК от расщепления рестрикционными ферментами типа II, которые распознают ту же последовательность
метилтрансферазы m5C (C-5 цитозин-специфическая ДНК-метилаза) (C5 Mtase) являются ферментами, специфически метилировать C-5 углерод из цитозинов в ДНК с образованием C5-метилцитозина. В клетках млекопитающих цитозин-специфические метилтрансферазы метилируют определенные последовательности CpG, которые, как считается, модулируют экспрессию гена и дифференцировку клеток. В бактериях эти ферменты являются компонентом систем рестрикции-модификации и служат ценными инструментами для манипулирования ДНК. Структура метилтрансферазы HhaI (M.HhaI) была разрешена до 2,5 A : молекула складывается в 2 домена - более крупный каталитический домен, содержащий каталитические сайты и сайты связывания кофактора, и меньший домен распознавания ДНК.
Сообщалось о высококонсервативных ДНК-метилтрансферазах типов m4C, m5C и m6A, которые выглядят как многообещающие мишени для разработки новых эпигенетических ингибиторов для борьбы с бактериальной вирулентностью, устойчивостью к антибиотикам, а также для других биомедицинских применений.
De novo метилтрансферазы распознают что-то в ДНК, что позволяет им метилировать цитозины заново. Они выражаются в основном в раннем развитии эмбриона и устанавливают паттерн метилирования.
Поддерживающие метилтрансферазы добавляют метилирование ДНК, когда одна цепь уже метилирована. Они работают на протяжении всей жизни организма, поддерживая паттерн метилирования, установленный de novo метилтрансферазами.
Три активных ДНК-метилтрансферазы были идентифицированы у млекопитающих. Они называются DNMT1, DNMT3a и DNMT3b. Недавно был обнаружен четвертый фермент DNMT3c, специфически экспрессирующийся в мужской зародышевой линии мыши.
DNMT3L представляет собой белок, тесно связанный с DNMT3a и DNMT3b по структуре и критический для метилирования ДНК, но, по-видимому, сам по себе неактивен.
DNMT1 является самой распространенной ДНК-метилтрансферазой в клетках млекопитающих и считается ключевой поддерживающей метилтрансферазой у млекопитающих. Он преимущественно метилирует гемиметилированные CpG динуклеотиды в геноме млекопитающих. Несмотря на возможность использования гемиметилированного, а также неметилированного цитозина в качестве субстрата, DNMT1 не участвует в метиалиции de novo генома во время эмбрионального развития мыши. Мотив распознавания человеческого фермента включает только три основания в динуклеотидной паре CpG: C на одной цепи и CpG на другой. Это ослабленное требование субстратной специфичности позволяет ему метилировать необычные структуры, такие как промежуточные звенья проскальзывания ДНК, со скоростью de novo, которая равна скорости его поддержания. Как и другие ДНК-цитозин-5-метилтрансферазы, человеческий фермент распознает перевернутые цитозины в двухцепочечной ДНК и действует по механизму нуклеофильной атаки. В раковых клетках человека DNMT1 отвечает как за de novo, так и за поддерживающее метилирование генов-супрессоров опухолей. Длина фермента составляет около 1620 аминокислот. Первые 1100 аминокислот составляют регуляторный домен фермента, а остальные остатки составляют каталитический домен. К ним присоединяются повторы Gly - Lys. Оба домена необходимы для каталитической функции DNMT1.
DNMT1 имеет несколько изоформ, соматический DNMT1, вариант сплайсинга (DNMT1b) и ооцит -специфичную изоформу (DNMT1o). DNMT1o синтезируется и хранится в цитоплазме ооцита и перемещается в клеточное ядро на раннем эмбриональном развитии, в то время как соматический DNMT1 всегда находится в ядре соматической ткани.
нуль-мутант DNMT1 эмбриональные стволовые клетки были жизнеспособными и содержали небольшой процент метилированной ДНК и активности метилтрансферазы. Эмбрионы мышей, гомозиготные по делеции в Dnmt1, умирают на 10–11-й день беременности.
Хотя этот фермент имеет сильное сходство последовательностей с 5-метилцитозинметилтрансферазами как прокариот, так и эукариот, в 2006 г. Было показано, что фермент метилирует положение 38 в транспортной РНК аспарагиновой кислоты и не метилирует ДНК. Название этой метилтрансферазы было изменено с DNMT2 на TRDMT1 (тРНК метилтрансфераза 1 аспарагиновой кислоты), чтобы лучше отразить ее биологическую функцию. TRDMT1 - первая цитозинметилтрансфераза РНК, идентифицированная в клетках человека.
DNMT3 представляет собой семейство ДНК метилтрансфераз, которые могут метилировать гемиметилированные и неметилированные CpG с одинаковой скоростью. Архитектура ферментов DNMT3 сходна с архитектурой DNMT1, с регуляторной областью, прикрепленной к каталитическому домену. Известно четыре члена семейства DNMT3: DNMT3a, 3b, 3c и 3L.
DNMT3a и DNMT3b могут опосредовать независимую от метилирования репрессию генов. DNMT3a может совместно локализоваться с гетерохроматином белком (HP1) и метил-CpG-связывающим белком (MeCBP). Они также могут взаимодействовать с DNMT1, что может быть совместным событием во время метилирования ДНК. DNMT3a предпочитает CpG метилирование метилированию CpA, CpT и CpC, хотя, по-видимому, существует некоторое предпочтение последовательности метилирования для DNMT3a и DNMT3b. DNMT3a метилирует сайты CpG со скоростью, намного меньшей, чем DNMT1, но большей, чем DNMT3b.
DNMT3L содержит мотивы ДНК-метилтрансферазы и требуется для установления материнских геномных импринтов, несмотря на то, что он каталитически неактивен. DNMT3L экспрессируется во время гаметогенеза, когда имеет место геномный импринтинг. Утрата DNMT3L приводит к би- аллельной экспрессии генов, обычно не экспрессируемых материнским аллелем. DNMT3L взаимодействует с DNMT3a и DNMT3b и совместно локализуется в ядре. Хотя DNMT3L кажется неспособным к метилированию, он может участвовать в репрессии транскрипции.
Из-за эпигенетических эффектов семейства DNMT некоторые ингибиторы DNMT находятся в стадии исследования. для лечения некоторых видов рака: