 | |
 | |
| Клинические данные | |
|---|---|
| Торговые наименования | Сабрил, Вигадрон |
| Другие названия | γ-Vinyl-GABA |
| AHFS / Drugs.com | Монография |
| MedlinePlus | a610016 |
| Беременность. категория |
|
| Пути. введения | Устно |
| Код УВД | |
| Правовой статус | |
| Правовой статус | |
| Фармакокинетические данные | |
| Биодоступность | 80–90% |
| Связывание с белками | 0% |
| Метаболизм | не метаболизируется |
| Период полувыведения | 5–8 часов у молодых людей, 12–13 часов у пожилых людей. |
| Экскреция | Почек |
| Идентификаторы | |
Название ИЮПАК
| |
| Номер CAS | |
| PubChem CID | |
| IUPHAR / BPS | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| ChEMBL |
|
| C ompTox Dashboard (EPA ) | |
| ECHA InfoCard | 100.165.122 |
| Химические и физические данные | |
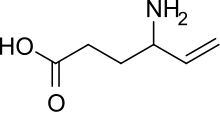
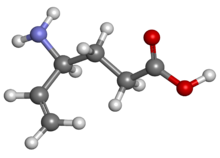
| Формула | C6H11NO2 |
| Молярная масса | 129,159 г · моль |
| 3D-модель (JSmol ) | |
| Температура плавления | от 171 до 177 ° C (от 340 до 351 ° F) |
УЛЫБКА
| |
InChI
| |
Вигабатрин, торговая марка Sabril, представляет собой лекарство, используемое для лечения эпилепсии. Он стал доступен как дженерик в 2019 году.
Он работает, подавляя распад γ-аминомасляной кислоты (ГАМК). Он также известен как γ-винил-ГАМК и является структурным аналогом ГАМК, но не связывается с рецепторами ГАМК.
В Канаде вигабатрин одобрен для использования в качестве дополнительного лечения (с другими лекарствами) при устойчивой к лечению эпилепсии, сложных парциальных припадках, вторичных генерализованных припадков и для монотерапии инфантильных спазмов при синдроме Веста.
С 2003 года вигабатрин одобрен в Мексике для лечения эпилепсии. не контролируется в достаточной степени традиционной терапией (дополнительной или монотерапия) или у недавно диагностированных пациентов, которые не пробовали другие препараты (монотерапия).
Вигабатрин также показан для использования в монотерапии при вторично генерализованных тонико-клонических приступах, парциальных припадках и при инфантильных спазмах из-за синдрома Веста.
21 августа 2009 года Лундбек объявил, что Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США выдало два разрешения на применение вигабатрина на новые лекарства. Препарат показан в качестве монотерапии для педиатрических пациентов в возрасте от одного месяца до двух лет с инфантильными спазмами, для которых потенциальные преимущества перевешивают потенциальный риск потери зрения, а также в качестве дополнительной (дополнительной) терапии для взрослых пациентов. с рефрактерными комплексными парциальными припадками (КПС), которые неадекватно ответили на несколько альтернативных методов лечения и для которых потенциальные преимущества перевешивают риск потери зрения.
В 1994 г. Фейхт и Брантнер-Инталер сообщили, что вигабатрин уменьшал судороги на 50-100% у 85% детей с синдромом Леннокса-Гасто, у которых были плохие результаты с вальпроатом натрия..
Вигабатрин уменьшал холецистокинин-тетрапептид -индуцированные симптомы панического расстройства, в дополнение к повышению кортизола и АКТГ у здоровых добровольцев.
Вигабатрин также используется для лечения судорог при недостаточности янтарной полуальдегиддегидрогеназы (SSADHD), которая является врожденным дефектом метаболизма ГАМК, вызывающим умственную отсталость, гипотония, судороги, нарушение речи и атаксия из-за накопления гамма-оксимасляной кислоты (GHB ). Вигабатрин помогает снизить уровень ГОМК за счет ингибирования трансаминазы ГАМК. Однако это только в мозгу; он не влияет на периферическую ГАМК-трансаминазу, поэтому ГОМК продолжает накапливаться и в конечном итоге достигает мозга.
Сонливость (12,5%), головная боль (3,8%), головокружение (3,8%), нервозность (2,7%), депрессия (2,5%), нарушения памяти (2,3%), диплопия (2,2%), агрессия (2,0%), атаксия (1,9%), головокружение (1,9%), гиперактивность (1,8%), потеря зрения ( 1,6%) (см. Ниже), спутанность сознания (1,4%), бессонница (1,3%), нарушение концентрации внимания (1,2%), проблемы с личностью (1,1%). Из 299 детей 33 (11%) стали гиперактивными.
У некоторых пациентов развивается психоз во время курса терапии вигабатрином, который чаще встречается у взрослых, чем у детей. Это может произойти даже с пациентами, у которых в анамнезе не было психоза. Другие редкие побочные эффекты со стороны ЦНС включают беспокойство, эмоциональную лабильность, раздражительность, тремор, аномальную походку и нарушение речи.
боли в животе (1,6 %), запор (1,4%), рвота (1,4%) и тошнота (1,4%). Диспепсия и повышение аппетита наблюдались менее чем у 1% участников клинических испытаний.
Усталость (9,2%), прибавка в весе (5,0%), астения (1.1%).
A тератологическое исследование, проведенное на кроликах, показало, что доза 150 мг / кг / день вызвала волчью пасть у 2% детенышей и в дозе 200 мг / кг / сут вызывало его у 9%. Согласно исследованию, опубликованному в марте 2001 г., это может быть связано со снижением уровня метионина. В 2005 г. было опубликовано исследование, проведенное в Университете Катании, в котором говорилось, что крысы, чьи матери потребляли 250–1000 мг / кг / день показали худшие результаты в водном лабиринте, и крысы в группе 750 мг при рождении имели недостаточный вес и не догоняли контрольную группу, а крысы в группе 1000 мг не выживали беременность.
На сегодняшний день нет данных о контролируемой тератологии у людей.
В 2003 г. Фризен и Мальмгрен показали, что вигабатрин вызывает необратимую диффузную атрофию ретинального нервного волокна слоя в ретроспективном исследовании 25 пациентов. Это имеет наибольшее влияние на внешнюю область (в отличие от желтого пятна или центральной области) сетчатки. О дефектах поля зрения сообщили еще в 1997 году Том Эке и другие в Великобритании. Некоторые авторы, включая Comaish et al. считают, что потеря поля зрения и электрофизиологические изменения могут быть продемонстрированы почти у 50% пользователей Вигабатрина.
Токсичность вигабатрина для сетчатки может быть связана с истощением таурина.
Из соображений безопасности программа вигабатрина REMS требуется FDA для принятия обоснованных решений до начала и обеспечения надлежащего использования этого препарата.
Исследование, опубликованное в 2002 году, показало, что вигабатрин вызывает статистически значимое увеличение плазменный клиренс карбамазепина.
В 1984 году доктора Риммер и Риченс из Университета Уэльса сообщили, что введение вигабатрина с фенитоином снижает концентрацию фенитоина в сыворотке у пациентов с устойчивостью к лечению. эпилепсия. Пять лет спустя те же двое ученых сообщили о падении концентрации фенитоина на 23% в течение пяти недель в статье, описывающей их неудачную попытку выяснить механизм этого взаимодействия.
Вигабатрин представляет собой необратимый ингибитор механизма аминотрансферазы гамма-аминомасляной кислоты (GABA-AT), фермента, ответственного за катаболизм ГАМК. Ингибирование ГАМК-АТ приводит к увеличению уровней ГАМК в головном мозге. Вигабатрин представляет собой рацемическое соединение, и его [S] - энантиомер является фармакологически активным.
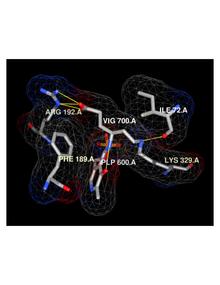 Кристаллическая структура (pdb: 1OHW), демонстрирующая связывание вигабатрина со специфическими остатками в активном сайте ГАМК-АТ, основанный на экспериментах Storici et al.
Кристаллическая структура (pdb: 1OHW), демонстрирующая связывание вигабатрина со специфическими остатками в активном сайте ГАМК-АТ, основанный на экспериментах Storici et al. Для большинства лекарств период полувыведения является полезным предиктором графика дозирования и времени, необходимого для достижения устойчивых концентраций. Однако в случае вигабатрина было обнаружено, что период полураспада биологической активности намного больше, чем период полувыведения.
Для вигабатрина не существует диапазона целевых концентраций, поскольку исследователи не обнаружили разница между уровнями концентрации в сыворотке респондеров и тех, кто не отвечает. Напротив, считается, что продолжительность действия больше зависит от скорости ресинтеза ГАМК-Т; уровни ГАМК-Т обычно не возвращаются к своему нормальному состоянию в течение шести дней после прекращения приема лекарств.
Вигабатрин был разработан в 1980-х годах с конкретной целью повышения концентрации ГАМК в организме человека. мозг, чтобы остановить эпилептический припадок. Для этого был разработан препарат, который необратимо ингибирует трансаминазу ГАМК, которая разрушает субстрат ГАМК. Хотя препарат был одобрен для лечения в Великобритании в 1989 г., санкционированное использование вигабатрина Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов США дважды откладывалось в Соединенных Штатах до 2009 г. Это было отложено в 1983 г., поскольку испытания на животных вызвали внутримиелиновый отек, однако Эффекты не были очевидны в испытаниях на людях, поэтому разработка препарата продолжалась. В 1997 году испытания были временно приостановлены, поскольку они были связаны с дефектами периферического поля зрения у людей.
Вигабатрин продается в Канаде как Sabril, Мексика и Великобритания. Торговая марка в Дании - Sabrilex. Sabril был одобрен в США 21 августа 2009 г. и продается в США компанией Lundbeck Inc., которая приобрела Ovation Pharmaceuticals, американского спонсора в марте 2009 г.
16 января 2019 г. Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) одобрило первую генерическую версию Сабрила (вигабатрина) в США.