| V-ATPase | |
|---|---|
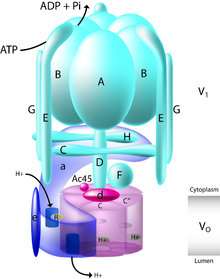 Схема V-ATPase Схема V-ATPase | |
| Идентификаторы | |
| Символ | V- АТФаза |
| TCDB | 3.A.2 |
| суперсемейство OPM | 5 |
| белок OPM | 2bl2 |
| Мембранома | 226 |
| V-АТФаза, субъединица c (Vo) | |||||||||
|---|---|---|---|---|---|---|---|---|---|
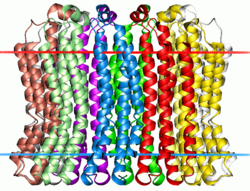 Мембранная область натриевой АТФазы V-типа из Enterococcus hirae. Расчетные углеводородные границы липидного бислоя показаны красными и синими точками Мембранная область натриевой АТФазы V-типа из Enterococcus hirae. Расчетные углеводородные границы липидного бислоя показаны красными и синими точками | |||||||||
| Идентификаторы | |||||||||
| Символ | ATP-synt_C | ||||||||
| Pfam | PF00137 | ||||||||
| InterPro | IPR002379 | ||||||||
| PROSITE | PDOC00526 | ||||||||
| SCOPe | 1aty / SUPFAM | ||||||||
| |||||||||
| V-АТФаза, субъединица C (V1) | |||||||||
|---|---|---|---|---|---|---|---|---|---|
 кристаллическая структура субъединицы C (vma5p) дрожжевой v-атпазы кристаллическая структура субъединицы C (vma5p) дрожжевой v-атпазы | |||||||||
| Идентификаторы | |||||||||
| Символ | V-ATPase_C | ||||||||
| Pfam | PF03223 | ||||||||
| InterPro | IPR004907 | ||||||||
| SCOPe | 1u7l / SUPFAM | ||||||||
| |||||||||
| V-ATPase, I / a субъединицы | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Идентификаторы | |||||||||
| Symbol | V_ATPase_I | ||||||||
| Pfam | PF01496 | ||||||||
| InterPro | IPR002490 | ||||||||
| SCOPe | 3rrk / SUPFAM | ||||||||
| TCDB | 3.A.2 | ||||||||
| |||||||||
| V-ATPase, субъединица E | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Идентификаторы | |||||||||
| Symbol | vATP-synt_E | ||||||||
| Pfam | PF01991 | ||||||||
| Pfam clan | CL0255 | ||||||||
| InterPro | IPR002842 | ||||||||
| |||||||||
| V-АТФаза, субъединица d / d2 | |||||||||
|---|---|---|---|---|---|---|---|---|---|
 кристаллическая структура субъединицы C (дрожжевая субъединица d) v-атпазы кристаллическая структура субъединицы C (дрожжевая субъединица d) v-атпазы | |||||||||
| Идентификаторы | |||||||||
| Символ | vATP-synt_AC39 | ||||||||
| Pfam | PF01992 | ||||||||
| InterPro | IPR002843 | ||||||||
| SCOPe | 1r5z / SUPFAM | ||||||||
| |||||||||
| V-АТФаза, субъединица H, N-концевой | |||||||||
|---|---|---|---|---|---|---|---|---|---|
 кристаллическая структура регуляторной субъединицы H атпазы v-типа saccharomyces cerevisiae кристаллическая структура регуляторной субъединицы H атпазы v-типа saccharomyces cerevisiae | |||||||||
| Идентификаторы | |||||||||
| Symbol | V-ATPase_H_N | ||||||||
| Pfam | PF03224 | ||||||||
| Pfam clan | CL0020 | ||||||||
| InterPro | IPR004908 | ||||||||
| SCOPe | 1ho8 / SUPFAM | ||||||||
| |||||||||
| V-ATPase, субъединица G | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Идентификаторы | |||||||||
| Symbol | V-ATPase_G | ||||||||
| Pfam | PF03179 | ||||||||
| Pfam clan | CL0255 | ||||||||
| InterPro | IPR005124 | ||||||||
| |||||||||
АТФаза вакуолярного типа (V-АТФаза ) представляет собой высококонсервативный эволюционно древний фермент с чрезвычайно разнообразным функционирует в эукариотических организмах. V-АТФазы подкисляют широкий спектр внутриклеточных органелл и перекачивают протоны через плазматические мембраны многих типов клеток. V-АТФазы связывают энергию гидролиза АТФ с транспортом протонов через внутриклеточные и плазматические мембраны эукариотических клеток. Обычно его считают полной противоположностью АТФ-синтазы, потому что АТФ-синтаза - это протонный канал, который использует энергию протонного градиента для производства АТФ. Однако V-АТФаза - это протонный насос, который использует энергию гидролиза АТФ для создания протонного градиента.
АТФаза типа архей (А-АТФаза ) - это родственная группа АТФаз, обнаруженная у архей, которые часто работают как АТФ-синтаза. Он образует кладу V / A-ATPase с V-ATPase. Большинство членов любой группы челночных протонов (H.), но некоторые члены эволюционировали, чтобы использовать вместо них ионы натрия (Na.).
V-ATPases находятся в мембранах многие органеллы, такие как эндосомы, лизосомы и секреторные везикулы, где они играют различные роли, важные для функции этих органелл. Например, протонный градиент через вакуолярную мембрану дрожжей, генерируемый V-АТФазами, стимулирует поглощение кальция в вакуоль через систему антипортеров H. / Ca.. При синаптической передаче в нейрональных клетках V-АТФаза подкисляет синаптические везикулы. Норэпинефрин проникает в везикулы с помощью V-АТФазы.
V-АТФазы также обнаруживаются в плазматических мембранах самых разных клеток, таких как интеркалированные клетки почки, остеокласты ( клетки, резорбирующие кости), макрофаги, нейтрофилы, сперматозоиды, клетки средней кишки насекомых и некоторые опухолевые клетки. V-АТФазы плазматической мембраны участвуют в таких процессах, как pH гомеостаз, сопряженный транспорт и опухолевые метастазы. V-АТФазы в акросомной мембране сперматозоидов подкисляют акросому. Это закисление активирует протеазы, необходимые для просверливания плазматической мембраны яйца. V-АТФазы в плазматической мембране остеокластов перекачивают протоны на поверхность кости, что необходимо для резорбции кости. В интеркалированных клетках почек V-АТФазы перекачивают протоны в мочу, обеспечивая реабсорбцию бикарбоната в кровь. Кроме того, другие разнообразные биологические процессы, такие как доставка токсина, проникновение вируса, нацеливание на мембрану, апоптоз, регуляция цитоплазматического pH, протеолитический процесс и подкисление внутриклеточных систем, играют важную роль V-ATPases.
V-АТФазы также играют важную роль в развитии клеточного морфогенеза. Нарушение гена vma-1, который кодирует каталитическую субъединицу (A) фермента, серьезно снижает скорость роста, дифференциации и способность производить жизнеспособные споры у гриба Neurospora crassa.
дрожжевая V-АТФаза охарактеризована лучше всего. Идентифицировано по крайней мере тринадцать субъединиц, образующих функциональный комплекс V-АТФазы, который состоит из двух доменов. Субъединицы принадлежат либо домену V o (связанные с мембраной субъединицы, строчные буквы на рисунке), либо домену V 1 (периферически связанные субъединицы, прописные буквы на рисунке).
V 1 включает восемь субъединиц, AH, с тремя копиями каталитических субъединиц A и B, тремя копиями субъединиц E и G статора и одной копией регуляторных C и Субъединицы H. Кроме того, домен V 1 также содержит субъединицы D и F, которые образуют центральную ось ротора. Домен V 1 содержит тканеспецифические изоформы субъединиц, включая B, C, E и G. Мутации изоформы B1 приводят к заболеванию человека, вызывающему дистальный почечный канальцевый ацидоз и нейросенсорную глухоту.
Домен V o содержит шесть различных субъединиц, a, d, c, c ', c "и e, при этом стехиометрия c-кольца все еще является предметом обсуждения с декамер постулируется для V-АТФазы табачного рогатого червя (Manduca sexta ). Домен V o млекопитающих содержит тканеспецифические изоформы для субъединиц a и d, тогда как V-АТФаза дрожжей содержит две изоформы субъединиц органелл a, Vph1p и Stv1p. Мутации в изоформе a3 приводят к детскому злокачественному заболеванию человека остеопетрозу, а мутации в изоформе a4 приводят к ацидозу дистальных почечных канальцев, в некоторых случаях с нейросенсорная глухота.
Домен V 1 отвечает за гидролиз АТФ, тогда как домен V o отвечает за транслокацию протонов. Гидролиз АТФ в каталитических сайтах связывания нуклеотидов на субъединице A приводит во вращение центральный стержень, состоящий из субъединиц D и F, который, в свою очередь, приводит во вращение цилиндр из субъединиц c относительно субъединицы a. Сложная структура V-АТФазы была выявлена через структуру комплексов M. Sexta и Yeast, которые были решены одночастичной крио-ЭМ и негативным окрашиванием, соответственно. Эти структуры показали, что V-АТФаза имеет сеть из 3 статоров, связанную плотным воротником, образованным субъединицами C, H и a, которые, разделяя V 1 и V o, не взаимодействуют с центральной осью ротора, образованной субъединицами F, D и d. Вращение этой центральной оси ротора, вызванное гидролизом АТФ в каталитических доменах AB, приводит к перемещению ствола субъединиц c мимо субъединицы α, которая управляет переносом протонов через мембрану. стехиометрия двух протонов, транслоцированных для каждого гидролизованного АТФ, была предложена Джонсоном.
В дополнение к структурным субъединицам дрожжевой V-АТФазы были идентифицированы связанные белки, которые необходимы для сборки. Эти ассоциированные белки необходимы для сборки домена V o и называются Vma12p, Vma21p и Vma22p. Два из трех белков, Vma12p и Vma22p, образуют комплекс, который временно связывается с Vph1p (субъединица а), чтобы способствовать его сборке и созреванию. Vma21p координирует сборку субъединиц V o, а также сопровождает домен V o в пузырьки для транспортировки в Golgi.
V 1 домен V-АТФазы является сайтом гидролиза АТФ. В отличие от V o, домен V 1 является гидрофобным. Этот растворимый домен состоит из гексамера чередующихся субъединиц A и B, центрального ротора D, периферических статоров G и E и регуляторных субъединиц C и H. Гидролиз АТФ вызывает конформационные изменения в шести интерфейсах A | B и, соответственно, их вращение. центрального ротора D. В отличие от АТФ-синтазы, домен V 1 не является активной АТФазой при диссоциации.
| Субъединица | Ген человека | Примечание |
|---|---|---|
| A, B | ATP6V1A, ATP6V1B1, ATP6V1B2 | Каталитический гексамер. |
| ATP6V1C1, ATP6V1C2 | ||
| ATP6V1D | Центральная ножка ротора, отвечающая за ионную специфичность. | |
| ATP6V1E1, ATP6V1E2, ATP6V1G1, ATP6V1G2, ATP6V1G3 | ||
| ATP6V1F | ||
| ATP6V1H |
V-ATPase (Vacuolar-ATPase) C представляет собой C-концевую субъединицу, которая является частью и локализована на границе раздела между комплексами V1 и Vo.
Субъединица C играет важную роль в контроле сборки V-АТФазы, действуя как гибкий статор, удерживающий вместе каталитическую (V1) и мембрану (VO) секторов фермента. Высвобождение субъединицы C из комплекса АТФазы приводит к диссоциации субкомплексов V1 и Vo, что является важным механизмом контроля активности V-АТФазы в клетках. По сути, создавая высокий электрохимический градиент и низкий pH, фермент вырабатывает больше АТФ.
Эти связанные субъединицы составляют основу (и) A / V-ATPase. Они важны при сборке и могут действовать как толкатели. E имеет крышку для подключения к A / B, а G - нет. Вероятно, они произошли от одного белка путем дупликации гена.
Эта субъединица участвует только в активности, а не в сборке. Эта субъединица также действует как ингибитор свободных субъединиц V1; он останавливает гидролиз АТФ, когда V1 и Vo диссоциируют.
Домен V o отвечает за перемещение протонов. В отличие от ATP-синтазы F-типа, домен V o обычно транспортирует протоны против их собственного градиента концентрации. Вращение домена V o переносит протоны в движении, координированном с доменом V 1, который отвечает за гидролиз АТФ. Домен V o является гидрофильным и состоит из нескольких диссоциируемых субъединиц. Эти субъединицы присутствуют в домене V o, чтобы сделать его функциональной протонной транслоказой; они описаны ниже.
| Субъединица | Ген человека | Примечание |
|---|---|---|
| ATP6V0A1, ATP6V0A2, ATP6V0A4 | ||
| c | ATP6V0B, ATP6V0C | Кольцо разного размера. |
| ATP6V0D1, ATP6V0D2 | ||
| ATP6V0E1, | 9 кДа гидрофобный сборочный белок. | |
| ATP6AP1 | Дополнительная субъединица | |
| S2 | ATP6AP2 | Дополнительная субъединица |
Субъединица 116 кДа (или субъединица a) и субъединица I находятся в комплексе Vo или Ao V- или A-ATPases соответственно. Субъединица 116 кДа представляет собой трансмембранный гликопротеин, необходимый для сборки и активности транспорта протонов комплекса АТФазы. Существует несколько изоформ субъединицы 116 кДа, обеспечивающих потенциальную роль в дифференциальном нацеливании и регуляции V-АТФазы для конкретных органелл.
Функция субъединицы 116 кДа не определена, но ее предсказанная структура состоит из 6-8 трансмембранозных секторов, что позволяет предположить, что она может функционировать аналогично субъединице a FO.
Субъединица d в V-ATPases, называемая субъединицей C в A-ATpases, является частью комплекса Vo. Они входят в середину c-образного кольца, поэтому считаются ротором. У эукариот существует две версии этой субъединицы: d / d1 и d2.
У млекопитающих d1 (ATP6V0D1 ) является повсеместно экспрессируемой версией, а d2 (ATP6V0D2 ) экспрессируется только в определенных типах клеток.
Подобно АТФ-синтазе F-типа, трансмембранная область V-АТФазы включает кольцо трансмембранных субъединиц, которые являются в первую очередь отвечает за перемещение протонов. Однако в отличие от АТФ-синтазы F-типа, V-АТФаза имеет несколько связанных субъединиц в с-кольце; У грибов, таких как дрожжи, есть три связанных субъединицы (различной стехиометрии), а у большинства других эукариот - две.
Дрожжевые V-АТФазы не могут собраться, когда какой-либо из генов, кодирующих субъединицы, удален, за исключением субъединиц H и c ". Без субъединицы H собранная V-АТФаза не активен, и потеря с "субъединицы приводит к разъединению ферментативной активности.
Точные механизмы, с помощью которых сборка V-АТФаз все еще противоречивы, с доказательствами, предполагающими две разные возможности. Мутационный анализ и анализы in vitro показали, что предварительно собранные домены V o и V 1 могут объединяться с образованием одного комплекса в процессе, называемом независимой сборкой. Поддержка независимой сборки включает данные о том, что собранный домен V o может быть найден в вакуоли в отсутствие домена V 1, тогда как свободный домен V 1 домены могут быть обнаружены в цитоплазме, а не в вакуоли. Напротив, эксперименты с отслеживанием импульсов in vivo выявили ранние взаимодействия между субъединицами V o и V 1, а именно субъединицами a и B, что позволяет предположить, что субъединицы добавляются в поэтапный способ формирования единого комплекса в согласованном процессе сборки.
Относительно новый метод, названный воскрешение предкового гена, пролил новый свет на эволюционная история V-АТФазы. Было показано, как структура V-АТФазы предковой формы, состоящей из двух разных белков, эволюционирует в грибную версию с тремя разными белками. АТФаза V-типа похожа на так называемую архейную (так называемую), что подтверждает архейное происхождение эукариот (например, Гипотеза эоцитов, см. Также Lokiarchaeota ). Исключительная встречаемость некоторых ветвей архей с F-типом и некоторых ветвей бактерий с АТФазой А-типа, соответственно, рассматривается как результат горизонтального переноса генов.
Известно, что V-АТФазы специфически ингибируются макролидными антибиотиками, такими как конканамицин (CCA) и балифомицин A 1. Регуляция активности V-АТФазы in vivo осуществляется путем обратимой диссоциации домена V 1 от домена V o. После начальной сборки как насекомые Manduca sexta, так и дрожжевые V-АТФазы могут обратимо распадаться на свободные домены V o и V 1 после 2–5-кратного минутное лишение глюкозы. Обратимая разборка может быть общим механизмом регуляции активности V-АТФазы, поскольку она существует у дрожжей и насекомых. Предполагается, что повторной сборке способствует комплекс, называемый RAVE (регулятор H. -АТФазы вакуолярной и эндосомальной мембран). Разборка и повторная сборка V-АТФаз не требует синтеза нового белка, но требует наличия интактной микротрубочковой сети.
Остеопетроз Общее название, которое представляет группу наследственных состояний, при которых имеется дефект резорбции остеокластической кости. У людей встречаются как доминантный, так и рецессивный остеопетроз. Аутосомно-доминантный остеопетроз проявляется легкими симптомами у взрослых, которые часто испытывают переломы костей из-за хрупкости костей. Более тяжелая форма остеопетроза называется аутосомно-рецессивным инфантильным злокачественным остеопетрозом. Идентифицированы три гена, ответственных за рецессивный остеопетроз у человека. Все они непосредственно участвуют в путях генерации и секреции протонов, которые необходимы для резорбции кости. Одним из генов является карбоангидраза II (CAII), которая при мутации вызывает остеопетроз с почечным канальцевым ацидозом (тип 3). Мутации гена ClC7 хлоридного канала также приводят как к доминантному, так и к рецессивному остеопетрозу. Примерно у 50% пациентов с рецессивным инфантильным злокачественным остеопетрозом наблюдаются мутации изоформы субъединицы a3 V-АТФазы. У людей было идентифицировано 26 мутаций в изоформе а3 субъединицы V-АТФазы, обнаруженных в остеокластах, которые приводят к аутосомно-рецессивному остеопетрозу заболевания костей.
Важность активности V-АТФазы в секреции протонов почками подчеркивается наследственным заболеванием дистального почечного канальцевого ацидоза. Во всех случаях почечный канальцевый ацидоз возникает из-за нарушения нормальных почечных механизмов, регулирующих системный pH. Существует четыре типа почечного канальцевого ацидоза. Тип 1 - дистальный почечный канальцевый ацидоз, возникающий в результате неспособности кортикального собирательного канала подкислять мочу ниже pH 5. У некоторых пациентов с аутосомно-рецессивным dRTA также нейросенсорный слух. потеря. Наследование этого типа RTA является результатом либо мутаций изоформы B1 субъединицы V-АТФазы или изоформы a4, либо мутаций полосы 3 (также называемой AE1), обменника Cl- / HCO3-. Двенадцать различных мутаций изоформы B1 V-АТФазы и двадцать четыре различных мутации в a4 приводят к dRTA. Обратная транскрипция Цепная реакция полимеразы исследования показали экспрессию субъединицы a4 в интеркалированной клетке почек и в улитке. dRTA, вызванная мутациями в гене субъединицы а4, в некоторых случаях может быть связана с глухотой из-за неспособности нормально подкислять эндолимфу внутреннего уха.
Х-связанная миопатия с чрезмерной аутофагией - редкое генетическое заболевание, возникающее в результате мутаций в гене VMA21. Заболевание возникает в детстве и приводит к медленно прогрессирующей мышечной слабости, обычно начинающейся в ногах, и некоторым пациентам в конечном итоге может потребоваться инвалидная коляска в пожилом возрасте. Белок Vma21 способствует сборке V-АТФазы, а мутации, связанные с XMEA, приводят к снижению активности V-АТФазы и увеличению лизосомальной pH.
Термин V o имеет в нижнем индексе строчную букву «о» (а не цифру «ноль»). «O» означает олигомицин, который связывается с гомологичной областью в F-АТФазы. Стоит отметить, что в нотации генов человека в NCBI он обозначается как «ноль», а не как буква «о». Например, ген c-субъединицы Vo человека указан в базе данных генов NCBI как «ATP6V0C» (с нулем), а не как «ATP6VOC» (с «о»). Многие литературные источники также допускают эту ошибку.