| Сенсорная тугоухость | |
|---|---|
 | |
| Поперечный разрез улитки. | |
| Специальность | Оториноларингология |
Нейросенсорная тугоухость (SNHL ) - это тип потерь слуха, первопричина которого ухо или сенсорный орган ( улитка и связанные с ней структурами) или вестибулокохлеарный нерв (черепной нерв VIII). На SNHL приходится около 90% зарегистрированных случаев слуха. SNHL обычно носит постоянный характер и может быть легкой, средней, тяжелой, тотальной. В зависимости от формы аудиограммы разные другие дескрипторы, например, высокочастотный, низкочастотный, U-образный, зазубренный, заостренный или плоский.
Сенсорная потеря слуха часто возникают повреждения или недостаточность улитки волосковых клеток. Волосковые клетки могут быть аномальными при рождении или повреждаться в течение жизни человека. Существуют внешние причины повреждений, включая инфекции и ототоксические препараты, так и внутренние причины, включая генетические мутации. Частая причина или усугубляющий фактор в SNHL - длительное воздействие шума на окружающую среду или потеря слуха, вызванная шумом. Воздействие одного очень громкого шума, такой как выстрел из пистолета или взрыв бомбы, может вызвать вызванную шумом потерю слуха. Использование наушников на большом уровне с течением времени или регулярное нахождение в шумной обстановке, например, на громком рабочем месте, на спортивных мероприятиях, концертах и использовании шумных машин, также может быть риском слуха из-за шума.
Невральная, или «ретрокохлеарная» потеря слуха из-за повреждений улиткового нерва (CVIII). Это может повлиять на инициирование кохлеарном нервного импульса или передачу нервного импульса в ствол мозга.
. В большинстве случаев SNHL проявляется плохим порога слышимости, происходящим от лет до десятилетий.. В некоторых случаях потери могут быть в конечном итоге повлиять на большие части диапазона частот. Это может сопровождаться другими симптомами, такими как звон в ушах (шум в ушах ) и головокружение или дурноту (вертиго ). Самый распространенный вид нейросенсорной тугоухости - возрастная (пресбиакузис ), за которую следует потеря слуха, вызванная шумом (NIHL).
Частыми симптомами SNHL являются потеря остроты зрения на различение голосов на переднем плане на фоне шума, трудности с пониманием по телефону, некоторые виды звуков, кажущиеся чрезмерно громкими или пронзительными, трудности с пониманием некоторых частей речи (фрикативные и свистящие ), потеря направленности звука (особенно с высокочастотными звуками), ощущение того, что люди бормочут при разговоре, и трудности с помощью речи. Подобные симптомы также связаны с другими видами потери слуха; аудиометрия или другие диагностические тесты необходимы для определения нейросенсорной тугоухости.
Выявление нейросенсорной тугоухости обычно осуществляется путем аудиометрии с чистым тоном (аудиограммы), при которой измеряются пороги костной проводимости. Тимпанометрия и речевая аудиометрия могут быть полезны. Обследование проводит аудиолог.
Не существует доказанного или рекомендованного лечения или лечения SNHL; лечение потери слуха обычно осуществляется с помощью слуховых аппаратов и слуховых аппаратов. В случаях глубокой или полной глухоты кохлеарный имплант представляет собой специализированный слуховой аппарат, который может восстановить функциональный уровень слуха. SNHL, по крайней мере, частично можно предотвратить, избегая шума окружающей среды, ототоксичных химикатов и лекарств, травм головы, а также путем лечения или вакцинации против определенных триггерных заболеваний и состояний, таких как менингит.
Времен внутреннее ухо не Прямой доступ к инструментам, идентификация по отчету пациента о симптомах и аудиометрическому тесту. Из тех, кто обратился к врачу с нейросенсорной тугоухостью, 90% сообщают о снижении слуха, 57% сообщают о ощущении заложенности в ухе и 49% сообщают о звоне в ухе (тиннитус ). Около половины сообщают о вестибулярных проблемах (головокружении).
Для подробного описания симптомов, полезных для скрининга, Американской академией отоларингологии был разработан опросник для самооценки, который называется «Опросник нарушений слуха для взрослых» (HHIA). Это опрос субъективных симптомов, состоящий из 25 вопросов.
Сенсорно-невральная потеря слуха может быть генетической или вызванной (т. Е. Как следствие болезни, шума, травмы и т. Д.). У людей может быть потеря слуха от рождения (врожденная ) или потеря слуха может случиться позже. Многие случаи связаны со старостью (возрастными).
Потеря слуха может передаваться по наследству. Более 40 генов вовлечены в причину глухоты. Существует 300 синдромов, связанных с потерей слуха.
Рецессивные, доминантные, Х-сцепленные или митохондриальные генетические мутации влиять на пищеварение или метаболизм внутреннего уха. Некоторые из них могут быть одноточечными мутациями, тогда как другие вызваны хромосомными аномалиями. Некоторые генетические причины приводят к поздней потереха. Митохондриальные мутации могут вызывать SNHL iem1555A>G, что делает человека чувствительным к ототоксическим эффектом аминогликозидных антибиотиков.
Прогрессирующая возрастная потеря остроты или чувствительности слуха может начаться уже в возрасте 18 лет, в первую очередь оцениивая высокие частоты, причем у мужчин чаще, чем у женщин. Такие потери стать очевидными только в более зрелом возрасте. Пресбиакузис на сегодняшний день доминирующей причиной нейросенсорной тугоухости в промышленно развитых странах. Исследование, проведенное в Судане с населением, не подвергающимся воздействию громкого шума, показало значительно меньшее количество случаев по сравнению с подобными по возрасту случаями из промышленно развитой страны. Аналогичные результаты получены в ходе исследования населения острова Пасхи, в котором сообщалось о худшем слухе у тех, кто жил в промышленных странах, по сравнению с теми, кто никогда не покидал остров. Исследователи утверждали, что помимо различных воздействий шума, факторов, таких как генетика, также могли повлиять на результаты. Потеря слуха, которая показывает причины, вызываемые факторами, отличными от нормального старения, такими как потеря слуха, вызванная шумом, не является пресбиакузией, хотя дифференцировать индивидуальные последствия нескольких причин потери слуха может быть сложно. Каждый третий человек к 65 годам сильно теряет слух; к 75 годам - каждый второй. Возрастная потеря слуха не является ни предотвращимой, ни обратимой.
Большинство людей, живущих в обществе, страдают некоторой степенью прогрессирующей нейросенсорной (т.е. постоянной) потери слуха, вызванной шумом (NIHL), в результате перегрузки и повреждений сенсорного или нервного аппарата слуха во внутреннем ухе. NIHL обычно представляет собой выпадение или вырез с частотой на частоте 4000 Гц. Как интенсивность (SPL), так и продолжительность воздействия, а также происходящее воздействие небезопасных уровней шума способствуют повреждению улитки, которое приводит к потере слуха. Чем громче шум, тем меньше безопасное время воздействия. NIHL может быть постоянным или временным, называемым пороговым сдвигом. Небезопасный уровень шума может составлять всего 70 дБ (примерно в два раза громче, чем при обычном разговоре) при продолжительном (24 часа) или непрерывном воздействии. 125 дБ (громкий рок-концерт ~ 120 дБ) - уровень боли; звуки выше этого уровня мгновенное и необратимое повреждение ушей.
Шум и старение вызывающими причинами пресбиакузиса, или возрастной потери слуха, наиболее распространенного вида потерь слуха в индустриальном обществе. Опасность воздействия шума на всю среду на рабочем месте широко признана. Многочисленные национальные и международные организации установили стандарты безопасных уровней воздействия шума в промышленности, окружающей среде, вооруженных силах, транспорте, сельском хозяйстве, горнодобывающей промышленности и других областях. Интенсивность звука или уровень звукового давления (SPL) измеряется в децибелах (дБ). Для справки:
| Уровень дБ | Пример |
|---|---|
| 45 дБ | Уровень окружающего шума вокруг дома |
| 60 дБ | Тихий офис |
| 60– 65 дБ | Обычный разговор |
| 70 дБ | Городской уличный шум на расстоянии 25 футов или средний уровень звука телевизора |
| 80 дБ | Шумный офис |
| 95– 104 дБ | танцпол в ночном клубе |
| 120 дБ | Гром поблизости или громкий рок-концерт |
| 150–160 дБ | Выстрел из ручного пистолета |
Увеличение на 6 дБ означает удвоение уровня звукового давления, или энергии звуковой волны, и, следовательно, ее склонность вызывает повреждение ушей. Требуется увеличение на 10 дБ, чтобы произвести звук, который воспринимается как вдвое громче, человеческие уши слышат логарифмически. Повреждение ушей из-за шума влияет на уровень звука, поэтому неверно полагается на субъективное восприятие громкости как на показатель риска для слуха, т.е.это может значительно недооценить опасность.
Хотя стандарты умеренно различаются по уровням напряженности и продолжительности воздействия, считающегося безопасным, можно получить некоторые рекомендации.
Безопасная величина воздействия уменьшается в 2 раза для каждого обменного курса (3 стандарта для стандарта NIOSH или 5 стандартов для стандарта OSHA ) увеличение SPL. Например, безопасное суточное воздействие при 85 дБ (90 дБ для OSHA) составляет 8 часов, а безопасное воздействие при 94 дБ (A) (уровень ночного клуба) - всего 1 час. Шумовая травма также может вызвать обратимую потерю слуха, называемую временным смещением порога. Обычно это происходит у людей, которые подвергаются нападению или взрывам и слышат звон в ушах после происшествия (тиннитус ).
Некоторые чрезмерно- безрецептурные, отпускаемые по рецепту лекарства и некоторые промышленные химикаты ототоксичны. Их воздействие может привести к временной или постоянной потере слуха.
Некоторые лекарствавызывает необратимое повреждение уха, и по этой причине их использование ограничено. Самая важная группа - это аминогликозиды (основной член гентамицин ). Редкая митохондриальная мутация, m.1555A>G, может повышать предрасположенность человека к ототоксическому эффекту аминогликозидов. Известно, что длительное злоупотребление гидрокодоном (викодином) вызывает быстро прогрессирующую нейросенсорную тугоухость, обычно без вестибулярных симптомов. Метотрексат, химиотерапевтический агент, также известен тем, что вызывает потерю слуха. В большинстве случаев потеря слуха не восстанавливается после прекращения приема препарата. Как это ни парадоксально, метотрексат также используется для лечения воспалительных заболеваний слуха, вызванной аутоиммунными заболеваниями.
Различные другие лекарства могут обратимо плохи слух. Сюда входят петлевые диуретики, силденафил (Виагра), высокие или длительные дозы НПВП (аспирин, ибупрофен, напроксен и различные рецептурные препараты: целекоксиб и т. Д.), хинин и макролидные антибиотики (эритромицин и т. д.). Цитотоксические агенты, такие как карбоплатин, используемые для лечения злокачественных новообразований, могут вызывать зависящий от доз SNHL, как и лекарства, такие как десфериоксамин, применяемые при гематологических расстройствах, таких как талассемия; Пациенты, которым прописаны эти препараты, нуждаются в наблюдении за слухом.
Продолжительное или повторяющееся воздействие ототоксичных химикатов в окружающей среде или на работе также может привести к нейросенсорной тугоухости. Некоторые из этих химикатов:
Может повреждено либо само ухо, либо к центральным слуховым путям, которые обрабатывают информацию, передаваемую ушами. Люди, получившие травму головы, подвержены временной или постоянной потере слуха тиннитусу. Контактные виды спорта, такие как футбол (НФЛ США), хоккей и крикет, часто имеют травмы головы (сотрясения мозга). В одном опросе вышедших на пенсию игроков НФЛ, все из которых сообщили об одном или нескольких сотрясениях мозга во время своей игровой карьеры, 25% имели потерю слуха и 50% - шум в ушах.
Это намного больше. часто встречается у недоношенных детей, особенно младше 1500 г. Преждевременные роды могут быть связаны соксами, которые вызывают нейросенсорной тугоухости, такими как аноксия или гипия (низкий уровень кислорода), желтуха, внутричерепные кровотечения, менингит. Фетальный алкогольный синдром вызывает потерю слуха у 64% младенцев, рожденных матерями-алкоголиками из-за ототоксического воздействия на развивающийся плод, а также недоедания. во время беременности от избыточного потребления алкоголя.
дефицит йода и эндемический гипотиреоз связаны с потерей слуха. Недостаточное потребление йода беременной матерью во время беременности влияет на развитие внутреннего уха у плода, что приводит к нейросенсорной глухоте. Это происходит в определенных регионах мира, таких как Гималаи, где йода не хватает в почве и, следовательно, в питании. В регионах этих высока заболеваемость эндемическим зобом. Эту причину глухоты можно предотвратить, добавив к соли йод.
Мозговой инсульт в области, оказывающей влияние на слуховую функцию, например инфаркт заднего кровообращения, был связан с глухотой.
Сенсорная потеря слуха вызвана аномальной структурой или функцией волосковых клеток кортиевого органа в улитке.. Нервные нарушения слуха возникают в результате повреждений восьмого черепного нерва (вестибулокохлеарный нерв ) или слуховых путей ствола мозга. Если поражены более высокие уровни слухового тракта, это называется. Центральная глухота может проявляться как сенсоневральная глухота, но ее следует отличать от анамнеза и аудиологического тестирования.
Нарушение слуха может быть связано с повреждением волосковых клеток в улитке. Иногда может наблюдаться потеря функций внутренних волосковых клеток (ВВК) в области улитки; это называется «мертвая зона». Область может быть определена в пределах диапазона характеристик частот (CF) IHC и / нейронов, непосредственно прилегающих к мертвой области.
 Рисунок 3: Поперечное сечение улитки.
Рисунок 3: Поперечное сечение улитки. Наружные волосковые клетки (OHC) вносят вклад в структуру кортиевого органа, который расположен между базилярной мембраной и текториальной мембраной внутри улитки (см. Рисунок 3). Кортиевый туннель, который проходит через кортиевый орган, разделяет OHC и внутренние клетки (IHC). OHC связаны с ретикулярной ламинарной сеткой и клетками Дейтерса. В каждом человеческом ухе примерно двенадцать тысяч OHC, и они расположены в пять рядов. Каждая OHC имеет небольшие пучки «волосков» или ресничек на своей верхней поверхности, известной как стереоцилии, и они также установлены в ряды, которые различаются по высоте. На каждом OHC имеется примерно 140 стереоцилий.
Фундаментальная роль OHC и IHC заключается в том, чтобы функционировать как сенсорные рецепторы. Основная функция ИГК - передача звуковую информацию через афферентные нейроны. Они делают это, преобразовывая механические движения или сигналы в нервную активность. При стимуляции стереоцилии на IHC перемещаются, вызывая прохождение электрического тока через волосковые клетки. Этот электрический ток создает потенциалы действия внутри связанных афферентных нейронов.
OHC отличаются тем, что они действительно участвуют в активном механизме улитки. Они делают это, получая механические сигналы или вибрации вдоль базилярной мембраны и преобразовывая их в электрохимические сигналы. Стереоцилии, обнаруженные на OHC, контактируют с текториальной мембраной. Следовательно, когда базилярная мембрана движется из-за вибраций, стереоцилии изгибаются. Направление, в котором они изгибаются, определяет скорость возбуждения слуховых нейронов, связанных с OHC.
Изгиб стереоцицилов в направлении базального тела OHC возбуждение волосковой клетки.. Таким образом, происходит возбуждение клеточного возбуждения слуховых нейронов, связанных с волосковойкой. С другой стороны, изгиб стереоцилий от базального тела OHC ингибирование волосковой клетки. Таким образом, происходит снижение стимуляции возбуждения слуховых нейронов, связанных с волосковойкой. OHC уникальны тем, что они могут сжиматься и расширяться (электромобильность). Следовательно, в ответ на электрическую стимуляцию, обеспечиваемую эфферентным нервом, они изменяются по длине, жесткости. Эти изменения действуют на реакцию базилярной мембраны на звук. Таким образом, что OHC играет важную роль в активных процессах улитки. Основная функция активного механизма - тонкая настройка базилярной мембраны и обеспечение ее высокой чувствительности к тихим звукам. Активный механизм зависит от хорошего физиологического состояния улитки. Однако улитка очень восприимчива к повреждениям.
SNHL чаще всего вызывается повреждением OHC и IHC. Есть два способа их повреждения. Во-первых, может погибнуть вся волосковая клетка. Во-вторых, стереоцилии могут искажаться или разрушаться. Повреждение улитки может происходить через путями, например, вирусной инфекцией, воздействием ототоксичных химических веществ и интенсивным шумовым воздействием. Повреждение OHC приводит к тому, что он может вообще не эффективному механизму работать. OHC высокая чувствительность к тихим звукам в определенном диапазоне частот (приблизительно 2–4 кГц). Таким образом, повреждение OHC приводит к снижению чувствительности базилярной мембраны к слабым звукам. Следовательно, требуется усиление этих звуков, чтобы базилярная мембрана могла эффективно реагировать. IHC менее подвержены повреждениям по сравнению с OHC. Однако, если они будут повреждены, это приведет к общей потере чувствительности.
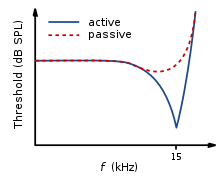 Рисунок 4: Кривая нервной настройки для нормального слуха.
Рисунок 4: Кривая нервной настройки для нормального слуха. бегущая волна вдоль базилярной мембраны движется пиков в разных местах вдоль нее, в зависимости от того, ли звук низкочастотным или высокочастотным. Из-за массы и жесткости базилярной мембраны низкочастотные волны достигают максимума в верхушке, высокочастотные звуки достигают максимума в базальном конце улитки. Следовательно, положение вдоль базилярной мембраны точно настроено на определенную частоту. Эти специально настроенные частоты называются характеристическими частотами (CF).
Если звук, входящий в ухо, смещается от характерной частоты, то сила отклика базилярной мембраны будет постепенно уменьшаться. Тонкая настройка базилярной мембраны осуществляется двумя механизмами. Первый механизм представляет собой линейный пассивный механизм, который зависит от механической структуры базилярной мембраны и окружающих ее структур. Второй механизм - это нелинейный активный механизм, который, в первую очередь, зависит от функционирования OHC, а также от общего физиологического состояния самой улитки. Основание и базилярная мембраны различаются по жесткости и вершине, что заставляет базилярную мембрану по-разному реагировать на различные частоты по своей длине. Основание базилярной мембраны узкое и жесткое, поэтому лучше всего реагирует на высокочастотные звуки. Вершина базилярной мембраны шире намного менее жесткая по сравнению с основанием, поэтому она лучше реагирует на низкие частоты.
Эту избирательность к определенным частотам можно проиллюстрировать с помощью кривых нервной настройки. Они демонстрируют частоты, на которые реагирует волокно, уровень пороговых уровней (дБ SPL) волокон слухового нерва в зависимости от различных частот. Это демонстрирует, что волокно имеет естественные окружающие его ткани. Говорят, что базилярная мембрана «резко настроена» из-за резкой V-образной кривой с ее «концом», центрированным образцом характеристической частоты слуховых волокон. Эта форма показывает, на сколько частот отвечает волокно. Если бы это была более широкая V-образная форма, она бы реагировала на большее количество частот (см. Рисунок 4).
 Рисунок 5: Кривая нейронной настройки для потерь OHC. Адаптировано из.
Рисунок 5: Кривая нейронной настройки для потерь OHC. Адаптировано из.  Рисунок 6: Кривая нейронной настройки для потерь в первом ряду OHC и потерь IHC. Адаптировано из.
Рисунок 6: Кривая нейронной настройки для потерь в первом ряду OHC и потерь IHC. Адаптировано из. Нормальная кривая настройки нервной системы характеризуется широко настроенным низкочастотным "хвостом" с точно настроенным среднечастотным "концом". Однако при частичном или полном повреждении OHC, но с неповрежденными IHC, результирующая кривая настройки покажет устранение чувствительности при тихих звуках. Т.е. где кривая нервной настройки обычно будет наиболее чувствительной (на `` кончике '') (см. рисунок 5).
Если повреждены как OHC, так и IHC, полученная кривая нейронной настройки будет показывать устранение чувствительности на «кончике». Однако из-за повреждения IHC вся кривая настройки становится приподнятой, что приводит к потере чувствительности на всех частотах (см. Рисунок 6). Необходимо только повредить первый ряд OHC, чтобы произошло устранение точно настроенного «наконечника». Это подтверждает идею о том, что частота повреждения OHC и, следовательно, потеря чувствительности к тихим звукам происходит больше, чем потеря IHC.
Когда IHC или часть базилярной мембраны повреждены или разрушены, так что они не дольше функционируют как преобразователи, в результате получается «мертвая зона». Мертвые области могут быть определены в терминах характерных частот IHC, связанных с конкретным местом вдоль базилярной мембраны, где находится мертвая область. Предполагая, что не было сдвига в характеристических частотах, относящихся к определенным областям базилярной мембраны, из-за повреждения OHC. Это часто происходит при повреждении IHC. Мертвые зоны также могут быть определены по анатомическому месту нефункционирующей ИГХ (например, «апикальная мертвая зона») или по характерным частотам ИГХ, прилегающей к мертвой зоне.
Мертвые зоны влияют на аудиометрические результаты, но, возможно, не так, как ожидалось. Например, можно ожидать, что пороговые значения не будут получены на частотах в пределах мертвой области, но будут получены на частотах, смежных с мертвой зоной. Следовательно, если предположить, что вокруг мертвой зоны существует нормальный слух, это приведет к созданию аудиограммы с резко крутым наклоном между частотой, на которой получается порог, и частотой, на которой порог не может быть получен из-за мертвого
 Рисунок 7: Ответ базилярной мембраны на чистый тон.
Рисунок 7: Ответ базилярной мембраны на чистый тон.  Рисунок 8: Ответ базилярной мембраны на чистый тон, когда есть мертвая область.
Рисунок 8: Ответ базилярной мембраны на чистый тон, когда есть мертвая область. Однако, похоже, это не так. Мертвые области нельзя однозначно разрушить с помощью аудиограммы PTA . Это может быть связано с тем, что нейроны, иннервирующие мертвую область, не могут реагировать на вибрацию на своей характерной частоте. Если вибрация базилярной мембраны способствует увеличению, нейроны, настроенные на разные характеристики частоты, например, соседние с мертвой зоной стимулируются из-за распространения распространения. Таким образом, будет получен ответ от пациента на тестовой част. Это называется «прослушиванием вне помещения» и также известно как «прослушиванием вне помещения». Это приведет к обнаружению ложного порога. Таким образом, оказывается, что у человека слух лучше, чем на самом деле, в результате чего не видно мертвой зоны. Следовательно, только используя PTA, невозможно определить степень мертвой зоны (см. Рис. 7 и 8).
Следовательно, насколько тональный сигнал с его помощью в мертвой зоне влияет на аудиометрический порог. ? Это зависит от расположения мертвой зоны. Пороги в мертвых высокой низкой частоты более неточны, чем пороги в мертвых высокой частоты. Это объясняется тем фактом, что возбуждение из-за вибрации базилярной мембраны распространяется вверх от апикальных областей базилярной мембраны в большей степени, чем возбуждение от более высокочастотных базальных областей улитки. Эта модель возбуждения похожа на явление «маскировки вверх». Чтобы вызвать такое возбуждение в нормально функционирующей области улитки, он был выше порогового значения области. Тон будет обнаружен из-за прослушивания вне частоты, что приводит к вводящему в заблуждение порогу.
Чтобы решить проблему, которая может использовать маскирование области за пределами мертвой области, что PTA помогает настроить области мертвых областей. Это означает распространение возбуждения от тона. Этот метод привел к предположению, что мертвая зона низких частот может быть связана с потерями в 40-50 дБ. Однако, для определения наличия или отсутствия мертвой зоны, можно определить, какие частоты маскировать без использования других тестов.
На основании исследований это было сделано предположение, что мертвая зона низких частот может приводить к относительно ровным потерям или к очень плавным потерям в сторону высоких частот. Мертвая зона будет менее заметна из-за распространения возбуждения вверх. В то же время могут быть очевидные крутые потери на высоких частотах для высокочастотной мертвой зоны. Хотя вполне вероятно, что наклон представляет собой менее выраженный нисходящий разброс возбуждения, а не точные пороги для тех частот с нефункционирующими волосковыми сигналами. Среднечастотные мертвые зоны с небольшим диапазоном, по-видимому, могут иметь меньшее влияние на слышать в повседневной жизни и могут создавать отметку в пороговых значениях PTA. Хотя ясно, что PTA - не лучший тест для определения мертвой зоны.
 Рисунок 9: Кривая психоакустической настройки.
Рисунок 9: Кривая психоакустической настройки. Хотя некоторые показатели надежности таких тестов продолжаются, было высказано предположение, что кривые психоакустической настройки (PTC) и результаты выравнивающего порогового шума (TEN) могут быть полезны для обнаружения мертвых, а не PTA. PTC похожи на кривые настройки нейронов. Они уровень маскирующего тона (дБ SPL) на пороге как характеристики показывают отклонения от центральной частоты (Гц). Они измеряются путем представления фиксированного чистого тона низкой плотности, а также представления узкополосного маскера с изменяющейся центральной точностью. Уровень маскера определяется, так что уровень маскера, необходимый для простой маскировки тестового сигнала, находится для маскера на каждой центральной частоте. На вершине PTC уровень маскирования, необходимый только для маскировки тестового сигнала, является самым низким. Для людей с нормальным слухом это происходит, когда центральная частота наиболее близка к частоте тестового сигнала (см. Рисунок 9).
В случае мертвых зон, когда тестовый сигнал находится в границах мертвой области, кончик PTC будет смещен в краю мертвой области, которая все еще функционирует и запускает распространение возбуждения по сигналу. В случае низкочастотной мертвой зоны вершина смещается вверх случае низкочастотную мертвую зону, начинающуюся на вершине кривой. Для высокочастотной мертвой зоны наконечник смещается вниз от частоты сигнала в рабочей зоне ниже мертвой зоны. Однако используется метод PTC непрактичен для клинического использования, и было высказано мнение, что TEN недостаточно точны. Был разработан быстрый метод поиска PTC, который может обеспечить решение. Однако необходимы дополнительные исследования для подтверждения этого метода.
Конфигурации аудиограммы не являются хорошими индикаторами того, как мертвая область повлияет на человека функционально, в основном из-за индивидуальных различий. Например, наклонная аудиограмма часто присутствует с мертвой зоной из-за распространения возбуждения. Тем не менее, человек может быть поражен иначе, чем человек с наклонной аудиограммой, вызванной частичным повреждением волосковых клеток, а не мертвой области. Они будут воспринимать звуки по-разному, но аудиограмма предполагает, что у них одинаковая степень потери. Хасс и Мур исследовали, как пациенты с нарушением слуха воспринимают чистые тона, и представляют, что они воспринимают тона как шумные и искаженные, в большей степени (в среднем), чем человек без нарушения слуха. Однако они также представлены, как шумовых не было связано с частотами в мертвых сигналах, следовательно, не было индикатором зон. Таким образом, это говорит о том, что аудиограммы и их плохое представление о мертвых областях являются неточными предикторами восприятия пациентом чистого качества звука.
Исследования Клука и Мура показали, что мертвые области также могут влиять на восприятие пациентом частот. за пределами мертвых регионов. Улучшена способность различать тона, которые очень незначительно различаются по областям сразу за мертвыми зонами по с тонами дальше. Объяснение этому может заключаться в том, что произошло повторное картирование коры. Таким образом, нейроны, которые обычно стимулируют мертвой области, были переназначены, чтобы реагировать на функционирующие области рядом с ней. Это приводит к чрезмерному представлению этих областей, что приводит к повышенной чувствительности восприятия к частотным различиям тонов.
Перед обследованием истории болезни дает представление о контексте потери слуха.
прямая осмотр наружного канала и барабанной перепонки (барабанной перепонки) с помощью отоскопа, медицинское устройство, вставляемого в слуховой проход, которое использует свет для исследования состояния наружного уха и барабанной перепонки, а также среднего уха через полупрозрачная мембрана.
Дифференциальное тестирование наиболее полезным при односторонней потере слуха и позволяет отличить кондуктивную потерю от нейросенсорной. Они несут с помощью низкочастотного камертона, обычно 512 Гц, и измерения контрастности проводимого звука через воздух и кости.
Таблица 1. Таблица 1. Таблица, сравнивающая нейросенсорная тугоухость с кондуктивной тугоухостью
| Критерии | сенсоневральной тугоухостью | Кондуктивная туго Анухость |
| Анатомическая область | Внутреннее ухо, черепной нерв VIII, или центральные центры обработки | Среднее ухо (цепь слуховых косточек), барабанная перепонка или наружное ухо |
| Тест Вебера | Звук локализуется в нормальном ухе в одностороннем SNHL | Звук локализуется в пораженное ухо (ухо с кондуктивной потерей) в односторонних случаях |
| тест Ринне | Положительный результат Ринне; воздушная проводимость>костная проводимость (и воздушная, и костная проводимость уменьшены одинаково, но разница между ними не изменилась). | Отрицательный Ринне; костная проводимость>воздушная проводимость (кость / воздушный промежуток) |
Для различных типов испытаний слуха требуются, более сложные тесты слуховой функции. Пороги костной проводимости позволяют дифференцировать нейросенсорную тугоухость от кондуктивной тугоухости. Другие тесты, такие как отоакустическая эмиссия, акустические ступенчатые рефлексы, речевая аудиометрия и аудиометрия вызванных откликов, необходимы для различения сенсорных, нервных и слуховых нарушений слуха.
A тимпанограмма - результат теста с тимпанометром. Он проверяет функцию среднего уха и подвижность барабанной перепонки. Это может помочь выявить кондуктивную потерю слуха из-за заболеваний среднего уха или барабанной перепонки от других видов слуха, включая SNHL.
аудиограмма - результат проверки слуха. Наиболее распространенный тип проверки слуха - аудиометрия чистым тоном (ЗБТ). Он отображает пороги чувствительности слуха при выборе стандартных частот от 250 до 8000 Гц. Существует также высокочастотная аудиометрия чистого тона, которая проверяет частоты от 8000 до 20 000 Гц. PTA можно использовать для различения кондуктивной тугоухости, нейросенсорной тугоухости и смешанной тугоухости. Потеря слуха может быть описана по степени, то есть легкой, средней, тяжелой или глубокой, или по форме, то есть высокочастотной или наклонной, низкой или восходящей, зазубренной, U-образной или остроконечной или плоской.
Существуют также другие виды аудиометрии, предназначенные для проверки остроты слуха, а не чувствительности (речевая аудиометрия), или для проверки передачи слуховых нервных путей (аудиометрия вызванных ответов).
МРТ-сканирование можно использовать для грубых структурных причин потери слуха. Они используются при врожденной потере слуха, когда изменение формы внутреннего уха или слухового нерва может помочь в диагностике причины потери слуха. Они полезны в случаях, когда подозревается опухоль, или для повреждения повреждения слуха, вызванного бактериальной инфекцией или аутоиммунным заболеванием. Сканирование не имеет значения при возрастной глухоте.
Пресбиакузис является ведущей причиной SNHL, прогрессирующим и неизлечимым, и в настоящее время у нас нет ни соматической, ни генной терапии, противостоять SNHL, связанному с наследственностью. Причины приобретенного SNHL в другой степени можно предотвратить, особенно причины нозокусного типа. Для этого нужно избежать шума окружающей среды и травмирующего шума, таких как рок-концерты и ночные клубы с громкой музыкой. Альтернативой является использование средств шумоподавления, таких как беруши, а также изучение уровней шума, которым он подвергается. В настоящее время существует несколько приложений для точного измерения уровня звука. Сокращение времени воздействия также может помочь снизить риск связанный с сильным воздействием.
Методы лечения делятся на три категории: фармакологические, хирургические и лечебные. SNHL представляет собой физиологическую деградацию и считается постоянной, на данный момент нет одобренных или рекомендованных методов лечения.
Были достигнуты значительные успехи в идентификации генов глухоты человека и их клеточных механизмов, а также их физиологические функции у мышей. Тем не менее возможности фармакологического лечения очень ограничены и клинически не доказаны. Применяемые фармацевтические методы лечения являются скорее паллиативными, чем лечебными, и используемое устранение первопричины.
Глубокая или полная потеря слуха поддается лечению с помощью кохлеарных имплантатов, которые напрямую стимулируют кохлеарные нервные окончания. Кохлеарный имплант - это хирургическая имплантация электронного медицинского устройства с батарейным питанием во внутреннее ухо. В отличие от слуховых аппаратов, которые издают более громкие звуки, кохлеарные имплантаты выполняют работу поврежденных частей внутреннего уха (улитки), передавая звуковые сигналы в мозг. Они состоят как из внутренних имплантированных электродов, так и из магнитов и внешних компонентов. Качество звука отличается от естественного слуха, но может получателю лучше распознавать речь и звуки окружающей среды. Из-за риска и затрат такая операция используется для случаев серьезного нарушения слуха, приводящего к инвалидности
Лечение нейросенсорной тугоухости включает использование стратегий существующего слуха, таких как чтение по губам, улучшенное общение и т. Д. И усиление с использованием слуховые аппараты. Слуховые аппараты специально адаптированы к индивидуальной потере слуха, чтобы обеспечить максимальную пользу.
Регенерация волосковых клеток с использованием стволовых клеток и генной терапии - это годы или десятилетия от клинических проявлений выполнимо. Однако в настоящее время ведутся исследования по этому вопросу, и первое исследование, одобренное FDA, начнется в феврале 2012 года.
Внезапная нейросенсорная потеря слуха (SSHL или SSNHL), широко известная как внезапная глухота, возникает как необъяснимая быстрая потеря слуха - обычно на одно ухо - сразу или в течение нескольких дней. Девять из десяти человек с SSHL теряют слух только на одно ухо. Это следует рассматривать как неотложную медицинскую помощь. Откладывание диагноза и лечение может сделать лечение эффективным или неэффективным.
По оценкам экспертов, SSHL поражает одного человека на 100 ежегодно, как правило, взрослых в возрасте от 40 до 50 лет. Фактическое количество новых случаев SSHL каждый год может быть намного выше, потому что это состояние часто не диагностируется.
Многие люди замечают, что у них SSHL, когда они просыпаются утром. Другие впервые замечают это, когда они используют глухое ухо, например, когда они разговаривают по телефону. Третьи замечают громкий, тревожный «хлопок» незадолго до того, как их слух пропадает. У людей с внезапной глухотой часто возникает головокружение, звон в ушах (тиннитус) или и то, и другое.
СШЛ диагностируется с помощью тональной аудиометрии. Если тест показывает потерю не менее 30 дБ на трех соседних частотах, потеря слуха диагностируется как SSHL. Например, потеря слуха на 30 дБ сделает разговорную речь более похожей на шепот.
Только от 10 до 15 процентов случаев диагностики как SSHL, имеют идентифицируемую причину. Большинство случаев классифицируются как идиопатические, также называемые внезапной идиопатической потерей слуха (SIHL) и идиопатической внезапной сенсоневральной тугоухостью (ISSHL или ISSNHL). Большинство данных указывает на тот или иной тип воспаления во внутреннем ухе как наиболее распространенный. частая причина ССНХЛ.
Потеря слуха полностью выздоравливает примерно у 35-39% пациентов с ВСПП, обычно в течение одной-двух недель от начала. Восемьдесят пять процентов из тех, кто проходит лечение у отоларинголога (иногда называемого ЛОР-хирургом), частично восстановят свой слух.
Общая потеря слуха затрагивает около 10% населения мира. Ожидается, что только в Соединенных Штатах 13,5 миллиона американцев страдают нейросенсорной тугоухостью. Из тех, кто страдает нейросенсорной тугоухостью, примерно 50% имеют врожденное родство. Остальные 50% связаны с инфекциями матери или плода, послеродовыми инфекциями, вирусными инфекциями, вызванными краснухой или цитомегаловирусом, ототоксичными препаратами, воздействием громких звуков, тяжелой травмой головы и преждевременные роды
Из генетически связанных случаев нейросенсорной тугоухости 75% являются аутосомно-рецессивными, 15-20% аутосомно-доминантными и 1-3% связаны с полом. Хотя конкретный ген и белок до сих пор неизвестны, считается, что мутации в гене коннексина 26 вблизи локуса DFNB1 хромосомы 13 являются причиной большей части аутосомно-рецессивной генетической сенсоневральной потери слуха
По крайней мере 8,5 на 1000 дети младше 18 лет страдают нейросенсорной тугоухостью. Общая потеря слуха пропорциональна возрасту. По крайней мере, 314 на 1000 человек старше 65 лет страдают потерей слуха. Несколько факторов риска сенсоневральной тугоухости были изучены за последнее десятилетие. Остеопороз, стапедэктомия, пневмококковые вакцины, пользователи мобильных телефонов и гипербилирубинемия при рождении - вот некоторые из известных факторов риска.
38. Газави Х., Каргошаи А.А., Джамшиди-Кухсари М. «Исследование уровней витамина D в пациенты с внезапной сенсорно-нервной потерей слуха и ее влияние на лечение », Американский журнал отоларингологии, медицины головы и шеи и хирургии, ноябрь 2019 г. https://doi.org/10.1016/j.amjoto.2019.102327
| Классификация | D |
|---|---|
| Внешний ресурсы |