| Посттравматическая эпилепсия | |
|---|---|
| Специальность | Неврология |
Посттравматическая эпилепсия (PTE ) представляет собой форму приобретенной эпилепсии, которая возникает в результате повреждения мозга, вызванного физической травмой головного мозга (черепно-мозговой травмой, сокращенно TBI). Человек с PTE страдает повторными посттравматическими припадками (PTS, припадками, возникшими в результате TBI) более чем через неделю после первоначальной травмы. По оценкам, PTE составляет 5% всех случаев эпилепсии и более 20% случаев приобретенной эпилепсии (при которых судороги вызваны идентифицируемым органическим заболеванием мозга).
Это не так. известно, как предсказать, у кого разовьется эпилепсия после ЧМТ, а у кого нет. Однако вероятность развития ПТЭ у человека зависит от тяжести и типа травмы; например, проникающие ранения и те, которые связаны с кровотечением в головном мозге, представляют более высокий риск. Начало PTE может произойти в течение короткого времени после физической травмы, которая его вызывает, либо через несколько месяцев или лет после нее. Люди с травмой головы могут оставаться в группе более высокого риска посттравматических припадков, чем население в целом, даже спустя десятилетия после травмы. ПТЭ может быть вызвано несколькими биохимическими процессами, которые происходят в головном мозге после травмы, включая перевозбуждение клеток мозга и повреждение тканей мозга свободными радикалами.
Диагностические меры включают электроэнцефалографию (ЭЭГ) и методы визуализации мозга, такие как магнитно-резонансная томография, но они не полностью надежны. Противоэпилептические препараты не предотвращают развитие ПТЭ после травмы головы, но могут использоваться для лечения этого состояния, если оно действительно возникает. Когда лекарства не помогают контролировать припадки, может потребоваться операция. Современные хирургические методы лечения ПТЭ уходят корнями в XIX век, но трепанация (вырезание отверстия в черепе), возможно, использовалась для лечения этого состояния в древних культурах.
Судороги могут возникают после черепно-мозговой травмы; они известны как посттравматические припадки (ПТС). Однако не все, у кого есть посттравматические припадки, будут продолжать страдать посттравматической эпилепсией, потому что последняя является хроническим заболеванием. Однако термины PTS и PTE в медицинской литературе используются как синонимы. Приступы, вызванные посттравматической эпилепсией, отличаются от неэпилептических посттравматических припадков в зависимости от их причины и времени после травмы. Человек с ПТЭ страдает поздними приступами, которые возникают более чем через неделю после первоначальной травмы. Поздние приступы считаются неспровоцированными, в то время как ранние приступы (возникающие в течение недели после травмы) считаются результатом прямого воздействия травмы. Спровоцированный припадок является результатом исключительной, не повторяющейся причины, такой как непосредственные последствия травмы, а не дефекта мозга; это не признак эпилепсии. Таким образом, для диагностики ПТЭ судороги должны быть неспровоцированными.
Существуют разногласия относительно того, следует ли определять ПТЭ как возникновение одного или нескольких поздних неспровоцированных приступов или следует ли диагностировать состояние только у людей с двумя или более. Медицинские источники обычно считают, что PTE присутствует, если происходит хотя бы один неспровоцированный припадок, но в последнее время стало принято ограничивать определение всех типов эпилепсии, чтобы включать только состояния, при которых происходит более одного приступа. Требование более одного припадка для диагностики ПТЭ больше соответствует современному определению эпилепсии, но исключает людей, у которых припадки контролируются лекарствами после первого припадка.
Как и в случае других форм эпилепсии, типы приступов при ПТЭ могут быть частичными (затрагивающими только часть одного полушария головного мозга) или генерализованными (затрагивающими оба полушария и связанные с ними с потерей сознания). Примерно в трети случаев у людей с ПТЭ наблюдаются парциальные припадки; они могут быть простыми или сложными. При простых парциальных припадках уровень сознания не изменяется, тогда как при сложных парциальных припадках сознание нарушается. Когда возникают генерализованные приступы, они могут начаться как парциальные, а затем распространиться и стать генерализованными.
 Кумулятивная заболеваемость после 30 лет ПТЭ у лиц с травмами головы
Кумулятивная заболеваемость после 30 лет ПТЭ у лиц с травмами головы Непонятно, почему некоторые пациенты развивают PTE, в то время как у других с очень похожими травмами нет. Однако были определены возможные факторы риска, включая тяжесть и тип травмы, наличие ранних припадков и генетические факторы.
Генетика может играть роль в риске того, что у человека разовьется ПТЭ; люди с аллелем ApoE-ε4 могут иметь более высокий риск развития PTE. Аллель гаптоглобина Hp2-2 может быть другим генетическим фактором риска, возможно потому, что он плохо связывает гемоглобин и, таким образом, позволяет большему количеству железа ускользать и повредить ткани. Однако большинство исследований показали, что наличие членов семьи, страдающих эпилепсией, существенно не увеличивает риск ПТС, что позволяет предположить, что генетика не является сильным фактором риска.
Чем серьезнее травма головного мозга, тем больше вероятность того, что у человека возникнет поздняя ПТЭ. Данные свидетельствуют о том, что легкие травмы головы не увеличивают риск развития ПТЭ, в отличие от более тяжелых. При простой легкой ЧМТ риск PTE примерно в 1,5 раза выше, чем у здорового населения. По некоторым оценкам, около половины людей с тяжелой травмой головного мозга испытывают PTE; по другим оценкам, риск составляет 5% для всех пациентов с ЧМТ и 15–20% для тяжелой ЧМТ. Одно исследование показало, что 30-летний риск развития ПТЭ составлял 2,1% для легкой ЧМТ, 4,2% для средней степени и 16,7% для тяжелых травм, как показано в таблице справа.
Характер травмы головы также влияет на риск ПТЭ. Особенно вероятны люди, которые страдают вдавленными переломами черепа, проникающими травмами головы, ранним ПТС и внутримозговыми и субдуральными гематомами из-за ЧМТ страдать PTE, который встречается более чем у 30% людей с любым из этих результатов. Около 50% пациентов с проникающей травмой головы развивают ПТЭ, а ракетные травмы и потеря объема мозга связаны с особенно высокой вероятностью развития этого состояния. Травмы, которые происходят в военных условиях, несут более высокий, чем обычно, риск развития ПТЭ, вероятно, потому, что они чаще связаны с проникающими черепно-мозговыми травмами и повреждениями головного мозга на более обширной территории. Внутричерепные гематомы, при которых кровь скапливается внутри черепа., являются одним из наиболее важных факторов риска PTE. Субдуральная гематома представляет более высокий риск развития ПТЭ, чем эпидуральная гематома, возможно, потому, что она вызывает больший ущерб ткани мозга. Повторные внутричерепные операции сопряжены с высоким риском позднего ПТЭ, возможно потому, что у людей, которым требуется дополнительное хирургическое вмешательство, с большей вероятностью будут иметь место факторы, связанные с более серьезной травмой головного мозга, такие как большие гематомы или отек мозга. Кроме того, шансы развития ПТЭ различаются в зависимости от местоположения поражения головного мозга: ушиб головного мозга, возникающий в одной или другой из лобных долей, несет 20% -ный риск ПТЭ, в то время как Ушиб одной из теменных долей имеет риск 19%, а ушиб височной доли - 16%. Когда ушибы возникают в обоих полушариях, риск составляет 26% для лобных долей, 66% для теменных и 31% для височных.
Риск того, что у человека разовьется PTE, увеличивается, но не на 100%, если PTS происходит. Поскольку многие факторы риска как для PTE, так и для ранних PTS одинаковы, неизвестно, является ли возникновение PTS фактором риска само по себе. Однако, даже независимо от других общих факторов риска, в большинстве исследований было обнаружено, что ранний посттравматический стрессовый синдром увеличивает риск PTE до более чем 25%. Человек, у которого был один поздний приступ, подвергается еще большему риску, чем тот, у кого был ранний ПТС; эпилепсия встречается у 80% людей с поздним приступом. Эпилептический статус, непрерывный приступ или множественные приступы в быстрой последовательности, особенно сильно коррелирует с развитием ПТЭ; судороги статуса происходят в 6% всех случаев ЧМТ, но связаны с ПТЭ в 42% случаев, и быстрое прекращение приступов статуса снижает шансы развития ПТЭ.
По неизвестным причинам травма может вызвать изменения в головном мозге, ведущие к эпилепсии. Существует ряд предложенных механизмов, посредством которых ЧМТ вызывает PTE, более одного из которых может присутствовать у данного человека. В период между травмой головного мозга и началом эпилепсии клетки мозга могут образовывать новые синапсы и аксоны, претерпевать апоптоз или некроз, и опыт изменил экспрессию гена . Кроме того, повреждение особо уязвимых областей коры, таких как гиппокамп, может вызвать ПТЭ.
Кровь, которая собирается в головном мозге после травмы, может повредить ткань мозга и тем самым вызвать эпилепсию. Продукты, образующиеся в результате распада гемоглобина из крови, могут быть токсичными для ткани мозга. «Гипотеза железа» утверждает, что ПТЭ возникает в результате повреждения кислородом свободными радикалами, образование которых катализируется железом из крови. Эксперименты на животных с использованием крыс показали, что эпилептические припадки могут быть вызваны инъекцией железа в мозг. Железо катализирует образование гидроксильных радикалов по реакции Габера-Вейсса ; такие свободные радикалы повреждают клетки мозга путем перекисного окисления липидов в их мембранах. Железо из крови также снижает активность фермента, называемого синтазой оксида азота, еще одного фактора, который, как считается, вносит вклад в PTE.
После ЧМТ в высвобождении появляются аномалии из нейротрансмиттеров, химических веществ, используемых клетками мозга для связи друг с другом; эти аномалии могут играть роль в развитии PTE. ЧМТ может привести к чрезмерному высвобождению глутамата и других возбуждающих нейромедиаторов (тех, которые стимулируют клетки мозга и повышают вероятность того, что они загорятся ). Это чрезмерное высвобождение глутамата может привести к эксайтотоксичности, повреждению клеток мозга из-за чрезмерной активации биохимических рецепторов, которые связываются и реагируют на возбуждающие нейротрансмиттеры. Сверхактивация рецепторов глутамата повреждает нейроны; например, это приводит к образованию свободных радикалов. Эксайтотоксичность - возможный фактор развития ПТЭ; это может привести к образованию хронического эпилептогенного очага. Эпилептический очаг - это часть мозга, из которой происходят эпилептические разряды.
Помимо химических изменений в клетках, в мозге могут происходить структурные изменения, которые приводят к эпилепсии. Судороги, возникающие вскоре после ЧМТ, могут реорганизовать нейронные сети и вызывать повторные и спонтанные припадки в дальнейшем. Гипотеза киндлинга предполагает, что в мозге формируются новые нейронные связи, которые вызывают повышение возбудимости. Слово «разжигание» является метафорой: реакция мозга на стимулы увеличивается при многократном воздействии, подобно тому, как маленькие горящие веточки могут вызвать большой пожар. Эта реорганизация нейронных сетей может сделать их более возбудимыми. Нейроны, находящиеся в состоянии гипервозбудимости из-за травмы, могут создавать эпилептический очаг в головном мозге, что приводит к судорогам. Кроме того, увеличение возбудимости нейронов может сопровождать потерю тормозных нейронов, которые обычно служат для уменьшения вероятности того, что другие нейроны сработают; эти изменения также могут вызывать PTE.
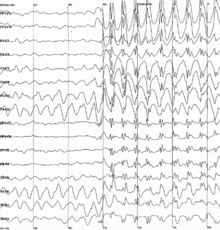 ЭЭГ показывает аномальную активность при некоторых типах судорожного расстройства, но может отображать или не отображать аномальные результаты в PTE.
ЭЭГ показывает аномальную активность при некоторых типах судорожного расстройства, но может отображать или не отображать аномальные результаты в PTE. Чтобы получить диагноз PTE, человек должен иметь в анамнезе травмы головы и не иметь припадков до травмы. Наблюдение за припадком - самый эффективный способ диагностировать ПТЭ. Электроэнцефалография (ЭЭГ) - это инструмент, используемый для диагностики судорожного расстройства, но большая часть людей с ПТЭ может не иметь аномальных «эпилептиформных» результатов ЭЭГ, указывающих на эпилепсию. В одном исследовании примерно у пятой части людей, у которых через три месяца после травмы была нормальная ЭЭГ, позже развился ПТЭ. Однако, хотя ЭЭГ бесполезна для прогнозирования того, у кого разовьется ПТЭ, она может быть полезна для локализации эпилептического очага, определения степени тяжести и прогнозирования того, будет ли у человека больше припадков, если он перестанет принимать противоэпилептические препараты.
визуализация (МРТ) выполняется у людей с ПТЭ, а КТ может использоваться для обнаружения поражений головного мозга, если МРТ недоступна. Однако часто невозможно обнаружить эпилептический очаг с помощью нейровизуализации.
. Для диагностики ПТЭ приступы не должны быть связаны с другой очевидной причиной. Судороги, возникающие после травмы головы, не обязательно связаны с эпилепсией или даже с травмой головы. Как и любой другой человек, пережившие ЧМТ могут страдать судорогами из-за факторов, включая дисбаланс жидкости или электролитов, эпилепсию по другим причинам, гипоксию (недостаток кислорода) и ишемию (недостаточный приток крови к мозгу). Отказ от алкоголя - еще одна потенциальная причина судорог. Таким образом, эти факторы должны быть исключены как причины судорог у людей с травмой головы, прежде чем можно будет поставить диагноз ПТЭ.
Профилактика PTE включает предотвращение травм головного мозга в целом; защитные меры включают велосипедные шлемы и детские сиденья. Специфического лечения для предотвращения развития эпилепсии после ЧМТ не существует. В прошлом противоэпилептические препараты использовались с целью предотвращения развития ПТЭ. Однако, хотя противоэпилептические препараты могут предотвратить ранний ПТС, клинические исследования не смогли показать, что профилактическое использование противоэпилептических препаратов предотвращает развитие ПТЭ. Почему противоэпилептические препараты в клинических испытаниях не смогли остановить развитие ПТЭ, неясно, но было предложено несколько объяснений. Лекарства могут просто не предотвращать эпилепсию, или испытания лекарств могут быть организованы таким образом, что не позволяет выявить пользу от лекарств (например, лекарства могут быть введены слишком поздно или в неадекватных дозах). Исследования на животных аналогичным образом не продемонстрировали значительного защитного эффекта наиболее часто используемых противосудорожных препаратов в исследованиях PTE, таких как фенитоин и карбамазепин. Противоэпилептические препараты рекомендуются для предотвращения поздних приступов только людям, у которых уже был диагностирован ПТЭ, а не в качестве профилактической меры. На основании вышеупомянутых исследований не существует широко распространенного лечения для предотвращения развития эпилепсии. Однако было высказано предположение, что может существовать узкое окно продолжительностью около одного часа после ЧМТ, в течение которого прием противоэпилептических средств может предотвратить эпилептогенез (развитие эпилепсии).
Были исследованы также кортикостероиды для профилактики ПТЭ, но клинические испытания показали, что препараты не уменьшают поздний ПТС и фактически были связаны с увеличением количества ранних ПТС.
 Карбамазепин, обычно используемый для лечения ПТЭ
Карбамазепин, обычно используемый для лечения ПТЭ Противоэпилептические препараты могут быть назначены для предотвращения дальнейших приступов; эти препараты полностью устраняют судороги примерно у 35% людей с ПТЭ. Однако противоэпилептические средства предотвращают приступы только во время их приема; они не уменьшают частоту возникновения после прекращения приема лекарств пациентом. Прием лекарств можно прекратить после того, как приступы купируются в течение двух лет. ПТЭ обычно трудно лечить с помощью лекарственной терапии, а противоэпилептические препараты могут быть связаны с побочными эффектами. Противоэпилептические средства карбамазепин и вальпроат являются наиболее распространенными лекарствами, применяемыми для лечения ПТЭ; фенитоин также можно использовать, но он может повысить риск когнитивных побочных эффектов, таких как нарушение мышления. Другие препараты, обычно используемые для лечения ПТЭ, включают клоназепам, фенобарбитол, примидон, габапентин и этосуксимид. Среди противоэпилептических препаратов, протестированных для предотвращения судорог после ЧМТ (фенитоин, вальпроат натрия, карбамазепин, фенобарбитал), ни одно из данных рандомизированных контролируемых исследований не показало превосходства одного над другим.
Люди, чье ПТЭ дает Если пациент не реагирует на лечение, ему может быть проведена операция по удалению эпилептогенного очага, части мозга, вызывающей припадки. Однако операция по поводу PTE может быть более трудной, чем при эпилепсии по другим причинам, и с меньшей вероятностью будет полезна при PTE, чем при других формах эпилепсии. При ПТЭ может быть особенно сложно локализовать эпилептический очаг, отчасти потому, что ЧМТ может поражать диффузные области мозга. Сложность определения очага припадка рассматривается как фактор, сдерживающий операцию. Однако для людей с склерозом мезиальной височной доли (во внутренней части височной доли), составляющих около трети людей с трудноизлечимым ПТЭ, хирургическое вмешательство, скорее всего, потребует хороший результат. Когда имеется несколько эпилептических очагов или очаг не может быть локализован, а медикаментозная терапия неэффективна, стимуляция блуждающего нерва является еще одним вариантом лечения ПТЭ.
Людям с ПТЭ назначают контрольные визиты., в которой медицинские работники контролируют неврологическую и нейропсихологическую функцию и оценивают эффективность и побочные эффекты лекарств. Как и людям, страдающим другими типами эпилепсии, пациентам с ПТЭ рекомендуется проявлять осторожность при выполнении действий, при которых судороги могут быть особенно опасными, таких как скалолазание.
Прогноз эпилепсии, обусловленный травмы хуже, чем эпилепсии неустановленной причины. Считается, что люди с ПТЭ имеют более короткую ожидаемую продолжительность жизни, чем люди с черепно-мозговой травмой, не страдающие судорогами. По сравнению с людьми с аналогичными структурными травмами головного мозга, но без PTE, людям с PTE требуется больше времени, чтобы оправиться от травмы, у них больше когнитивных и моторных проблем, и они хуже справляются с повседневными задачами. Это открытие может указывать на то, что PTE является индикатором более серьезной травмы головного мозга, а не осложнением, которое само по себе ухудшает исход. Было также установлено, что ПТЭ ассоциируется с худшими социальными и функциональными результатами, но не ухудшает реабилитацию пациентов или их способность вернуться к работе. Однако у людей с ПТЭ могут возникнуть проблемы с поиском работы, если они признают, что у них были припадки, особенно если их работа связана с работой с тяжелым оборудованием.
Период времени между травмой и развитием эпилепсии варьируется, и это не редкость. за травмой следует латентный период без повторных приступов. Чем дольше у человека не развиваются судороги, тем ниже вероятность развития эпилепсии. По крайней мере, 80–90% людей с ПТЭ имеют первый приступ в течение двух лет после ЧМТ. У людей, у которых в течение трех лет после травмы не было припадков, вероятность развития эпилепсии составляет всего 5%. Однако одно исследование показало, что выжившие после травмы головы подвергаются повышенному риску развития ПТЭ в течение 10 лет после умеренной ЧМТ и более 20 лет после тяжелой ЧМТ. Поскольку травма головы является довольно частым явлением, а эпилепсия может возникнуть на позднем этапе после травмы, может быть трудно определить, был ли случай эпилепсии результатом травмы головы в прошлом или травма была случайной.
Вопрос о том, как долго человек с PTE остается в группе более высокого риска судорог, чем остальное население. Около половины случаев PTE переходят в ремиссию, но у случаев, которые возникают позже, вероятность этого меньше.
Исследования показали, что частота ПТЭ колеблется от 1,9 до более чем 30% пациентов, страдающих ЧМТ, в зависимости от степени тяжести травмы и времени после ЧМТ, в течение которого исследования проводились с участием субъектов.
Травма головного мозга является одной из причин. являются сильнейшими предрасполагающими факторами к развитию эпилепсии и особенно важны для молодых людей. Молодые люди, которые подвергаются наибольшему риску травмы головы, также имеют самый высокий уровень ПТЭ, который является основной причиной новых случаев эпилепсии у молодых людей. Дети имеют меньший риск развития эпилепсии; У 10% детей с тяжелой ЧМТ и у 16–20% взрослых с аналогичной травмой развивается ПТЭ. Возраст старше 65 лет также является прогностическим фактором развития эпилепсии после травмы головного мозга. Одно исследование показало, что ПТЭ чаще встречается у переживших ЧМТ мужчин, чем у женщин.
 Бенджамин Уинслоу Дадли выполнил трепанацию по поводу ПТЭ до того, как стали доступны антисептики.
Бенджамин Уинслоу Дадли выполнил трепанацию по поводу ПТЭ до того, как стали доступны антисептики. Записи о ПТЭ существуют уже с 3000 До н.э. Трепанация, при которой в черепе вырезается отверстие, возможно, использовалась для лечения ПТЭ в древних культурах. В начале 19-го века хирурги и каждый из них сообщали о том, что сделали операцию по поводу PTE. Американский хирург с французским образованием Бенджамин Уинслоу Дадли (1785–1870) провел шесть трепанаций по поводу ПТЭ в период с 1819 по 1832 год в Кентукки и получил хорошие результаты, несмотря на отсутствие антисептика. Операция заключалась в вскрытии черепа на месте повреждения, санации поврежденной ткани, а иногда и в сливе крови или жидкости из-под твердой мозговой оболочки. Работа Дадли была самой крупной серией исследований такого рода, сделанных к тому моменту, и побудила других хирургов использовать трепанацию при посттравматических припадках. Его отчеты об операциях появились до того, как было признано, что операция по снижению избыточного давления в черепе была эффективной при лечении эпилепсии, но она помогла подготовить почву для того, чтобы трепанация стала обычной практикой. Эта процедура стала более распространенной в конце 19 века, когда стали доступны антисептики и церебральная локализация стала привычной концепцией. Однако в 1890 году известный немецкий врач раскритиковал эту процедуру; он поставил под сомнение ее эффективность (за исключением особых обстоятельств) и предположил, что операции были объявлены успешными слишком скоро после процедур, чтобы знать, принесут ли они долгосрочную пользу. В конце 19 века появилась внутричерепная хирургия, оперирующая повреждения головного мозга, которые, как считается, вызывали судороги, - шаг за пределы черепной хирургии, которая затрагивала только череп и мозговые оболочки. К 1893 году в США было выполнено по меньшей мере 42 внутричерепных операций по поводу PTE, с ограниченным успехом.
Хирургия была стандартным лечением PTE до тех пор, пока после Второй мировой войны это состояние не привлекло больше внимания во время войны. он развился у тех, кто пережил травму головы. Повышенная потребность в лекарствах для лечения ПТЭ привела к испытаниям противоэпилептических средств; эти ранние испытания показали, что препараты могут предотвратить эпилептогенез (развитие эпилепсии). В 1970-е годы все еще считалось, что противоэпилептические препараты могут предотвратить эпилептогенез; в 1973 г. 60% опрошенных врачей использовали их для предотвращения ПТЭ. Однако клинические испытания, которые подтвердили защитный эффект противоэпилептических средств, были неконтролируемыми; в более поздних контролируемых испытаниях препараты не показали противоэпилептогенного действия. Исследования действительно показали, что противоэпилептические средства предотвращают судороги, возникающие в течение недели после травмы, и в 1995 году целевая группа Фонда травм мозга опубликовала рекомендацию, в которой предлагалось их использовать для защиты от приступов сразу после травмы. Тем не менее, рекомендации против профилактического использования противоэпилептических препаратов были опубликованы Группой особого интереса по травмам головного мозга Американской академии физической медицины и реабилитации в 1998 году и Американской ассоциацией неврологических хирургов в отношении профилактического использования противоэпилептических препаратов более чем через неделю после травмы. в 2000 году.
Не до конца понятно, как развивается эпилепсия после травмы головного мозга, и получение такого понимания может помочь исследователям найти способы предотвратить ее или сделать ее менее серьезной или легкой. лечить. Исследователи надеются определить биомаркеры, биологические признаки того, что эпилептогенез происходит, как средство поиска лекарств, которые могут воздействовать на пути развития эпилепсии. Например, могут быть разработаны лекарственные препараты, которые препятствуют вторичному повреждению головного мозга (повреждению, которое возникает не в момент травмы, а является результатом процессов, инициированных им), путем блокирования таких путей, как свободные радикалы повреждение тканей мозга. Более глубокое понимание возрастных различий в развитии эпилепсии после травмы также может помочь исследователям найти биомаркеры эпилептогенеза. Также есть интерес к поиску большего количества противоэпилептических препаратов, которые могут влиять на эпилептогенез. Некоторые новые противоэпилептические препараты, такие как топирамат, габапентин и ламотриджин, уже разработаны и показали себя многообещающими при лечении ПТЭ. Нет животной модели, обладающей всеми характеристиками эпилептогенеза у человека, поэтому исследовательские усилия направлены на его выявление. Такая модель может помочь исследователям найти новые методы лечения и определить процессы, участвующие в эпилептогенезе. Однако наиболее распространенные механические модели черепно-мозговой травмы, такие как перкуссионное поражение жидкостью, контролируемое корковое воздействие и модели травм, вызванных падением веса, демонстрируют эпилептогенез в хронические моменты времени с задокументированными удаленными электроэнцефалографическими и поведенческими припадками и повышенной восприимчивостью к припадкам.
| Классификация | D |
|---|---|
| Внешние ресурсы |