 | |
 | |
| Клинические данные | |
|---|---|
| Торговые наименования | Дроксия, Гидрея, Сиклос и др. |
| Другие имена | Гидроксимочевина ( USAN, США) |
| AHFS / Drugs.com | Монография |
| MedlinePlus | a682004 |
| Данные лицензии | |
| Категория беременности | |
| Пути администрирования | Устно |
| Код УВД | |
| Легальное положение | |
| Легальное положение | |
| Фармакокинетические данные | |
| Метаболизм | Печень (для CO2 и мочевины) |
| Ликвидация Период полураспада | 2–4 часа |
| Экскреция | Почки и легкие |
| Идентификаторы | |
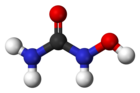
Название ИЮПАК
| |
| Количество CAS | |
| PubChem CID | |
| IUPHAR / BPS | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| КЕГГ | |
| ЧЭБИ | |
| ЧЭМБЛ | |
| NIAID ChemDB | |
| Панель управления CompTox ( EPA) | |
| ECHA InfoCard | 100.004.384 |
| Химические и физические данные | |
| Формула | C H 4 N 2 O 2 |
| Молярная масса | 76,055 г моль -1 |
| 3D модель ( JSmol ) | |
| Температура плавления | От 133 до 136 ° C (от 271 до 277 ° F) |
Улыбки
| |
ИнЧИ
| |
| (проверять) | |
Гидроксикарбамид, также известный как гидроксимочевина, представляет собой лекарство, используемое при серповидно-клеточной анемии, эссенциальной тромбоцитемии, хроническом миелолейкозе и раке шейки матки. При серповидно-клеточной анемии увеличивает гемоглобин плода и снижает количество приступов. Принимается внутрь.
Общие побочные эффекты включают подавление костного мозга, лихорадку, потерю аппетита, психиатрические проблемы, одышку и головные боли. Есть также опасения, что это увеличивает риск более поздних форм рака. Использование во время беременности обычно вредно для ребенка. Гидроксикарбамид относится к семейству противоопухолевых препаратов. Считается, что он блокирует создание ДНК.
Гидроксикарбамид был одобрен для медицинского применения в США в 1967 году. Он включен в Список основных лекарственных средств Всемирной организации здравоохранения. Гидроксикарбамид доступен как универсальный препарат.
Гидроксикарбамид применяется по следующим показаниям :
Сообщенные побочные эффекты: неврологические реакции (например, головная боль, головокружение, сонливость, дезориентация, галлюцинации и судороги ), тошнота, рвота, диарея, запор, мукозит, анорексия, стоматит, токсичность костного мозга (ограничивающая дозу токсичность; может потребоваться 7 дней). -21 дней, чтобы восстановиться после того, как был прекращен препарат), мегалобластная анемия, тромбоцитопения, кровотечение, кровоизлияние, желудочно - кишечные язвы и перфорация, иммуносупрессия, лейкопения, алопеция (выпадение волос), кожные высыпания (например, папулезная сыпь ), эритема, кожный зуд, образование пузырей или раздражение на коже и слизистых оболочек, отек легких, аномальные ферментов печени, креатинина и азота мочевины крови.
Из-за негативного воздействия на костный мозг регулярный контроль общего анализа крови жизненно важен, а также ранняя реакция на возможные инфекции. Кроме того, обычно проверяют функцию почек, мочевую кислоту и электролиты, а также ферменты печени. Более того, из-за этого его применение людям с лейкопенией, тромбоцитопенией или тяжелой анемией противопоказано.
Гидроксикарбамид использовался в первую очередь для лечения миелопролиферативных заболеваний, которым присущ риск трансформации в острый миелоидный лейкоз. Давно высказывались опасения, что гидроксикарбамид сам по себе несет в себе риск лейкемии, но крупные исследования показали, что риск либо отсутствует, либо очень мал. Тем не менее, это было препятствием для его более широкого использования у пациентов с серповидно-клеточной анемией.
Гидроксикарбамид снижает выработку дезоксирибонуклеотидов за счет ингибирования фермента рибонуклеотидредуктазы путем улавливания свободных радикалов тирозила, поскольку они участвуют в восстановлении нуклеозиддифосфатов (NDP).
При лечении серповидно-клеточной анемии гидроксикарбамид увеличивает концентрацию гемоглобина плода. Точный механизм действия еще не ясен, но похоже, что гидроксикарбамид увеличивает уровни оксида азота, вызывая активацию растворимой гуанилилциклазы с результирующим повышением циклического GMP, а также активацию экспрессии гена гамма-глобина и последующий синтез гамма-цепи, необходимый для фетального гемоглобина. (HbF) (который не полимеризует и не деформирует эритроциты, как мутировавший HbS, ответственный за серповидно-клеточную анемию). Взрослые эритроциты, содержащие более 1% HbF, называются F-клетками. Эти клетки являются потомками небольшого пула незрелых коммитированных предшественников эритроидов (BFU-e), которые сохраняют способность продуцировать HbF. Гидроксимочевина также подавляет производство гранулоцитов в костном мозге, что оказывает умеренное иммуносупрессивное действие, особенно в тех участках сосудов, где серповидные клетки перекрывают кровоток.
Сообщалось, что гидроксимочевина является эндогенной в плазме крови человека в концентрациях приблизительно от 30 до 200 нг / мл.
| Опасности | |
|---|---|
| Основные опасности | Мутаген - репродуктивная токсичность |
| Пиктограммы GHS |  |
| Сигнальное слово GHS | Опасность |
| Формулировки опасности GHS | H340, H361 |
| Меры предосторожности GHS | P201, P202, P281, P308 + 313, P405, P501 |
Гидроксимочевина была приготовлена разными способами с момента ее первоначального синтеза в 1869 году. Химики-медики, Дреслер и Штайн создали гидроксимочевину из гидроксиламина, соляной кислоты и цианида калия в качестве технического упражнения в органической химии в рамках серии экспериментов по получению производных мочевины.. Гидроксимочевина бездействовала более пятидесяти лет, пока не была изучена в рамках исследования токсичности белковых метаболитов. Благодаря своим химическим свойствам гидроксимочевина была изучена как средство от раздражения при лечении гематологических заболеваний.
Одним из распространенных механизмов синтеза гидроксимочевины является реакция цианата кальция с нитратом гидроксиламина в абсолютном этаноле и реакция цианатов солей (например, натрия или калия) и гидрохлорида гидроксиламина в водном растворе. Гидроксимочевина также была получена путем превращения анионообменной смолы четвертичного аммония из хлоридной формы в цианатную с помощью цианата натрия и взаимодействия смолы в цианатной форме с гидрохлоридом гидроксиламина. Этот метод синтеза гидроксимочевины был запатентован Hussain et al. (2015).
Гидроксимочевина представляет собой моногидроксилзамещенный антиметаболит мочевины (гидроксикарбамат). Подобно другим антиметаболитным противораковым препаратам, он действует, нарушая процесс репликации ДНК делящихся раковых клеток в организме. Гидроксимочевина избирательно ингибирует рибонуклеозиддифосфатредуктазу, фермент, необходимый для превращения рибонуклеозиддифосфатов в дезоксирибонуклеозиддифосфаты, тем самым предотвращая выход клеток из фазы G1 / S клеточного цикла. Этот агент также проявляет радиосенсибилизирующую активность, поддерживая клетки в чувствительной к излучению фазе G1 и препятствуя репарации ДНК.
Биохимические исследования показали его роль в качестве ингибитора репликации ДНК, который вызывает истощение дезоксирибонуклеотидов и приводит к двухцепочечным разрывам ДНК возле вилок репликации (см. Восстановление ДНК ). Восстановление ДНК, поврежденной химическими веществами или облучением, также ингибируется гидроксимочевиной, предлагая потенциальный синергизм между гидроксимочевиной и радиацией или алкилирующими агентами.
Гидроксимочевина имеет множество фармакологических применений в рамках системы классификации медицинских предметных рубрик :
Торговые марки включают: Hydrea, Litalir, Droxia и Siklos.