Круговой дихроизм (CD) - это дихроизм, включающий циркулярно поляризованный свет, т. Е. дифференциальное поглощение левого и правого света. Левосторонний круговой (LHC) и правосторонний круговой (RHC) поляризованный свет представляют два возможных состояния спинового углового момента для фотона, поэтому круговой дихроизм также называется дихроизмом для спинового углового момента. Это явление было обнаружено Жан-Батистом Био, Огюстэном Френелем и Эме Коттон в первой половине XIX века. Круговой дихроизм и круговое двойное лучепреломление являются проявлениями оптической активности . Он проявляется в полосах поглощения оптически активных хиральных молекул. CD спектроскопия имеет широкий спектр приложений во многих различных областях. В частности, UV CD используется для исследования вторичной структуры белков. КД в УФ / видимой области используется для исследования переходов с переносом заряда. КД в ближнем инфракрасном диапазоне используется для исследования геометрической и электронной структуры с помощью зондирование переходов металл d →d. Вибрационный круговой дихроизм, который использует свет из инфракрасной энергетической области, используется для структурных исследований малых органических молекул, а в последнее время - белков и ДНК.
Электромагнитное излучение состоит из электрического (E) и магнитного (B) поля, т. t колеблются перпендикулярно друг другу и направлению распространения, поперечная волна. В то время как линейно поляризованный свет возникает, когда вектор электрического поля колеблется только в одной плоскости, свет с круговой поляризацией возникает, когда направление вектора электрического поля вращается вокруг направления его распространения, в то время как вектор сохраняет постоянную величину. В единственной точке пространства вектор с круговой поляризацией будет очерчивать круг за один период частоты волны, отсюда и название. На двух диаграммах ниже показаны векторы электрического поля линейно и циркулярно поляризованного света в один момент времени для диапазона положений; график циркулярно поляризованного электрического вектора образует спираль вдоль направления распространения (k). Для света с левой круговой поляризацией (LCP), распространяющегося к наблюдателю, электрический вектор вращается на против часовой стрелки. Для света с правой круговой поляризацией (RCP) электрический вектор вращается по часовой стрелке.
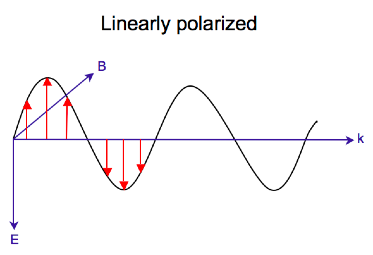
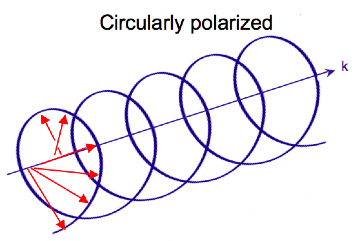
Когда свет с круговой поляризацией проходит через поглощающую оптически активную среду, скорости между правой и левой поляризациями различаются (c L ≠ c R), а также их длиной волны (λL≠ λ R) и степенью их поглощения (ε L≠εR). Круговой дихроизм - это разность Δε ≡ ε L - ε R. Электрическое поле светового луча вызывает линейное смещение заряда при взаимодействии с молекулой (электрический диполь ), тогда как его магнитное поле вызывает циркуляцию заряда (магнитный диполь ). Эти два движения вместе вызывают возбуждение электрона в спиральном движении, которое включает в себя смещение и вращение и связанные с ними операторы. Экспериментально определенная взаимосвязь между (R) образца и Δε выражается как

Вращательная сила также была определена теоретически,

Из этих двух уравнений видно, что в порядке иметь ненулевое значение 




Проще говоря, поскольку циркулярно поляризованный свет сам по себе является «хиральным», он по-другому взаимодействует с хиральными молекулами. То есть два типа света с круговой поляризацией поглощаются в разной степени. В эксперименте с компакт-диском равные количества света с левой и правой круговой поляризацией выбранной длины волны поочередно излучаются в (хиральный) образец. Одна из двух поляризаций поглощается больше, чем другая, и эта зависящая от длины волны разница поглощения измеряется, давая спектр КД образца. Из-за взаимодействия с молекулой вектор электрического поля света проходит по эллиптическому пути после прохождения через образец.
Важно, чтобы хиральность молекулы могла быть скорее конформационной, чем структурной. То есть, например, белковая молекула со спиральной вторичной структурой может иметь CD, который изменяется с изменением конформации.
По определению

где ΔA (Дельта-поглощение) - это разница между поглощением света с левой круговой поляризацией (LCP) и с правой круговой поляризацией (RCP) (это то, что обычно измеряется). ΔA является функцией длины волны, поэтому для того, чтобы измерение было значимым, должна быть известна длина волны, на которой оно проводилось.
Его также можно выразить, применив закон Бера, как:

где
Тогда

- молярный круговой дихроизм. Это внутреннее свойство обычно подразумевается под круговым дихроизмом вещества. Поскольку 

Во многих практических приложениях кругового дихроизма (КД), как обсуждается ниже, измеренный КД является не просто внутренним свойством молекулы, а скорее зависит от молекулярная конформация. В таком случае CD также может зависеть от температуры, концентрации и химической среды, включая растворители. В этом случае сообщаемое значение CD также должно указывать эти другие важные факторы, чтобы быть значимым.
В упорядоченных структурах, лишенных двоякой вращательной симметрии, оптическая активность, включая дифференциальное пропускание (и отражение) волн с круговой поляризацией, также зависит от направления распространения через материал. В этом случае так называемая внешняя трехмерная хиральность связана с взаимной ориентацией светового луча и структуры.
Хотя ΔA обычно измеряется, по историческим причинам большинство измерений указывается в градусах эллиптичности. Молярная эллиптичность - это круговой дихроизм с поправкой на концентрацию. Молярный круговой дихроизм и молярная эллиптичность [θ] легко преобразовываются друг в друга с помощью уравнения:
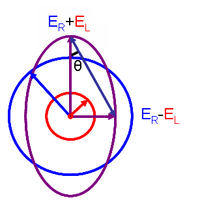 Эллиптический поляризованный свет (фиолетовый) состоит из неравных вкладов правого (синий) и левого (красный) света с круговой поляризацией.
Эллиптический поляризованный свет (фиолетовый) состоит из неравных вкладов правого (синий) и левого (красный) света с круговой поляризацией. ![[\ theta] = 3298.2 \, \ Delta \ varepsilon. \,](https://wikimedia.org/api/rest_v1/media/math/render/svg/c66e42a40570e3d3cb312c0eadd95d59170dc258)
Это отношение выводится путем определения эллиптичности поляризации как:

где
Когда E R равно E L (когда нет разницы в поглощении света с правой и левой круговыми поляризациями), θ составляет 0 °, и свет линейно поляризован. Когда E R или E L равно нулю (когда имеется полное поглощение света с круговой поляризацией в одном направлении), θ составляет 45 °, а свет с круговой поляризацией.
Обычно эффект кругового дихроизма невелик, поэтому tanθ мала и может быть аппроксимирована как θ в радианах. Поскольку интенсивность или освещенность, I, света пропорциональна квадрату вектора электрического поля, эллиптичность становится:

Затем, заменив I с помощью Закон Бера в форме натурального логарифма :

Теперь эллиптичность можно записать как:

Поскольку ΔA << 1, this expression can be approximated by expanding the exponentials in a Taylor серия до первого порядка, а затем di сравнение членов ΔA с единицей и преобразование из радиан в градусы:

Линейная зависимость концентрации растворенного вещества и длины пути устраняется путем определения молярной эллиптичности как
![[\ theta] = \ frac {100 \ th eta} {\ text {Cl}} \,](https://wikimedia.org/api/rest_v1/media/math/render/svg/17937dcb872d465ae30a0ca841fba3e953e1e9b2)
Затем, комбинируя последние два выражения с законом Бера, молярная эллиптичность становится:
![[\ theta] = 100 \, \ Delta \ varepsilon \ left (\ frac {\ ln 10} {4} \ right) \ left ( \ frac {180} {\ pi} \ right) = 3298.2 \, \ Delta \ varepsilon \,](https://wikimedia.org/api/rest_v1/media/math/render/svg/88756c2cb3877d28ff0932ef432b0a5e4861ab58)
Исторически сложились единицы измерения молярной эллиптичности (град · см / дмоль). Для расчета молярной эллиптичности необходимо знать концентрацию образца (г / л), длину пути ячейки (см) и молекулярную массу (г / моль).
Если образец представляет собой белок, средний вес остатка (средний молекулярный вес содержащихся в нем аминокислотных остатков) часто используется вместо молекулярного веса, по существу рассматривая белок как раствор аминокислот. Использование средней эллиптичности остатков облегчает сравнение CD белков с разной молекулярной массой; использование этого нормализованного CD важно при изучении структуры белка.
Методы оценки вторичной структуры в полимерах, белках и полипептидах, в частности, часто требуют, чтобы измеренный спектр молярной эллиптичности был преобразован в нормализованное значение, в частности, значение, не зависящее от длина полимера. Для этого используется средняя эллиптичность остатка; это просто измеренная молярная эллиптичность молекулы, деленная на количество мономерных единиц (остатков) в молекуле.
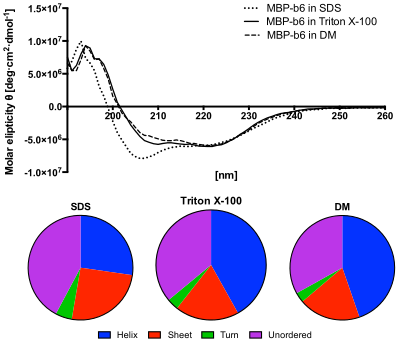 Верхняя панель: Спектроскопия кругового дихроизма в ультрафиолетовой области длин волн (УФ-КД) слитого белка МВР-цитохром b 6 в различных растворах детергентов. Это показывает, что белок в DM, как и в растворе Triton X-100, восстановил свою структуру. Однако спектры, полученные из раствора SDS, показывают снижение эллиптичности в диапазоне от 200 до 210 нм, что указывает на неполное восстановление вторичной структуры.. Нижняя панель: содержание вторичных структур, предсказанное из спектров КД с использованием алгоритма CDSSTR. Белок в растворе SDS показывает повышенное содержание неупорядоченных структур и пониженное содержание спиралей.
Верхняя панель: Спектроскопия кругового дихроизма в ультрафиолетовой области длин волн (УФ-КД) слитого белка МВР-цитохром b 6 в различных растворах детергентов. Это показывает, что белок в DM, как и в растворе Triton X-100, восстановил свою структуру. Однако спектры, полученные из раствора SDS, показывают снижение эллиптичности в диапазоне от 200 до 210 нм, что указывает на неполное восстановление вторичной структуры.. Нижняя панель: содержание вторичных структур, предсказанное из спектров КД с использованием алгоритма CDSSTR. Белок в растворе SDS показывает повышенное содержание неупорядоченных структур и пониженное содержание спиралей. Как правило, это явление будет проявляться в полосах поглощения любой оптически активной молекулы. Как следствие, круговой дихроизм проявляется биологическими молекулами из-за их правовращающего и левовращающего компонентов. Еще более важно то, что вторичная структура также будет сообщать отдельный CD своим соответствующим молекулам. Следовательно, альфа-спираль белков и двойная спираль нуклеиновых кислот имеют спектральные сигнатуры КД, характерные для их структур. Способность CD давать репрезентативную структурную сигнатуру делает его мощным инструментом в современной биохимии с приложениями, которые можно найти практически во всех областях исследования.
CD тесно связан с методом оптической вращательной дисперсии (ORD) и обычно считается более продвинутым. CD измеряется в полосах поглощения интересующей молекулы или рядом с ними, в то время как ORD можно измерять вдали от этих полос. Преимущество CD проявляется в анализе данных. Структурные элементы различимы более четко, поскольку их записанные полосы не перекрываются в значительной степени на определенных длинах волн, как это происходит в ORD. В принципе, эти два спектральных измерения могут быть взаимно преобразованы с помощью интегрального преобразования (соотношение Крамерса – Кронига ), если в измерения включены все поглощения.
Спектр КД белков в дальнем УФ (ультрафиолете ) может выявить важные характеристики их вторичной структуры. Спектры КД могут быть легко использованы для оценки доли молекулы, которая находится в конформации альфа-спираль, конформации бета-лист, бета-поворот конформация или некоторая другая (например, случайная спираль ) конформация. Эти дробные отнесения налагают важные ограничения на возможные вторичные конформации, в которых может находиться белок. CD, как правило, не может сказать, где обнаруживаются альфа-спирали, которые находятся внутри молекулы, или даже полностью предсказать, сколько их. Несмотря на это, CD - ценный инструмент, особенно для демонстрации изменений в экстерьере. Его можно, например, использовать для изучения того, как вторичная структура молекулы изменяется в зависимости от температуры или концентрации денатурирующих агентов, например Гуанидиния хлорид или мочевина. Таким образом, он может выявить важную термодинамическую информацию о молекуле (такую как энтальпия и свободная энергия Гиббса денатурации), которую иначе нельзя легко получить. Любой, кто пытается изучить белок, найдет CD ценным инструментом для проверки того, что белок находится в своей нативной конформации, прежде чем проводить с ним обширные и / или дорогостоящие эксперименты. Также существует ряд других применений КД-спектроскопии в химии белков, не связанных с оценкой фракции альфа-спирали. Более того, спектроскопия КД использовалась в исследованиях биоорганических интерфейсов. В частности, он использовался для анализа различий во вторичной структуре сконструированного белка до и после титрования реагентом.
Спектр КД в ближнем УФ-диапазоне (>250 нм) белков предоставляет информацию о третичная структура. Сигналы, полученные в области 250–300 нм, обусловлены поглощением, дипольной ориентацией и природой окружающей среды фенилаланина, тирозина, цистеина (или SS дисульфидных мостиков ) и триптофана амино кислоты. В отличие от КД в дальнем УФ, спектр КД в ближнем УФ не может быть отнесен к какой-либо конкретной трехмерной структуре. Скорее, спектры КД в ближнем УФ-диапазоне предоставляют структурную информацию о природе простетических групп в белках, например, гемовых групп в гемоглобине и цитохроме с.
КД-спектроскопия в видимом диапазоне является очень мощным методом. для изучения взаимодействий металл-белок и может разрешить отдельные электронные d-d переходы как отдельные полосы. Спектры КД в области видимого света создаются только тогда, когда ион металла находится в хиральном окружении, поэтому свободные ионы металла в растворе не обнаруживаются. Это имеет то преимущество, что позволяет наблюдать только металл, связанный с белком, поэтому легко получить зависимость от pH и стехиометрию. Оптическая активность в комплексах ионов переходных металлов приписывается конфигурационным, конформационным и вицинальным эффектам. Klewpatinond и Viles (2007) разработали набор эмпирических правил для предсказания появления видимых спектров КД для плоско-квадратных комплексов Cu и Ni с участием гистидина и координации основных цепей.
CD дает менее конкретную структурную информацию, чем, например, рентгеновская кристаллография, и белковая ЯМР спектроскопия, которые обе дают данные атомного разрешения. Однако КД-спектроскопия - это быстрый метод, который не требует большого количества белков или обширной обработки данных. Таким образом, CD можно использовать для исследования большого количества условий растворителя, изменения температуры,, pH, солености и наличия различных кофакторов.
CD спектроскопия обычно используется для изучения белков в растворе и, таким образом, дополняет методы исследования твердого состояния. Это также ограничение, поскольку многие белки встроены в мембраны в своем нативном состоянии, а растворы, содержащие мембранные структуры, часто сильно рассеивают. CD иногда измеряют в тонких пленках.
CD спектроскопия также проводилась с использованием полупроводниковых материалов, таких как TiO 2, для получения больших сигналов в УФ-диапазоне длин волн, где часто происходят электронные переходы для биомолекул..
ЦД также изучался в углеводах, но с ограниченным успехом из-за экспериментальных трудностей, связанных с измерением спектров КД в вакуумном ультрафиолете (ВУФ).) область спектра (100–200 нм), где лежат соответствующие полосы КД незамещенных углеводов. Замещенные углеводы с полосами выше VUV-области были успешно измерены.
Измерение CD также осложняется тем фактом, что типичные водные буферные системы часто поглощают в диапазоне, в котором структурные особенности демонстрируют дифференциальное поглощение света с круговой поляризацией. Фосфатный, сульфатный, карбонатный и ацетатный буферы, как правило, несовместимы с CD, если они не сделаны очень разбавленными, например в диапазоне 10–50 мМ. Следует полностью избегать использования буферной системы TRIS при выполнении CD вдали от ультрафиолета. Борат и Ониевые соединения часто используются для установления соответствующего диапазона pH для экспериментов с CD. Некоторые экспериментаторы заменили хлорид-ион фторидом, потому что фторид меньше поглощает в далеком УФ, а некоторые работали в чистой воде. Другой, почти универсальный метод состоит в том, чтобы минимизировать поглощение растворителя за счет использования ячеек с меньшей длиной пути при работе в дальнем УФ-диапазоне, длина пути 0,1 мм не является редкостью в этой работе.
Помимо измерения в водных системах, CD, особенно в дальнем УФ-диапазоне, можно измерять в органических растворителях, например этанол, метанол, трифторэтанол (TFE). Последний имеет то преимущество, что индуцирует формирование структуры белков, индуцируя бета-листы в одних и альфа-спирали в других, которые они не проявляют в нормальных водных условиях. Однако наиболее распространенные органические растворители, такие как ацетонитрил, THF, хлороформ, дихлорметан, несовместимы с CD в дальнем УФ-диапазоне.
Может быть интересно отметить, что спектры CD белка, используемые при оценке вторичной структуры, связаны с орбитальным поглощением от π до π * амидных связей, связывающих аминокислоты. Эти полосы поглощения частично лежат в так называемом вакуумном ультрафиолете (длины волн менее примерно 200 нм). Интересующий диапазон длин волн фактически недоступен в воздухе из-за сильного поглощения света кислородом на этих длинах волн. На практике эти спектры измеряются не в вакууме, а в бескислородном приборе (заполненном чистым газом азот ).
После удаления кислорода, возможно, вторым по важности техническим фактором при работе ниже 200 нм является разработка остальной части оптической системы с низкими потерями в этой области. В этом отношении критическим является использование алюминизированных зеркал , покрытия которых оптимизированы для низких потерь в этой области спектра.
Обычным источником света в этих приборах является короткодуговая ксеноновая лампа высокого давления. Обычные ксеноновые дуговые лампы не подходят для использования в условиях слабого УФ-излучения. Вместо этого необходимо использовать лампы специальной конструкции с колбами из синтетического плавленого кварца высокой чистоты.
Свет от синхротронных источников имеет гораздо больший поток на коротких волнах и использовался для записи компакт-дисков с длиной волны до 160 нм. В 2010 году спектрофотометр КД в электронном накопителе ISA в Университете Орхуса в Дании использовался для записи твердотельных спектров КД до 120 нм. На уровне квантовой механики характерная плотность кругового дихроизма и оптического вращения идентичны. Оптическая вращательная дисперсия и круговой дихроизм имеют одно и то же содержание квантовой информации.