A комплекс с переносом заряда (CT-комплекс ) или донор электронов акцепторный комплекс представляет собой ассоциацию двух или более молекул или разных частей одной большой молекулы, в которой часть электронного заряда переносится между молекулярными объектами. Возникающее в результате электростатическое притяжение обеспечивает стабилизирующую силу для молекулярного комплекса. Молекула-источник, от которой переносится заряд, называется донором электронов, а принимающая часть называется акцептором электронов.
Природа притяжения в комплексе с переносом заряда нестабильна. химическая связь, и поэтому она намного слабее, чем ковалентные силы. Многие такие комплексы могут претерпевать электронный переход в возбужденное электронное состояние. Энергия возбуждения этого перехода очень часто возникает в видимой области электромагнитного спектра, что дает характерный интенсивный цвет для этих комплексов. Эти полосы оптического поглощения часто называют полосами переноса заряда (CT-полосами). Оптическая спектроскопия - мощный метод определения характеристик полос переноса заряда.
Комплексы с переносом заряда существуют во многих типах молекул, как неорганических, так и органических, а также в твердых телах, жидкостях и растворах. Хорошо известным примером является комплекс, образованный йодом в сочетании с крахмалом, который демонстрирует интенсивную синюю полосу переноса заряда.
В неорганической химии большинство комплексов с переносом заряда включает перенос электрона между атомами металла и лигандами. Полосы переноса заряда комплексов переходных металлов возникают в результате сдвига плотности заряда между молекулярными орбиталями (МО), которые преимущественно являются металлическими по характеру, и теми, которые имеют преимущественно лигандный характер. Если перенос происходит от МО с лигандоподобным характером к металлоподобному, такой комплекс называется комплексом с переносом заряда лиганда на металл (LMCT). Если электронный заряд смещается от МО с металлоподобным характером к лигандоподобному, комплекс называется комплексом с переносом заряда металл-лиганд (MLCT). Таким образом, MLCT приводит к окислению металлического центра, тогда как LMCT приводит к восстановлению металлического центра. Резонансная рамановская спектроскопия также является мощным методом определения и характеристики полос переноса заряда в этих комплексах.
Комплексы с переносом заряда образуются при слабой ассоциации молекул или молекулярных подгрупп, один действует как донор электронов, а другой как акцептор электронов. Ассоциация не образует прочной ковалентной связи и зависит от температуры, концентрации и хозяина, например, от растворителя.
Ассоциация с переносом заряда происходит в химическом равновесии с независимыми молекулами донора (D) и акцептора (A):

С точки зрения квантовой механики это описывается как резонанс между несвязанным состоянием | D, A>и дативным состоянием | D... A>. Формирование дательного состояния представляет собой электронный переход, дающий начало красочным полосам поглощения.
Интенсивность полос переноса заряда в спектре поглощения сильно зависит от степени (константы равновесия) этой реакции ассоциации. Были разработаны методы определения константу равновесия для этих комплексов в растворе путем измерения интенсивности полос поглощения как функции концентрации донорных и акцепторных компонентов в растворе. Benesi-Hil Метод debrand, названный в честь его разработчиков, был впервые описан для ассоциации йода, растворенного в ароматических углеводородах.
Длина волны поглощения полос переноса заряда, т.е. энергия перехода с переносом заряда, характерна для конкретного типа донорных и акцепторных объектов.
Энергодонорная способность донорной молекулы измеряется ее потенциалом ионизации, который представляет собой энергию, необходимую для удаления электрона с самой высокой занятой молекулярной орбитали. Способность акцептора электронов принимать электроны определяется его сродством к электрону, которое представляет собой энергию, высвобождаемую при заполнении самой нижней незанятой молекулярной орбитали.
Общий энергетический баланс (ΔE) - это энергия, полученная при спонтанной передаче заряда. Он определяется разницей между сродством к электрону акцептора (E A) и потенциалом ионизации донора (E I), регулируемым возникающим электростатическим притяжением (J) между донором и акцептором. :

Расположение характеристических полос CT в электромагнитном спектре напрямую связана с этой разностью энергий и балансом резонансных вкладов несвязанных и дативных состояний в резонансное равновесие.
Комплексы с переносом заряда идентифицируются по
Перенос заряда часто происходит в химии неорганических лигандов с участием металлов. В зависимости от направления переноса заряда они классифицируются как перенос заряда от лиганда к металлу (LMCT) или от металла к лиганду (MLCT).
Комплексы LMCT возникают в результате переноса электронов от МО с лигандоподобным характером к электронам с металлоподобным характером. Этот тип переноса является преобладающим, если комплексы имеют лиганды с относительно высокоэнергетическими неподеленными парами (например, S или Se) или если металл имеет низколежащие пустые орбитали. Многие такие комплексы содержат металлы в высоких степенях окисления (даже d). Эти условия подразумевают, что акцепторный уровень доступен и имеет низкую энергию.
Рассмотрим d-октаэдрический комплекс, такой как IrBr 6, у которого уровни t 2g заполнены. Как следствие, наблюдается интенсивное поглощение около 250 нм, соответствующее переходу от лиганда σ MO к пустому e g MO. Однако в IrBr 6, который представляет собой d-комплекс, наблюдаются два поглощения, одно около 600 нм, а другое около 270 нм. Это связано с тем, что возможны два перехода: один в t 2g (который теперь может вместить еще один электрон), а другой - в e g. Полоса 600 нм соответствует переходу в МО t 2g, а полоса 270 нм - в МО e g.
Полосы переноса заряда могут также возникать в результате переноса электронов с несвязывающих орбиталей лиганда на e g МО.
| +7 | MnO 4< TcO4< ReO4 |
| +6 | CrO 4< MoO4< WO4 |
| +5 | VO4< NbO4< TaO4 |
Энергии переходов коррелируют с порядком электрохимического ряда. Наиболее легко восстанавливаемые ионы металлов соответствуют переходам с наименьшей энергией. Вышеупомянутая тенденция согласуется с переносом электронов от лиганда к металлу, что приводит к восстановлению ионов металла лигандом.
Примеры включают:
Комплексы металл (ион) с переносом заряда лигандом (MLCT) возникают в результате переноса электронов от МО с металлоподобным характером к электронам с лигандоподобным характером. Это чаще всего наблюдается в комплексах с лигандами, имеющими низколежащие π * -орбитали, особенно с ароматическими лигандами. Переход будет происходить при низкой энергии, если ион металла имеет низкую степень окисления, поскольку его d-орбитали будут относительно высокими по энергии.
Примеры таких лигандов, принимающих участие в MLCT, включают 2,2'-бипиридин (bipy), 1,10-фенантролин (phen), CO, CN и SCN. Примеры этих комплексов включают:
Фотореактивность комплексов MLCT является результатом природы окисленного металла и восстановленного лиганда. Хотя состояния традиционных комплексов MLCT, таких как Ru (bipy) 3 и Re (bipy) (CO) 3 Cl, по своей природе не были реактивными, некоторые комплексы MLCT, которые характеризуются реактивными состояниями MLCT, имеют были синтезированы.
Фоглер и Кункели считали комплекс MLCT изомером основного состояния, который содержит окисленный металл и восстановленный лиганд. Таким образом, различные реакции, такие как электрофильная атака и радикальные реакции на восстановленном лиганде, окислительное присоединение к металлическому центру из-за восстановленного лиганда и реакции переноса заряда во внешней сфере, могут быть отнесены к состояниям, возникающим в результате переходов MLCT. Реакционная способность состояний MLCT часто зависит от окисления металла. Последующие процессы включают ассоциативное замещение лиганда, образование эксиплекса и разрыв связей металл-металл.
 Рис. 1 I 2•PPh 3 комплексы с переносом заряда в CH2Cl2. Слева направо: (1) I 2 растворен в дихлорметане - нет комплекса CT. (2) Через несколько секунд после добавления избытка PPh 3 - образуется комплекс CT. (3) Через минуту после добавления избытка PPh 3 образовался комплекс CT [Ph 3 PI] I. (4) Сразу после добавления избытка I 2, который содержит [Ph 3 PI] [I 3].
Рис. 1 I 2•PPh 3 комплексы с переносом заряда в CH2Cl2. Слева направо: (1) I 2 растворен в дихлорметане - нет комплекса CT. (2) Через несколько секунд после добавления избытка PPh 3 - образуется комплекс CT. (3) Через минуту после добавления избытка PPh 3 образовался комплекс CT [Ph 3 PI] I. (4) Сразу после добавления избытка I 2, который содержит [Ph 3 PI] [I 3].Многие комплексы металлов окрашиваются из-за электронных переходов d-d. Видимый свет правильной длины волны поглощается, переводя более низкий d-электрон в более высокое возбужденное состояние. Это поглощение света вызывает цвет. Однако эти цвета обычно довольно тусклые. Это происходит из-за двух правил выбора . :
При продвижении электрон не должен изменять спин. Электронные переходы, в которых происходит изменение спина, называются запрещенными по спину, например, в запрещенных по спину реакциях.
dd переходы для комплексов, которые имеют центр симметрии запрещен - симметрия запрещена или запрещена по Лапорту.
Комплексы с переносом заряда не испытывают dd переходов. Таким образом, эти правила не действуют, и в целом поглощение очень интенсивное.
Например, классический пример комплекса с переносом заряда - это комплекс между йодом и крахмалом с образованием интенсивного пурпурного цвета. Это широко используется в качестве приблизительного прицела для фальшивой валюты. В отличие от большей части бумаги, бумага, используемая в валюте США, не содержит крахмала размера. Таким образом, появление пурпурного цвета при нанесении раствора йода указывает на подделку.
Гексафенилбензолы подобные H (фиг. 2) чрезвычайно хорошо подходят для образования комплексов с переносом заряда. Циклическая вольтамперометрия для H отображает 4 четко разделенных максимума, соответствующих от H вплоть до H, с первой ионизацией при E 1/2 всего 0,51 eV. Окисление этих аренов, например, додекаметилкарборанил (B) до синего кристаллического твердого комплекса HB, таким образом, является простым.
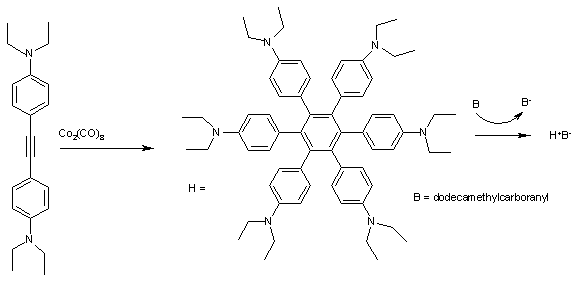
Все группы фенил расположены под углом около 45 ° да относительно центрального ароматического кольца и положительного заряда в катион-радикале следовательно, проходит через 6 бензольных колец в форме тороида . Комплекс имеет 5 полос поглощения в ближней инфракрасной области, которые могут быть отнесены к конкретным электронным переходам с помощью деконволюции и.
 Вид сбоку части кристаллической структуры гексаметиленовой соли с переносом заряда TTF / TCNQ, подчеркивая сегрегированное наложение.
Вид сбоку части кристаллической структуры гексаметиленовой соли с переносом заряда TTF / TCNQ, подчеркивая сегрегированное наложение.  Вид сбоку части кристаллическая структура соли гексаметилена TTF / TCNQ с переносом заряда. Расстояние между плоскостями TTF составляет 3,55 Å.
Вид сбоку части кристаллическая структура соли гексаметилена TTF / TCNQ с переносом заряда. Расстояние между плоскостями TTF составляет 3,55 Å. В 1954 году сообщалось, что соли с переносом заряда имели удельное сопротивление всего 8 Ом · см в комбинациях перилена с йодом или бром. В 1962 году было сообщено об известном акцепторе тетрацианохинодиметан (TCNQ). Тетратиафульвален (TTF) был синтезирован в 1970 году и оказался сильным донором электронов. В 1973 году было обнаружено, что комбинация этих компонентов образует прочный комплекс с переносом заряда, в дальнейшем называемый TTF-TCNQ. Комплекс образуется в растворе и может кристаллизоваться в хорошо сформированное кристаллическое твердое вещество. Твердое вещество демонстрирует почти металлическую электропроводность и было первым обнаруженным чисто органическим проводником. В кристалле TTF-TCNQ молекулы TTF и TCNQ расположены независимо в отдельных параллельно выровненных стопках, и перенос электрона происходит от донорных (TTF) к акцепторным (TCNQ) стопкам. Следовательно, электроны и электронные дырки разделены и сконцентрированы в стопках и могут перемещаться в одномерном направлении вдоль столбцов TCNQ и TTF соответственно, когда электрический потенциал прикладывается к концам кристалла в направление стека.
Сверхпроводимость проявляет тетраметил-тетраселенафульвален-гексафторфосфат (TMTSF 2PF6), который в условиях окружающей среды является полупроводником, проявляет сверхпроводимость при низкой температуре (критическая температура ) и высокое давление : 0,9 K и 12 k бар. Критические плотности тока в этих комплексах очень малы.