| |||
| |||
| Имена | |||
|---|---|---|---|
| Имена ИЮПАК Гуанидин. Иминометандиамин | |||
| Идентификаторы | |||
| Номер CAS | |||
| 3D-модель (JSmol ) | |||
| Ссылка Beilstein | 506044 | ||
| ChEBI | |||
| ChEMBL |
| ||
| ChemSpider | |||
| DrugBank | |||
| ECHA InfoCard | 100.003.656 | ||
| Номер EC |
| ||
| Справочная информация Gmelin | 100679 | ||
| IUPHAR/BPS | |||
| MeSH | Гуанидин | ||
| PubChem CID | |||
| UNII | |||
| Панель управления CompTox (EPA ) | |||
InChI
| |||
УЛЫБКИ
| |||
| Свойства | |||
| Химическая формула | CH5N3 | ||
| Молярная масса | 59,072 г · моль | ||
| Точка плавления | 50 ° C (122 ° F; 323 K) | ||
| log P | -1,251 | ||
| Кислотность (pK a) | 13,6 | ||
| Конъюгированная кислота | Гуанидиний | ||
| Термохимия | |||
| Стандартная энтальпия. формирование (ΔfH298) | -57 - -55 кДж моль | ||
| Стандартная энтальпия. горения (ΔcH298) | -1,0511 - -1,0531 МДж моль | ||
| Фармакология | |||
| Фармакокинетика : | |||
| Биологическая половина- жизнь | 7–8 часов | ||
| Опасности | |||
| Смертельная доза или концентрация (LD, LC): | |||
| LD50(средняя доза ) | 475 мг / кг (перорально, крыса) | ||
| Родственные соединения | |||
| Родственные соединения | |||
| Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки в информационном окне | |||
Гуанидин - это соединение с формулой HNC (NH 2)2. Это бесцветное твердое вещество, растворяющееся в полярных растворителях. Это прочная основа, которая используется при производстве пластмасс и взрывчатых веществ. Он обнаруживается в моче как нормальный продукт метаболизма белков . Фрагмент гуанидина также присутствует в более крупных органических молекулах, в том числе в боковой цепи аргинина.
Гуанидин можно рассматривать как азотистый аналог угольной кислоты. То есть группа C = O в угольной кислоте заменяется группой C = NH, и каждый OH заменяется группой NH. 2. Изобутилен можно рассматривать как аналог углерода во многих так же. Подробный кристаллографический анализ гуанидина был выяснен через 148 лет после его первого синтеза, несмотря на простоту молекулы. В 2013 году положения атомов водорода и параметры их смещения были точно определены с помощью дифракции нейтронов на монокристалле.
Гуанидин может быть получен из природных источников, сначала выделенный Адольф Стрекер посредством разложения гуанина. Впервые он был синтезирован в 1861 году путем окислительного разложения ароматического природного продукта, гуанина, выделенного из перуанского гуано.
. Лабораторный метод производства гуанидина - щадящий (180-190 ° C) термический разложение сухого тиоцианата аммония в безводных условиях:

Коммерческий путь включает двухстадийный процесс, начинающийся с реакции дициандиамида с солями аммония. Эта стадия аммонолиза посредством промежуточного соединения бигуанидина дает соли катиона гуанидиния (см. Ниже). На второй стадии соль обрабатывают основанием, таким как метоксид натрия.
с pK b 0,4, гуанидин - сильное основание. Большинство производных гуанидина фактически представляют собой соли, содержащие конъюгированную кислоту.
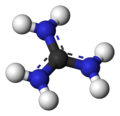
сопряженная кислота называется катионом гуанидиния, (C (NH. 2). 3). Этот плоский симметричный ион состоит из трех амино группы, каждая из которых связана с центральным атомом углерода ковалентной связью порядка 4/3. Это высокостабильный катион +1 в водном растворе благодаря эффективная резонансная стабилизация заряда и эффективная сольватация молекулами воды. В результате его pKa равен 13,6, что означает, что гуанидин является очень сильным основанием в воде; в нейтральной воде, он существует почти исключительно в виде гуанидиния.

Гуанидин может быть выборочно обнаружен с использованием 1,2- нафтохинон-4-сульфоновая кислота (реагент Фолина ) и подкисленная мочевина.
Основная соль, представляющая коммерческий интерес, - нитрат [C (NH. 2)3] NO. 3. Он используется в качестве пропеллента, например, в подушках безопасности.
Гуанидин существует в протонированном виде, как гуанидин, в растворе при физиологическом pH.
Хлорид гуанидиния (также известный как гидрохлорид гуанидина) обладает хаотропными свойствами и используется для денатурирования белков. Хлорид гуанидиния, как известно, денатурирует белки с линейной зависимостью между концентрацией и свободной энергией разворачивания. В водных растворах, содержащих 6 M гуанидинхлорид, почти все белки теряют всю свою вторичную структуру и становятся случайно скрученными пептидными цепями. Тиоцианат гуанидиния также используется из-за его денатурирующего действия на различные биологические образцы.
гуанидин хлорида используется в качестве адъюванта в лечении ботулизма, введенный в 1968 году, но теперь его роль считается спорным - потому, что у некоторых пациентов не было никакого улучшения после приема этого препарата.
Гидроксид гуанидиния является активным ингредиентом некоторых не содержащих щелок средств для расслабления волос.
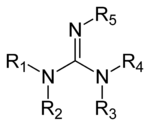 Общая структура гуанидина
Общая структура гуанидина Гуанидины представляют собой группу органических соединений, имеющих общую функциональную группу с общей структурой (R. 1R. 2N) (R. 3R. 4N) C = N-R. 5. Центральной связью в этой группе является связь имина, и группа структурно связана с амидинами и мочевинами. Примерами гуанидинов являются аргинин, триазабициклодецен, сакситоксин и креатин.
Галегин изоамиленгуанидин.