 | |
| Клинические данные | |
|---|---|
| Торговые наименования | Ongentys |
| Другие названия | BIA 9 -1067 |
| AHFS / Drugs.com | Монография |
| Данные лицензии | |
| Беременность. категория |
|
| Способы введения. | Внутрь (капсулы ) |
| код АТС | |
| Правовой статус | |
| Правовой статус | |
| Фармакокинетические данные | |
| Биодоступность | ~ 20% |
| Связывание с белками | 99,9% |
| Метаболизм | В основном сульфатирование, также восстановление, глюкуронирование, метилирование |
| Период полувыведения | от 0,7 до 3,2 часа |
| Продолжительность действия | >24 часа |
| Экскреция | Кал (67%), моча (13%) |
| Идентификаторы | |
Название ИЮПАК
| |
| Номер CAS | |
| PubChem CID | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| ChEBI | |
| ChEMBL |
|
| Химические и физические данные | |
| Формула | C15H10Cl2N4O6 |
| Молярная масса | 413,17 г · моль |
| 3D-модель ( JSmol ) | |
УЛЫБКИ
| |
InChI
| |
Опикапон, продаваемый под торговой маркой Ongentys, представляет собой лекарство, которое вводится вместе с леводопа у людей с болезнью Паркинсона.
Наиболее частыми побочными эффектами являются дискинезия (трудности с контролем движения), запор, повышение креатинкиназы, гипотония / обморок и снижение веса.
опикапон, работает для восстановления уровней дофамин в частях мозга, которые контролируют движение и координацию. Он усиливает действие леводопы, копии нейромедиатора дофамина, которую можно принимать внутрь. Опикапон блокирует фермент, который участвует в расщеплении леводопы в организме, называемый катехол-O-метилтрансферазой (COMT). В результате леводопа остается активным дольше. Это помогает улучшить симптомы болезни Паркинсона, такие как скованность и замедленность движений.
В июне 2016 года он был разрешен для использования в Европейском Союзе. Он был разрешен к применению в США в апреле 2020 года.
В ЕС опикапон является показан в качестве дополнительной терапии к препаратам леводопа / ингибиторов декарбоксилазы ДОФА (DDCI) у взрослых с болезнью Паркинсона и двигательными колебаниями в конце дозы, которые не могут быть стабилизированы этими комбинациями.
В США опикапон показан как дополнительное лечение леводопы / карбидопа у пациентов с болезнью Паркинсона (БП), испытывающих «неактивные» эпизоды.
Ингибитор СОМТ опикапон используется в качестве добавки к комбинации леводопы и Ингибитор ДОФА декарбоксилазы для лечения пациентов с болезнью Паркинсона, испытывающих двигательные колебания в конце приема, если они не могут быть стабилизируется этой комбинацией лекарств.
Этот препарат противопоказан людям с раком, который выделяет катехоламины (например, адреналин ), например феохромоцитома или параганглиома, потому что в качестве ингибитора СОМТ он блокирует разложение катехоламинов. Другими противопоказаниями являются злокачественный нейролептический синдром (ЗНС) или нетравматический рабдомиолиз в анамнезе, а также комбинация с ингибиторами моноаминоксидазы, которые не используются в качестве противопаркинсонических средств, поскольку возможных лекарственных взаимодействий.
NMS и связанный с ним рабдомиолиз редко наблюдались при применении более старых ингибиторов COMT толкапон и энтакапон. Обычно это происходит вскоре после начала дополнительной терапии ингибитором СОМТ, когда доза леводопы была снижена, или после прекращения приема ингибитора СОМТ.
Опикапон противопоказан людям с одновременным применением неселективного моноамина Ингибиторы оксидазы (МАО) или люди с феохромоцитомой, параганглиомой или другими новообразованиями, секретирующими катехоламины.
Люди, принимающие опикапон, очень часто (18%) испытывают дискинезию. Другие частые побочные эффекты (у 1-10% пациентов) включают головокружение, странные сны, галлюцинации, запор, сухость во рту, ортостатическая гипотензия (низкое кровяное давление) и мышечные спазмы. Помимо спазмов, эти побочные эффекты известны также у толкапона и энтакапона.
Как и в случае энтакапона, в исследованиях не было обнаружено соответствующей токсичности для печени. Это отличается от первого ингибитора СОМТ толкапона, который может вызвать - в некоторых случаях летальный - печеночная недостаточность.
Специфический антидот неизвестен.
Ингибиторы моноаминоксидазы (ингибиторы МАО) - это еще один класс лекарств, блокирующих разложение катехоламинов. Следовательно, их комбинация с опикапоном может привести к увеличению концентрации катехоламинов в организме и соответствующим побочным эффектам. Комбинация антипаркинсонических ингибиторов МАО селегилин или разагилин с опикапоном считается безопасным. Возможно также взаимодействие с лекарствами, метаболизируемыми COMT (например, изопреналин, адреналин, дофамин или добутамин ), трициклическими антидепрессантами и антидепрессанты типа ингибитор обратного захвата норэпинефрина. Возможные фармакокинетические взаимодействия связаны с субстратами печеночного фермента CYP2C8, такими как репаглинид, и белком-переносчиком SLCO1B1, например симвастатин.
Опикапон блокирует фермент катехол-O-метилтрансферазу (COMT) эффективно (>90% в терапевтических дозах), селективно и обратимо, и только вне центральная нервная система. Он медленно отделяется от СОМТ, в результате чего продолжительность действия превышает 24 часа, несмотря на его короткий период полувыведения из плазмы крови. Поскольку COMT и декарбоксилаза DOPA являются основными ферментами для разложения леводопы, их блокирование эффективно увеличивает его концентрацию в кровотоке. Больше леводопа достигает головного мозга, где он активируется до дофамина.
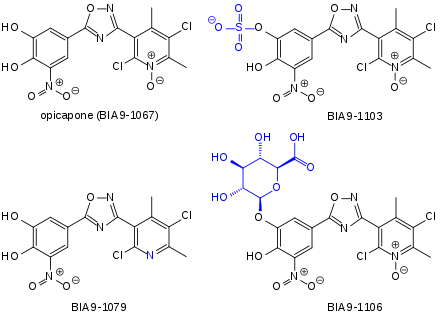 Опикапона и некоторых его метаболитов: основного неактивного метаболита сульфата опикапона (BIA 9-1103), активного сниженного производное (BIA 9-1079) и неактивный глюкуронид (BIA 9-1106).
Опикапона и некоторых его метаболитов: основного неактивного метаболита сульфата опикапона (BIA 9-1103), активного сниженного производное (BIA 9-1079) и неактивный глюкуронид (BIA 9-1106). Вещество быстро всасывается из кишечника, но только примерно до 20% от введенной дозы. Самые высокие концентрации в плазме крови достигаются через 1–2,5 часа. Находясь в кровотоке, он почти полностью (99,9%) связывается с белками плазмы, но, очевидно, с другими сайтами связывания, чем варфарин, дигоксин и другие препараты с высокое сродство к белкам плазмы. В основном он метаболизируется до сульфата, на долю которого приходится 67% циркулирующего лекарства после однократного приема, и до метилированного производного, на долю которого приходится 21%. Незначительные метаболиты представляют собой восстановленное производное (<10%) и глюкуронид. Все эти метаболиты неактивны, за исключением восстановленного производного. Опикапон выводится с конечным периодом полувыведения от 0,7 до 3,2 часа. В основном он выводится с фекалиями (67%), а в форме глюкуронида также через почки (13%). Сульфат имеет гораздо более длительный период полураспада - от 94 до 122 часов.
Сульфат опикапона переносится SLCO1B1; не исключена возможность того, что он заблокирует этот транспортер. Сам опикапон и сульфат также переносятся рядом других белков, но, учитывая низкие концентрации свободных веществ в плазме крови, очень маловероятно, что это приведет к лекарственным взаимодействиям. Опикапон - слабый ингибитор печеночных ферментов CYP1A2, CYP2B6, CYP2C8 и CYP2C9. Единственное взаимодействие CYP, обнаруженное в исследованиях, которое, вероятно, имеет отношение к делу, - это взаимодействие с репаглинидом, который метаболизируется CYP2C8. Метаболизм варфарина, субстрата CYP2C9, не подвергается значительному влиянию.
Опикапон был разрешен для медицинского применения в Европейском Союзе в июне 2016 года.
В феврале 2017 года, его разработчик Bial продал эксклюзивные права на маркетинг в США и Канаде Neurocrine Biosciences за первоначальный взнос в размере 30 миллионов долларов США.
Opicapone был разрешен для медицинского использования в США в апреле 2020 года.
Опикапон был одобрен на основании данных двух клинических испытаний (испытание 1 / NCT01568073 и испытание 2 / NCT01227655) с 522 участниками с болезнью Паркинсона (БП), симптомы которых не улучшались. контролируются при их регулярном лечении PD. Испытание 1 проводилось в 104 центрах в 19 европейских странах, а исследование 2 - в 69 центрах в Аргентине, Австралии, Бельгии, Чили, Чешской Республике, Эстонии, Индии, Израиле, Южной Корее, России, Южной Африке и Великобритании.
Было проведено два 12-недельных испытания с участием участников с болезнью Паркинсона (БП) с неадекватным контролем симптомов Паркинсона (время «выключения») при приеме препаратов карбидопа / леводопа для ПД. Участники были отобраны случайным образом для приема капсулы опикапона или плацебо один раз в день. Ни участники, ни медицинские работники не знали, какое лечение им проводилось, пока испытание не было завершено.
Во всех испытаниях участники вели ежедневные дневники количества часов отдыха для троих. дней до оценочного визита. Польза оценивалась путем измерения отклонения от исходного уровня общего ежедневного времени «отдыха» у участников, получавших опикапон и плацебо.