В химических науках метилирование означает добавление метильной группы к субстрату или замену атома (или группы) метильной группой. Метилирование - это форма алкилирования, при которой метильная группа заменяет атом водорода. Эти термины обычно используются в химии, биохимии, почвоведении и биологических науках.
В биологических системах, метилирование, катализируемой с помощью ферментов ; такое метилирование может быть вовлечено в модификацию тяжелых металлов, регуляцию экспрессии генов, регуляцию функции белков и процессинг РНК. Метилирование образцов ткани in vitro также является одним из методов уменьшения некоторых артефактов гистологического окрашивания. Аналог метилирования называется деметилированием.
В биологических системах метилирование осуществляется ферментами. Метилирование может изменять тяжелые металлы, регулировать экспрессию генов, процессинг РНК и функцию белков. Это было признано ключевым процессом, лежащим в основе эпигенетики.
Метаногенез, процесс образования метана из CO 2, включает серию реакций метилирования. Эти реакции осуществляются набором ферментов, содержащихся в семействе анаэробных микробов.
 Цикл метаногенеза, показывающий промежуточные продукты.
Цикл метаногенеза, показывающий промежуточные продукты. В обратном метаногенезе метан служит метилирующим агентом.
Многие фенолы подвергаются O-метилированию с образованием производных анизола. Этот процесс, катализируемый ферменты, такие как caffeoyl-СоА - O-метилтрансфераза, является реакцией ключевой роли в биосинтезе lignols, percursors к лигнину, основному структурному компонент растений.
Растения продуцируют флавоноиды и изофлавоны с метилированием по гидроксильным группам, то есть метокси-связями. Это 5-O-метилирование влияет на растворимость флавоноидов в воде. Примерами являются 5-O-метилгенистеин, 5-O-метилмирицетин или 5-O-метилкверцетин, также известный как азалеатин.
Вместе с убиквитином и фосфорилированием метилирование является основным биохимическим процессом изменения функции белка. Наиболее распространенные белковые метилирования продуцируют специфические гистоны из аргинина и лизина. В противном случае гистидин, глутамат, аспарагин, цистеин подвержены метилированию. Некоторые из этих продуктов включают S- метилцистеин, два изомера N- метилгистидина и два изомера N- метиларгинина.
 Реакция метилирования катализируется метионинсинтазой.
Реакция метилирования катализируется метионинсинтазой. Метионинсинтаза регенерирует метионин (Met) из гомоцистеина (Hcy). Общая реакция превращает 5-метилтетрагидрофолат (N 5 -MeTHF) в тетрагидрофолат (THF) при переносе метильной группы в Hcy с образованием Met. Метионинсинтазы могут быть кобаламин-зависимыми и кобаламин-независимыми: растения имеют и то, и другое, животные зависят от метилкобаламин-зависимой формы.
В метилкобаламин-зависимых формах фермента реакция протекает в две стадии в реакции пинг-понга. Фермент изначально переходит в реактивное состояние путем переноса метильной группы от N 5 -MeTHF на Co (I) в связанном с ферментом кобаламине (Cob), образуя метилкобаламин (Me-Cob), который теперь содержит Me-Co. (III) и активация фермента. Затем Hcy, который координируется с ферментом связанным цинком с образованием реактивного тиолата, вступает в реакцию с Me-Cob. Активированная метильная группа переносится от Me-Cob к тиолату Hcy, который регенерирует Co (I) в Cob, и Met высвобождается из фермента.
Биометилирование - это путь превращения некоторых тяжелых элементов в более мобильные или более летальные производные, которые могут попасть в пищевую цепь. Biomethylation из мышьяка соединений начинается с образованием methanearsonates. Таким образом, трехвалентные неорганические соединения мышьяка метилируются с образованием метанарсоната. S-аденозилметионин является донором метила. Метанарсонаты являются предшественниками диметиларсонатов, опять же по циклу восстановления (до метиларсоновой кислоты) с последующим вторым метилированием. Связанные пути применяются к биосинтезу в метилртути.
Метилирование ДНК у позвоночных обычно происходит в сайтах CpG ( сайты цитозин-фосфат-гуанин, то есть там, где за цитозином непосредственно следует гуанин в последовательности ДНК). Это метилирование приводит к превращению цитозина в 5-метилцитозин. Образование Me-CpG катализируется ферментом ДНК-метилтрансферазой. У млекопитающих метилирование ДНК является обычным явлением в клетках организма, а метилирование сайтов CpG, по-видимому, является стандартным. ДНК человека имеет около 80–90% метилированных сайтов CpG, но есть определенные области, известные как островки CpG, которые богаты CG (высокое содержание цитозина и гуанина, состоящее примерно из 65% остатков CG), где ни один из них не метилирован.. Они связаны с промоторами 56% генов млекопитающих, включая все гены, экспрессирующиеся повсеместно. От одного до двух процентов генома человека составляют кластеры CpG, и существует обратная зависимость между метилированием CpG и транскрипционной активностью. Метилирование, способствующее эпигенетическому наследованию, может происходить либо за счет метилирования ДНК, либо за счет метилирования белка. Неправильное метилирование генов человека может привести к развитию болезней, в том числе рака. Точно так же метилирование РНК происходит у разных видов РНК, а именно. тРНК, рРНК, мРНК, tmRNA, мяРНК, snoRNA, микроРНК, и вирусный РНК. Для метилирования РНК различными РНК-метилтрансферазами используются разные каталитические стратегии. Считается, что метилирование РНК существовало до метилирования ДНК в ранних формах жизни, развивающейся на Земле.
N6-метиладенозин (m6A) является наиболее распространенной и широко распространенной модификацией метилирования в молекулах РНК (мРНК), присутствующих у эукариот. 5-метилцитозин (5-mC) также часто встречается в различных молекулах РНК. Последние данные убедительно свидетельствуют о том, что метилирование РНК m6A и 5-mC влияет на регуляцию различных биологических процессов, таких как стабильность РНК и трансляция мРНК, и что аномальное метилирование РНК вносит вклад в этиологию заболеваний человека.
Метилирование белка обычно происходит на аминокислотных остатках аргинина или лизина в последовательности белка. Аргинин может быть метилирован один раз (монометилированный аргинин) или дважды с помощью обеих метильных групп на одном концевом азоте ( асимметричный диметиларгинин ) или одной на обоих атомах азота (симметричный диметиларгинин) протеин-аргинин-метилтрансферазами (PRMTs). Лизин может быть метилирован один, два или три раза лизинметилтрансферазами. Метилирование белков наиболее изучено в гистонах. Перенос метильных групп от S-аденозилметионина к гистонам катализируется ферментами, известными как гистоновые метилтрансферазы. Гистоны, которые метилированы по определенным остаткам, могут действовать эпигенетически, подавляя или активируя экспрессию генов. Метилирование белков - это один из типов посттрансляционной модификации.
Метаболизм очень древний и может быть обнаружен у всех организмов на Земле, от бактерий до людей, что указывает на важность метаболизма метила для физиологии. Действительно, фармакологическое подавление глобального метилирования у различных видов, от человека, мышей, рыб, мух, круглых червей, растений, водорослей и цианобактерий, вызывает те же эффекты на их биологические ритмы, демонстрируя сохраняющуюся физиологическую роль метилирования в процессе эволюции.
Термин метилирование в органической химии относится к процессу алкилирования, используемому для описания доставки группы CH 3.
Метилирование обычно проводят с использованием электрофильных источников метила, таких как йодметан, диметилсульфат, диметилкарбонат или хлорид тетраметиламмония. Менее распространенные, но более мощные (и более опасные) метилирующие реагенты включают метилтрифлат, диазометан и метилфторсульфонат ( магический метил ). Все эти реагенты реагируют посредством нуклеофильных замещений S N 2. Например, карбоксилат может быть метилирован кислородом с образованием метилового эфира ; алкоксид соль RO - может быть аналогичным образом метилированный с получением эфира, Рох 3 ; или енолят кетона можно метилировать на углероде с образованием нового кетона.

Метилирование Парди является специфическим для метилирования при кислороде углеводов с использованием иодметана и оксида серебра.
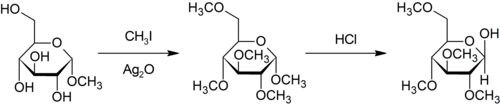
Реакция Эшвейлера – Кларка - метод метилирования аминов. Этот метод позволяет избежать риска кватернизации, которая возникает при метилировании аминов метилгалогенидами.

Диазометан и более безопасный аналог триметилсилилдиазометанметилата карбоновых кислот, фенолов и даже спиртов:
Преимущество метода заключается в том, что побочные продукты легко удаляются из смеси продуктов.
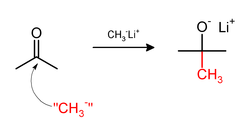
Метилирование иногда включает использование нуклеофильных метильных реагентов. Сильно нуклеофильные метилирующие агенты включают метиллитий (CH 3 Li) или реагенты Гриньяра, такие как бромид метилмагния (CH 3 MgX). Например, CH 3 Li будет добавлять метильные группы к карбонилу ( C = O ) кетонов и альдегидов:
Более мягкие метилирующие агенты включают тетраметилолово, диметилцинк и триметилалюминий.