Глифлозины - это класс препаратов для лечения диабета 2 типа (T2D). Они действуют путем ингибирования котранспортера натрия / глюкозы 2 (SGLT-2) и поэтому также называются ингибиторами SGLT-2. Эффективность препарата зависит от почечной экскреции и предотвращает попадание глюкозы в кровообращение, способствуя глюкозурии. Механизм действия инсулино-независимый.
Три препарата были одобрены Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) в США ; дапаглифлозин, канаглифлозин и эмпаглифлозин. Канаглифлозин был первым ингибитором SGLT-2, одобренным FDA в марте 2013 года. Дапаглифлозин и эмпаглифлозин были приняты в 2014 году.
Существует не менее четырех членов SLC -5 генное семейство, которые являются вторичными активными переносчиками глюкозы. Белки-переносчики натрия глюкозы SGLT-1 и SGLT-2 являются двумя главными членами этого семейства. Эти два члена обнаруживаются в почках, среди других транспортеров, и являются там основными ко-транспортерами, связанными с сахаром в крови. Они играют роль в реабсорбции глюкозы в почках и в абсорбции глюкозы в кишечнике.
Глюкоза крови свободно фильтруется клубочками, а SGLT-1 и SGLT-2 реабсорбируют глюкозу в почках и помещают ее обратно в циркуляционные ячейки. SGLT-2 отвечает за 90% реабсорбции, а SGLT-1 - за остальные 10%.
ко-переносчик натрия / глюкозы (SGLT ) белки связаны с клеточной мембраной и выполняют роль транспорта глюкозы через мембрану в клетки против градиента концентрации глюкозы. Это делается с помощью градиента натрия, создаваемого насосами натрий / калий АТФаза, поэтому одновременно с глюкозой в клетки транспортируется натрий. Поскольку он против градиента, для его работы требуется энергия. Белки SGLT вызывают реабсорбцию глюкозы из клубочкового фильтрата, независимо от инсулина.
SGLT-2 является членом семейства переносчиков глюкозы и имеет низкое сродство, транспортер глюкозы большой емкости. SGLT-2 в основном экспрессируется в сегментах S-1 и S-2 проксимальных почечных канальцев, где абсорбируется большая часть отфильтрованной глюкозы. SGLT-2 играет роль в регуляции глюкозы и отвечает за большую часть реабсорбции глюкозы в почках.
При диабете концентрация внеклеточной глюкозы увеличивается, и этот высокий уровень глюкозы приводит к активации SGLT. -2, что, в свою очередь, приводит к большему всасыванию глюкозы в почках. Эти эффекты вызывают поддержание гипергликемии. Поскольку натрий всасывается одновременно с глюкозой через SGLT-2, активация SGLT-2, вероятно, приводит к развитию или поддержанию гипертензии. В исследовании, в котором крысам давали рамиприл или лозартан, уровни белка SGLT-2 и мРНК были значительно снижены. У пациентов с диабетом гипертония является распространенной проблемой, поэтому это может иметь отношение к этому заболеванию.
Лекарства, которые ингибируют котранспортер натрия / глюкозы 2, подавляют реабсорбцию глюкозы почками, что приводит к усилению экскреции глюкозы с мочой и снижению содержания глюкозы в крови. Они работают независимо от инсулина и могут снижать уровень глюкозы, не вызывая гипогликемии или увеличения веса.
Средневековые врачи обычно пробовали мочу и писали беседы о своих наблюдениях. Врач, который первоначально думал, что сахарный диабет был заболеванием почек из-за глюкозы, обнаруженной в моче, по-видимому, утерян. После открытия инсулина основное внимание при лечении диабета было сосредоточено на поджелудочной железе. Традиционные направления терапевтических стратегий при диабете заключались в усилении секреции эндогенного инсулина и улучшении чувствительности к инсулину. В предыдущее десятилетие изучалась роль почек в развитии и поддержании высоких уровней глюкозы. Роль почек привела к разработке лекарств, которые ингибируют белок транспортера 2 натрия / глюкозы. Каждый день около 180 граммов глюкозы фильтруется через клубочки и теряется с первичной мочой у здоровых взрослых, но более 90% глюкозы, которая изначально фильтруется, реабсорбируется системой высокой емкости, контролируемой SGLT. -2 в раннем извитом сегменте проксимальных канальцев. Почти вся оставшаяся отфильтрованная глюкоза реабсорбируется транспортером натрия / глюкозы 1, поэтому при нормальных обстоятельствах почти вся отфильтрованная глюкоза будет реабсорбироваться, и менее 100 мг глюкозы попадает в мочу людей, не страдающих диабетом. 128>
 Флоризин
Флоризин Флоризин - соединение, известное уже более века. Это природный ботанический глюкозид, который вызывает почечную глюкозурию и блокирует всасывание глюкозы в кишечнике за счет ингибирования натрий / глюкозных симпортеров, расположенных в проксимальных почечных канальцах и слизистой оболочке. тонкой кишки. Флоризин был впервые выделен в 1835 году, и впоследствии было обнаружено, что он является мощным, но довольно неизбирательным ингибитором белков SGLT-1 и SGLT-2.
Флоризин, по-видимому, обладал очень интересными свойствами и результатами исследований на животных были обнадеживающими, это улучшило чувствительность к инсулину, а на моделях крыс с диабетом казалось, что уровень глюкозы в моче увеличился, а также нормальная концентрация глюкозы в плазме наблюдалась без гипогликемии. К сожалению, несмотря на эти свойства, флоризин не подходил для клинической разработки по нескольким причинам. Флоризин имеет очень низкую биодоступность при пероральном приеме, поскольку он расщепляется в желудочно-кишечном тракте, поэтому его следует вводить парентерально. Флоретин, активный метаболит флоризина, является мощным ингибитором стимулирующих переносчиков глюкозы, и флоризин, по-видимому, вызывает серьезные побочные эффекты в желудочно-кишечном тракте, такие как диарея и обезвоживание. По этим причинам флоризин никогда не применялся на людях.
Хотя флоризин не подходил для дальнейших клинических испытаний, он сыграл важную роль в разработке ингибиторов SGLT-2. Это послужило основой для признания ингибиторов SGLT с улучшенными профилями безопасности и переносимости. Например, ингибиторы SGLT не связаны с нежелательными явлениями со стороны желудочно-кишечного тракта, и их биодоступность намного выше.
Ингибирование SGLT-2 приводит к лучшему контролю уровня глюкозы, более низкому инсулину, более низкому кровяному давлению и уровни мочевой кислоты и увеличивает расход калорий. Некоторые данные подтверждают гипотезу о том, что ингибирование SGLT-2 может иметь прямое ренопротекторное действие. Это включает действия по ослаблению канальцевой гипертрофии и гиперфильтрации, связанных с диабетом, и по снижению канальцевой токсичности глюкозы. Ингибирование SGLT-2 после лечения дапаглифлозином снижает способность канальцев к реабсорбции глюкозы примерно на 30–50%.
Флоризин состоит из глюкозного фрагмента и двух ароматические кольца (агликоновый фрагмент), соединенные алкильным спейсером. Первоначально флоризин был выделен для лечения лихорадки и инфекционных заболеваний, в частности малярии. По словам и его партнеров, в 1950-х годах были проведены исследования флоризина, которые показали, что он может блокировать транспорт сахара в почках, тонком кишечнике и некоторых других тканях. В начале 1990-х котранспортер натрия / глюкозы 2 был полностью охарактеризован, поэтому механизм действия флоризина стал представлять реальный интерес. В более поздних исследованиях было сказано, что сахароблокирующие эффекты флоризина были связаны с ингибированием белков-котранспортеров натрия / глюкозы.
Большинство зарегистрированных ингибиторов SGLT-2 являются аналогами глюкозида, которые могут можно проследить до о-арилглюкозида, встречающегося в природе. Проблема с использованием о-глюкозидов в качестве ингибиторов SGLT-2 заключается в нестабильности, разложение которой можно отслеживать с помощью β-глюкозидазы в тонком кишечнике. По этой причине о-глюкозиды, вводимые перорально, должны быть эфирами пролекарства. Эти пролекарства претерпевают изменения в организме, приводящие к углерод-углеродной связи между глюкозой и агликоновой составляющей, поэтому с-глюкозид образуются из о-глюкозидов.. С-глюкозиды имеют фармакокинетический профиль, отличный от о-глюкозидов (например, период полувыведения и продолжительность действия), и не разлагаются β-глюкозидазой. Первым открытым c-глюкозидом был препарат дапаглифлозин. Дапаглифлозин был первым высокоселективным ингибитором SGLT-2, одобренным Европейским агентством по лекарственным средствам. Все ингибиторы SGLT-2, находящиеся в клинической разработке, являются пролекарствами, которые для активности должны быть преобразованы в его активную форму «А».
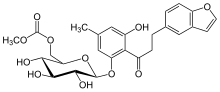 Структура T-1095
Структура T-1095 Поскольку Флоризин является неселективным ингибитором с плохой пероральной биодоступностью, было синтезировано производное флоризина, получившее название Т-1095. Т-1095 представляет собой пролекарство метилкарбоната, которое всасывается в кровоток при пероральном введении и быстро превращается в печени в активный метаболит Т-1095А. За счет ингибирования SGLT-1 и SGLT-2 экскреция глюкозы с мочой увеличивалась у диабетических животных. T-1095 не прошел клиническую разработку, вероятно, из-за ингибирования SGLT-1, но неселективные ингибиторы SGLT могут также блокировать переносчик глюкозы 1 (GLUT-1). Поскольку 90% отфильтрованной глюкозы реабсорбируется через SGLT-2, исследования были сосредоточены именно на SGLT-2. Ингибирование SGLT-1 может также привести к генетическому заболеванию мальабсорбции глюкозы-галактозы, которое характеризуется тяжелой диареей.
Согласно предварительным данным новый метод ингибирования SGLT-2, антисмысловой олигонуклеотид ISIS 388626 улучшил уровень глюкозы в плазме у грызунов и собак за счет снижения экспрессии мРНК в проксимальных почечных канальцах на величину до 80% при приеме раз в неделю. На SGLT-1 это не повлияло. Результаты исследования длительного использования ISIS 388626 у нечеловеческих приматов выявили более чем 1000-кратное увеличение глюкозурии без какой-либо связанной с этим гипогликемии. Это увеличение глюкозурии может быть связано с дозозависимым снижением экспрессии SGLT-2, где самая высокая доза приводила к снижению более чем на 75%. В 2011 году Ionis Pharmaceuticals инициировала клиническое исследование фазы 1 с ISIS-SGLT-2RX, 12-нуклеотидным антисмысловым олигонуклеотидом. Результаты этого исследования были опубликованы в 2017 году, и лечение было «связано с неожиданными почечными эффектами». Авторы пришли к выводу, что «прежде чем концепция антисмыслового блокирования SGLT2 с помощью ISIS 388626 может быть исследована дальше, необходимы дополнительные доклинические данные, чтобы оправдать дальнейшие исследования».
Майкл Наук рассказывает, что метаанализ исследований активности ингибиторов SGLT-2 в контроле гликемии у пациентов типа 2 У пациентов с сахарным диабетом наблюдается улучшение контроля уровня глюкозы по сравнению с плацебо, метформином, сульфонилмочевиной, тиазолидиндионами, инсулином и другими. HbA1c исследовали после того, как ингибиторы SGLT-2 давали отдельно (в качестве монотерапии) и в качестве дополнительной терапии к другим лекарствам от диабета. В качестве ингибиторов SGLT-2 использовались дапаглифлозин, канаглифлозин и другие препараты того же класса. Метаанализ был проведен на основе исследований, продолжавшихся от нескольких недель до более 100 недель.
Суммированные результаты заключались в том, что 10 мг дапаглифлозина показали больший эффект, чем плацебо, в контроле глюкозы. при приеме в течение 24 недель. Однако не было показано худшей эффективности 10 мг дапаглифлозина при применении в качестве дополнительной терапии к метформину по сравнению с глипизидом после использования в течение 52 недель. 10 мг дапаглифлозина не показали меньшей эффективности по сравнению с метформином, когда оба препарата применялись в виде монотерапии в течение 24 недель.
Результаты метаанализа при исследовании канаглифлозина показали, что сравнение к плацебо канаглифлозин влияет на HbA1c. Исследования метаанализа также показали, что 10 мг и 25 мг эмпаглифлозина улучшили HbA1c по сравнению с плацебо.
агликоны и флоризин, и дапаглифлозин обладают слабым ингибирующим действием на SGLT-1 и SGLT-2. Две синергические силы участвуют в связывании ингибиторов с SGLT. Различные сахара на агликоне будут влиять и изменять его ориентацию в преддверии доступа, потому что одна из сил, участвующих в связывании, - это связывание сахара с сайтом глюкозы. Другой силой является связывание агликона, которое влияет на аффинность связывания всего ингибитора.
Открытие Т-1095 привело к исследованию того, как повысить эффективность, селективность и биодоступность при пероральном введении путем добавления различных заместителей. к гликозидному ядру. В качестве примера мы можем взять изменение о-гликозидов на с-гликозиды путем создания углерод-углеродной связи между глюкозой и агликоновым фрагментом. С-глюкозиды более стабильны, чем о-глюкозиды, что приводит к изменению периода полураспада и продолжительности действия. Эти модификации также привели к большей специфичности SGLT-2. С-глюкозиды, которые имеют гетероциклическое кольцо в дистальном кольце или проксимальном кольце, лучше, когда дело доходит до антидиабетического эффекта и физико-химических свойств вместе взятых. С-глюкозид, несущий тиазол на дистальном кольце канаглифлозина, продемонстрировал хорошие физико-химические свойства, которые могут привести к клиническому развитию, но все же обладает такой же антидиабетической активностью, что и дапаглифлозин, как показано в таблицах 1 и 2.
Сонг и его партнеры получили тиазольное соединение, исходя из карбоксильной кислоты. Работая с этим, им потребовалось три этапа, чтобы получить такое соединение, как дапаглифлозин, с тиазольным кольцом. Тормозящее действие соединений на SGLT-2 было испытано Сонгом и его партнерами. В таблицах 1, 2 и 3 значение IC 50 изменяется в зависимости от того, какое соединение находится в положении кольца, в области C-4 проксимального фенильного кольца и как соотносится тиазольное кольцо. 128>
Многие соединения дают различное значение IC 50 в положении кольца при активности in vitro. Например, была большая разница, если была н-пентильная группа (IC 50 = 13,3 нМ), н-бутил (IC 50 = 119 нМ), фенил с 2-фурилом (IC 50 = 0,720) или 3-тиофенилом (IC 50 = 0,772). Как видно из таблицы 1, активность in vitro увеличивается в зависимости от того, какое соединение связано с дистальным кольцом (учитывая, что в области C-4 проксимального фенильного кольца находится атом Cl).
Таблица 1: Различия в активности in vitro в зависимости от того, какое соединение связано с дистальным кольцом.
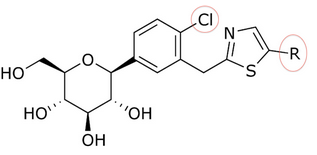
| R | IC50(nM) | Activity |
|---|---|---|
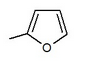 | 0.720 | активность in vitro улучшилась * |
 | 1,14 | активность in vitro улучшилась * |
| 13,3 | По мере увеличения количества атомов углерода значение IC-50 колеблется | |
| 19,6 | активность in vitro снизилась * | |
 | 21.2 | активность in vitro снизилась * |
* компаратор с этильной группой (IC 50 = 16,7)
В таблице 2 активность in vitro изменяется в зависимости от соединения в области C-4 проксимального фенильного кольца (X). Небольшие метильные группы или другие атомы галогена в положении C-4 дали IC 50 в диапазоне 0,72–36,7 (при условии, что фенил с 2-фурилом находится в положении кольца).
Таблица 2: Различия в активности in vitro в зависимости от того, какое соединение находится в области C-4 проксимального фенильного кольца.

| X | IC50(нМ) |
|---|---|
| Cl | 0,720 |
| Me | 1,43 |
| F | 6,11 |
| H | 22,6 |
| CN | 36,7 |
Таблица 3: Разница в значении IC 50 в зависимости от того, как относится тиазольное кольцо (в структуре больше ничего не изменяется (X = Cl, R = фенил с 2-фурилом).
| Соединение | IC50(нМ) |
|---|---|
 | 0,720 |
 | 1,11 |