 | |
 | |
| Клинические данные | |
|---|---|
| Торговые наименования | Velcade, Chemobort, Bortecad, другие |
| Другие названия | PS-341 |
| AHFS / Drugs.com | Монография |
| MedlinePlus | a607007 |
| Данные лицензии |
|
| Беременность. категория |
|
| Способы. введения | Подкожно, внутривенное |
| код АТС | |
| Legal st atus | |
| Юридический статус | |
| фармакокинетические данные | |
| Связывание с белками | 83% |
| Метаболизм | Печень, CYP активно участвует |
| Период полувыведения | от 9 до 15 часов |
| Идентификаторы | |
IUPAC имя
| |
| Номер CAS | |
| PubChem CID | |
| IUPHAR / BPS | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| ChEMBL |
|
| PDB лиганд | |
| CompTox Dashboard (EPA ) | |
| ECHA InfoCard | 100.125.601 |
| Химические и физические данные | |
| Формула | C19H25BN4O4 |
| Молярная масса | 384,24 г · моль |
| 3D-модель (JSmol ) | |
УЛЫБКИ
| |
InChI
| |
Бортезомиб, продаваемый, среди прочего, под торговой маркой Velcade, является анти- противораковое средство, используемое для лечения множественной миеломы и лимфомы из клеток мантии. Это включает множественную миелому у тех, кто ранее и не получал лечение. Обычно он используется вместе с другими лекарствами. Его вводят путем инъекции.
Общие побочные эффекты включают тошноту, диарею, усталость, низкий уровень тромбоцитов, лихорадку, онемение, низкий уровень лейкоцитов, одышку, сыпь и боли в животе. Другие серьезные побочные эффекты включают низкое кровяное давление, синдром лизиса опухоли, сердечную недостаточность и синдром обратимой задней лейкоэнцефалопатии. Он относится к классу лекарств, известных как ингибитор протеасомы. Он действует путем ингибирования протеасом, клеточных комплексов, расщепляющих белки.
Бортезомиб был одобрен для медицинского применения в США в 2003 году и в Европе в 2004 году. Он находится на Список основных лекарственных средств Всемирной организации здравоохранения.
Два открытых исследования установили эффективность бортезомиба ( с или без дексаметазона ) на 1, 4, 8 и 11 дни 21-дневного цикла в течение максимум восьми циклов у людей с рецидивирующей / рефрактерной множественной миеломой, предварительно получавших тяжелое лечение. Фаза III продемонстрировала превосходство бортезомиба над режимом приема высоких доз дексаметазона (например, медиана ТТП 6,2 против 3,5 месяца и 1-летняя выживаемость 80% против 66%). Новые исследования показывают, что бортезомиб может потенциально помочь в восстановлении после лечения винкристином при лечении острого лимфобластного лейкоза при замене винкристина в процессе.
Бортезомиб также оценивался вместе с другими препаратами для лечения множественных миелом у взрослых пациентов. Было замечено, что бортезомиб плюс леналидомид плюс дексаметазон, а также бортезомиб плюс мелфалан и преднизон могут привести к значительному увеличению прогрессирования -свободная выживаемость.
Желудочно-кишечные (ЖКТ) эффекты и астения являются наиболее частыми нежелательными явлениями. Бортезомиб связан с периферической невропатией у 30% пациентов, приводящей к боли. Это может быть хуже у пациентов с ранее существовавшей невропатией. Кроме того, миелосупрессия, вызывающая нейтропению и тромбоцитопению, также может иметь место и ограничивать дозу. Однако эти побочные эффекты обычно незначительны по сравнению с трансплантацией костного мозга и другими вариантами лечения пациентов с запущенным заболеванием. Бортезомиб часто вызывает опоясывающий лишай, хотя профилактическое ацикловир может снизить риск этого.
Побочные эффекты со стороны глаз, такие как халязион или гордеол (ячмень) могут чаще встречаться у женщин и приводить к прекращению лечения. Сообщалось также об остром интерстициальном нефрите.
Полифенолы, полученные из экстракта зеленого чая, включая эпигаллокатехин галлат (EGCG), которые, как ожидается, будут иметь синергетический эффект, вместо этого было обнаружено, что он снижает эффективность бортезомиба в экспериментах на культуре клеток.
 Бортезомиб связывается с коровой частицей в протеасоме дрожжей. Молекула бортезомиба находится в центре, окрашенном в зависимости от типа атома (бор = розовый, углерод = голубой, азот = синий, кислород = красный), и окружена локальной поверхностью белка. Синий участок представляет собой каталитический остаток треонина, активность которого блокируется присутствием бортезомиба.
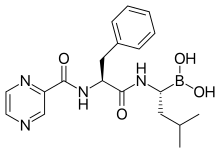
Бортезомиб связывается с коровой частицей в протеасоме дрожжей. Молекула бортезомиба находится в центре, окрашенном в зависимости от типа атома (бор = розовый, углерод = голубой, азот = синий, кислород = красный), и окружена локальной поверхностью белка. Синий участок представляет собой каталитический остаток треонина, активность которого блокируется присутствием бортезомиба. Лекарственное средство представляет собой N-защищенный дипептид и может быть записывается как Pyz-Phe-boroLeu, что означает пиразиновую кислоту, фенилаланин и лейцин с бороновой кислотой вместо карбоновая кислота.
Атом бора в бортезомибе связывает каталитический сайт 26S протеасомы с высоким сродством и специфичностью. В нормальных клетках протеасома регулирует экспрессию и функцию белков за счет деградации убиквитилированных белков, а также избавляет клетку от аномальных или неправильно свернутых белков. Клинические и доклинические данные подтверждают роль протеасомы в поддержании бессмертного фенотипа миеломных клеток, а данные культивирования клеток и ксенотрансплантатов подтверждают аналогичную функцию при раке солидных опухолей. Хотя, вероятно, задействованы несколько механизмов, ингибирование протеасом может предотвратить деградацию проапоптотических факторов, тем самым вызывая запрограммированную гибель клеток в неопластических клетках. Недавно было обнаружено, что бортезомиб вызывает быстрое и резкое изменение уровней внутриклеточных пептидов, продуцируемых протеасомой. Было показано, что некоторые внутриклеточные пептиды являются биологически активными, поэтому влияние бортезомиба на уровни внутриклеточных пептидов может вносить вклад в биологические и / или побочные эффекты препарата.
После подкожного введения пиковые уровни в плазме составляют ~ 25-50 нМ, и этот пик сохраняется в течение 1-2 часов. После внутривенной инъекции пиковые уровни в плазме составляют ~ 500 нМ, но только в течение ~ 5 минут, после чего уровни быстро падают по мере того, как лекарство распределяется по тканям (объем распределения составляет ~ 500 л). Оба пути обеспечивают равное воздействие лекарств и в целом сопоставимую терапевтическую эффективность. Период полувыведения составляет 9–15 часов, и препарат выводится в первую очередь за счет метаболизма в печени.
Фармакодинамика бортезомиба определяется путем количественной оценки ингибирования протеасом в мононуклеарных клетках периферической крови, взятых у пациентов, получавших препарат, средство, медикамент.
Бортезомиб был первоначально произведен в 1995 году на предприятии Myogenics. Препарат (PS-341) был протестирован в небольшом клиническом исследовании фазы I на пациентах с множественной миеломой. Millennium Pharmaceuticals представила его для дальнейших клинических испытаний в октябре 1999 года.
В мае 2003 года, через семь лет после первоначального синтеза, бортезомиб (продаваемый как Velcade компанией Millennium Pharmaceuticals Inc.) был одобрен. в США Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) США для использования при множественной миеломе на основании результатов исследования SUMMIT Phase II. В 2008 году бортезомиб был одобрен в США для начального лечения пациентов с множественной миеломой. Бортезомиб был ранее одобрен в 2005 году для лечения пациентов с множественной миеломой, которые ранее получали хотя бы одну терапию, и в 2003 году для лечения более устойчивой множественной миеломы.
Утверждение 2008 года было основано на международном, многоцентровое открытое исследование с активным контролем с участием ранее нелеченных пациентов с симптоматической множественной миеломой. Пациенты были рандомизированы для получения девяти циклов перорального приема мелфалана (М) и преднизона (П) или МП плюс бортезомиб. Пациенты получали М (9 мг / м2) плюс преднизон (60 мг / м2) ежедневно в течение четырех дней каждые 6 недель или по той же схеме МП с бортезомибом, 1,3 мг / м2 внутривенно в дни 1, 8, 11, 22, 25, 29. и 32 из каждого 6-недельного цикла для 4 циклов, затем один раз в неделю в течение 4 недель для 5 циклов. Время до прогрессирования (ВДП) было первичной конечной точкой эффективности. Общая выживаемость (OS), выживаемость без прогрессирования (PFS) и частота ответа (RR) были вторичными конечными точками. Подходящие пациенты были в возрасте>65 лет. Всего было рандомизировано 682 пациента: 338 получали МП и 344 получали комбинацию бортезомиб + МП. Демографические характеристики и исходные характеристики заболевания были схожими между двумя группами.
Исследование было остановлено после предварительно определенного промежуточного анализа, показавшего статистически значимое улучшение ВДП при добавлении бортезомиба к МП (в среднем 20,7 месяца) по сравнению с MP (медиана 15 месяцев) [ОР: 0,54 (95% ДИ: 0,42, 0,70), p = 0,000002]. ОВ, ВБП и ОР также значительно превосходили комбинацию бортезомиб-МП.
В августе 2014 года бортезомиб был одобрен в США для повторного лечения взрослых пациентов с множественной миеломой, которые ранее ответили на терапию Велкейдом. и рецидив произошел по крайней мере через шесть месяцев после завершения предыдущего лечения.
В октябре 2014 года бортезомиб был одобрен в США для лечения пациентов с лимфомой из клеток мантии (MCL), не получавшей лечения..
В Великобритании NICE первоначально рекомендовал против Velcade в октябре 2006 года из-за его стоимости около 18 000 фунтов стерлингов на человека, а также из-за того, что исследования, рассмотренные NICE, сообщили что он может увеличить продолжительность жизни в среднем только на шесть месяцев по сравнению со стандартным лечением. Однако позже компания предложила снижение затрат, связанное с производительностью, при множественной миеломе, и это было принято.