 | |
| Имена | |
|---|---|
| Название IUPAC Хлорид бериллия | |
| Идентификаторы | |
| CAS Номер | |
| 3D-модель (JSmol ) |
|
| ChemSpider | |
| ECHA InfoCard | 100.029.197 |
| PubChem CID | |
| номер RTECS |
|
| Панель управления CompTox (EPA ) | |
InChI
| |
SMILES
| |
| Свойства | |
| Химическая формула | BeCl 2 |
| Молярная масса | 79,9182 г / моль |
| Внешний вид | Белые или желтые кристаллы |
| Плотность | 1,899 г / см, твердое вещество |
| Температура плавления | 399 ° C (750 ° F; 672 K) |
| Температура кипения | 482 ° C (900 ° F; 755 K) |
| Растворимость в воде | 15,1 г / 100 мл (20 ° C) |
| Растворимость | растворим в спирт, эфир, бензол и пиридин. малорастворимые в хлороформе и сере диоксид |
| Структура | |
| Кристаллическая структура | гексагональная |
| Молекулярная форма | полимер |
| Термохимия | |
| Теплоемкость (C) | 7,808 Дж / К или 71,1 Дж / моль K |
| Стандартная молярная. энтропия (S 298) | 63 Дж / моль K |
| Стандартная энтальпия образования. (ΔfH298) | -6,136 кДж / г или -494 кДж / моль |
| свободная энергия Гиббса (ΔfG˚) | -468 кДж / моль |
| Стандартная энтальпия. сгорания (ΔcH298) | 16 кДж / моль |
| Опасности | |
| Смертельная доза или концентрация (LD, LC): | |
| LD50(средняя доза ) | 86 мг / кг (крыса, перорально) |
| NIOSH (пределы воздействия на здоровье в США): | |
| PEL (допустимо) | TWA 0,002 мг / м. C 0,005 мг / м (30 минут), с максимальным пиком 0,025 мг / м (как Be) |
| REL (рекомендуется) | Ca C 0,0005 мг / м (в виде Be) |
| IDLH (Непосредственная опасность) | Ca [4 мг / м (как Be)] |
| Родственные соединения | |
| Другие анионы | Фторид бериллия. Бромид бериллия. Йодид бериллия |
| Прочие катионы | Хлорид магния. Хлорид кальция. Хлорид стронция. Хлорид бария. Хлорид радия |
| Если не указано иное, данные приведены для материалов в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки ink | |
хлорид бериллия неорганическое соединение с формулой BeCl 2. Это бесцветное гигроскопичное твердое вещество, которое хорошо растворяется во многих полярных растворителях. Его свойства аналогичны свойствам хлорида алюминия из-за диагонального соотношения бериллия с алюминием.
Хлорид бериллия получают реакцией металла с хлором при высоких температурах:
BeCl 2 можно также получить карботермическим восстановлением оксида бериллия в присутствии хлора.. BeCl 2 может быть получен обработкой бериллия хлористым водородом.
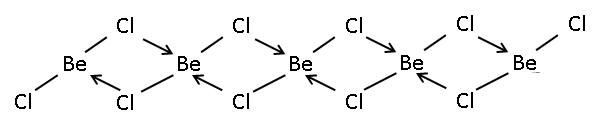
. Твердое вещество представляет собой 1-размерный полимер, состоящий из из общих ребер тетраэдров. Напротив, BeF 2 представляет собой 3-мерный полимер со структурой, аналогичной структуре кварца. В газовой фазе BeCl 2 существует как в виде линейного мономера, так и в виде мостикового димера с двумя мостиковыми атомами хлора, где атом бериллия это 3-х координатный. Линейная форма мономерной формы соответствует теории VSEPR. Линейная форма контрастирует с мономерными формами некоторых из дигалогенидов более тяжелых членов группы 2, например CaF 2, SrF 2, BaF 2, SrCl 2, BaCl 2, BaBr 2 и BaI 2, которые все нелинейны.
Хлорид бериллия устойчив в сухом воздухе. Хлорид бериллия является кислотой Льюиса и использовался в качестве катализатора в некоторых органических реакциях. Он гидролизует, выделяя хлористый водород :
Он образует тетрагидрат, BeCl 2 • 4H 2 O ([Be (H 2O)4] Cl 2 BeCl 2 также растворим в кислородсодержащих растворителях, таких как простые эфиры.
Хлорид бериллия используется в качестве сырья для электролиза бериллия и в качестве катализатора для реакций Фриделя-Крафтса.