 | |
 | |
| Имена | |
|---|---|
| Предпочтительно Название ИЮПАК Окись бериллия (II) | |
| Систематическое название ИЮПАК Оксобериллий | |
| Другие названия Бериллия, Термалокс, Бромеллит, Термалокс 995. | |
| Идентификаторы | |
| Номер CAS | |
| 3D-модель (JSmol ) | |
| Ссылка Бейльштейна | 3902801 |
| ChEBI | |
| ChemSpider | |
| ECHA InfoCard | 100.013.758 |
| Номер EC |
|
| MeSH | бериллий + оксид |
| PubChem CID | |
| Номер RTECS |
|
| UNII | |
| Номер ООН | 1566 |
| CompTox Dashboard (EPA ) | |
InChI
| |
УЛЫБКА
| |
| Свойства | |
| Химические формула | BeO |
| Молярная масса | 25,011 г · моль |
| Внешний вид | Бесцветные стекловидные кристаллы |
| Запах | Без запаха |
| Плотность | 3,01 г / см |
| Точка плавления | 2507 ° C (4545 ° F; 2780 K) |
| Температура кипения | 3900 ° C (7050 ° F; 4170 K) |
| Растворимость в воде | 0,00002 г / 100 мл |
| Ширина запрещенной зоны | 10,6 эВ |
| Термический проводимость | 330 Вт / (К · м) |
| Показатель преломления (nD) | 1,719 |
| Структура | |
| Кристаллическая структура | Гексагональная |
| Пространственная группа | P63mc |
| Точечная группа | C6v |
| Координационная геометрия | Тетрагональная |
| Молекулярная форма | Линейная |
| Термохимия | |
| Теплоемкость (C) | 25,5 Дж / (К · моль) |
| Стандартный молярный. энтропия (S 298) | 13,73–13,81 Дж / (К · моль) |
| Стандартная энтальпия образования. (ΔfH298) | −599 кДж / моль |
| Без Гиббса энергия (ΔfG˚) | -582 кДж / моль |
| Опасности | |
| Основные опасности | Очень токсичный, канцероген |
| Паспорт безопасности | См.: страница данных |
| Пиктограммы GHS |    |
| Сигнальное слово GHS | Опасно |
| Краткая характеристика опасности GHS | H301, H315, H317, H319, H330, H335, H350, H372 |
| Меры предосторожности GHS | P201, P260, P280, P284, P301 + 310, P305 + 351 + 338 |
| NFPA 704 (огненный алмаз) |  0 4 0 0 4 0 |
| Смертельная доза или концентрация (LD, LC): | |
| LD50(средняя доза ) | 2062 мг / кг (мышь, перорально) |
| NIOSH (пределы воздействия на здоровье США): | |
| PEL (допустимое) | TWA 0,002 мг / м. C 0,005 мг / м (30 минут), с максимальным пиком 0,025 мг / м (в виде Be) |
| REL (рекомендуется) | Ca C 0,0005 мг / м (как Be) |
| IDLH (Непосредственная опасность) | Ca [4 мг / м (как Be)] |
| Родственные соединения | |
| Другие анионы | Теллурид бериллия |
| Прочие катионы | |
| Страница дополнительных данных | |
| Структура и. свойства | Показатель преломления (n),. Диэлектрическая проницаемость (εr) и т. Д. |
| Термодинамические. данные | Фазовое поведение. твердое тело – жидкость – газ |
| Спектральные данные | UV, IR, ЯМР, MS |
| Если не указано иное, данные являются дано для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на информационные панели | |
Быть Оксид риллия (BeO ), также известный как бериллия, представляет собой неорганическое соединение с формулой BeO. Это бесцветное твердое вещество является заметным электрическим изолятором с более высокой теплопроводностью, чем любой другой неметалл, за исключением алмаза, и превосходит большинство металлов. В качестве аморфного твердого вещества оксид бериллия имеет белый цвет. Его высокой температурой плавления, приводит к его использованию в качестве огнеупорной материала. В природе встречается как минерал бромеллит. Исторически и в материаловедении оксид бериллия назывался глюцином или оксидом глюциния.
Оксид бериллия может быть получен путем прокаливания (обжига) карбоната бериллия, дегидратации гидроксида бериллия или зажигания металлического бериллия :
Воспламенение бериллия в воздухе дает смесь BeO и нитрида Be3N2. В отличие от оксидов, образованных другими элементами группы 2 (щелочноземельные металлы), оксид бериллия является амфотерным, а не основным.
Оксид бериллия, образующийся при высоких температурах (>800 ° C), инертен, но легко растворяется в горячем водном бифториде аммония (NH 4HF2) или растворе горячего концентрированного серная кислота (H2SO4) и сульфат аммония ((NH 4)2SO4).
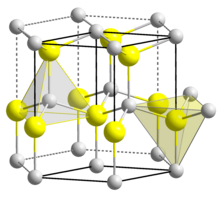
BeO кристаллизуется в гексагональной структуре вюрцита, с тетраэдрическими центрами Be и O, такими как лонсдейлит и w- BN (оба из которых являются изоэлектронными ). Напротив, оксиды большей группы -2 металла, т.е. MgO, CaO, SrO, BaO, кристаллизуются в кубической каменной соли мотив с октаэдрической геометрией вокруг дикатионов и дианионов. При высокой температуре структура трансформируется в тетрагональную форму.
В паровой фазе оксид бериллия присутствует в виде дискретных двухатомных молекул. в теории валентных связей, эти молекулы могут быть описаны как применяющие sp-орбитальную гибридизацию на обоих атомах, fea с учетом одной σ (между одной sp-орбиталью на каждом атоме) и одной π-связи (между выровненными p-орбиталями на каждом атоме, ориентированными перпендикулярно оси молекулы). Теория молекулярных орбиталей дает несколько иную картину без чистой сигма-связи (поскольку 2s-орбитали двух атомов объединяются, образуя заполненную сигма-связывающую орбиталь и заполненную сигма * орбиталь, препятствующую связыванию) и двух пи-связей, образованных между обеими парами p орбитали, ориентированные перпендикулярно оси молекулы. Сигма-орбиталь, образованная p-орбиталями, выровненными вдоль оси молекулы, незаполнена. Соответствующее основное состояние - это... (2sσ) (2sσ *) (2pπ) (как в изоэлектронной молекуле C 2), где обе связи можно рассматривать как дативные связи от кислорода к бериллию.
Высококачественные кристаллы могут быть выращены гидротермально или иным образом с помощью метода Вернейля. По большей части оксид бериллия производится в виде белого аморфного порошка , спеченного в более крупные формы. Примеси, такие как углерод, могут придавать различные цвета бесцветным кристаллам-хозяевам.
Спеченный оксид бериллия представляет собой очень стабильную керамику. Оксид бериллия используется в ракетных двигателях и в качестве прозрачного защитного покрытия на алюминизированных зеркалах телескопов.
Оксид бериллия используется во многих высокоэффективных полупроводниках. детали для таких приложений, как радиооборудование, потому что они имеют хорошую теплопроводность, а также являются хорошим электрическим изолятором. Он используется в качестве наполнителя в некоторых материалах с термоинтерфейсом, таких как термопаста. В некоторых силовых полупроводниковых устройствах между кристаллом кремния и металлическим монтажным основанием корпуса использовалась керамика на основе оксида бериллия для достижения более низкого значения теплового сопротивления, чем у аналогичных конструкция из оксида алюминия. Он также используется в качестве структурной керамики для высокопроизводительных микроволновых устройств, электронных ламп, магнетронов и газовых лазеров. ВеО был предложен в качестве замедлителя нейтронов для морских высокотемпературных реакторов с газовым охлаждением (MGCR), а также ядерных реакторов NASA Kilopower для космических приложений.
BeO является канцерогенным в порошкообразной форме и может вызывать хроническое заболевание легких аллергического типа бериллиоз. После обжига в твердую форму с ним безопасно обращаться, если он не подвергается механической обработке, в результате которой образуется пыль, чистая поломка выделяет немного пыли, но дробление или измельчение могут представлять опасность. Керамика на основе оксида бериллия не является опасными отходами в соответствии с федеральным законодательством США.