Элиас Джеймс "EJ" Кори (родился 12 июля 1928 г.) - американский химик-органик. В 1990 году он получил Нобелевскую премию по химии «за разработку теории и методологии органического синтеза », в частности ретросинтетического анализа. Многие считают его одним из величайших современных химиков, он разработал множество синтетических реагентов, методологий и тотальных синтезов, а также значительно продвинул науку об органическом синтезе.
EJ Кори (фамилия была англизирована от ливанского арабского Хури, что означает священник) родился в христианских ливанских иммигрантах в Метуэне, Массачусетс, 50 км (31 миль) к северу от Бостона. Его мать изменила его имя на «Элиас» в честь отца, который умер через восемнадцать месяцев после рождения Кори. Его овдовевшая мать, брат, две сестры, тетя и дядя жили вместе в просторном доме, борясь с Великой депрессией. В детстве Кори был независимым и увлекался такими видами спорта, как бейсбол, футбол и пешие прогулки. Он посещал католическую начальную школу и среднюю школу Лоуренса в Лоуренс, Массачусетс.
В возрасте 16 лет Кори поступил в Массачусетский технологический институт, где получил степень бакалавра степень в 1948 году и доктор философии под руководством профессора Джона С. Шихана в 1951 году. После поступления в Массачусетский технологический институт, Кори получил научный опыт только в области математики, и он начал свою карьера в колледже со степенью инженера. После первого урока химии на втором курсе он начал переосмысливать свои долгосрочные карьерные планы и окончил университет со степенью бакалавра химии. Сразу после этого, по приглашению профессора Джона С. Шихана, Кори остался в Массачусетском технологическом институте, чтобы защитить докторскую диссертацию. После его аспирантуры ему предложили назначение в Иллинойсский университет в Урбане-Шампейн, где он стал профессором химии в 1956 году в возрасте 27 лет. Он был инициирован как член Зетов. главу Alpha Chi Sigma в Университете Иллинойса в 1952 году. В 1959 году он перешел в Гарвардский университет, где в настоящее время является почетным профессором органической химии с активным исследованием группы Кори. программа. Он решил работать в области органической химии из-за «присущей ей красоты и большого значения для здоровья человека». Он также был советником Pfizer более 50 лет.
Среди множества наград Кори был удостоен Национальной медали науки в 1988 году, Нобелевской премии по химии в 1990 г. и высшей наградой Американского химического общества, медалью Пристли в 2004 г.
EJ Кори разработал несколько новых синтетических реагентов:

Одно из этих преимуществ состоит в том, что соединение доступно в виде стабильного на воздухе твердого вещества желтого цвета, которое не очень гигроскопично. В отличие от других окислителей, PCC может выполнять однократное окисление всего лишь с 1,5 эквивалентами (схема 1). Спирт выполняет нуклеофильную атаку на электроположительный металл хром (VI), вытесняя хлор. Затем хлорид анион действует как основание, давая альдегидный продукт и хром (IV). Слабокислый характер PCC делает его полезным для реакций циклизации со спиртами и алкенами (Схема 2).
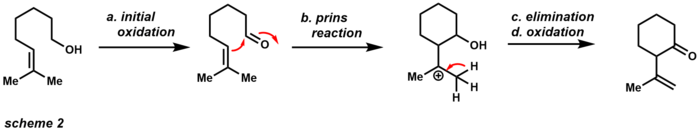
Начальное окисление дает соответствующий альдегид, который затем может подвергаться реакции Принса с соседним алкеном. После удаления и дальнейшего окисления продукт представляет собой циклический кетон. Если этот продукт нежелателен, порошкообразный ацетат натрия можно использовать в качестве буфера для достижения только начального окисления. Устойчивость PCC как окислителя также сделала его полезным в области полного синтеза (схема 3). Этот пример иллюстрирует, что PCC способен выполнять окислительную перегруппировку Даубена с третичными спиртами посредством [3,3] -сигматропной перегруппировки.
![[3,3] перегруппировать Ent с PCC](http://upload.wikimedia.org/wikipedia/commons/thumb/8/87/PCC_rearrangement3.png/700px-PCC_rearrangement3.png)
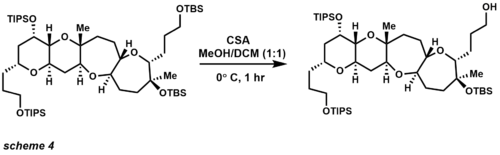
В области синтеза сложных молекул TBS широко используется как один из наиболее универсальных кремнийорганических соединений. на основе защитных групп (схема 4). Использование CSA обеспечивает селективное удаление первичного эфира TBS в присутствии третичного эфира TBS и простых эфиров TIPS. Другие способы снятия защиты TBS включают кислоты (также кислоты Льюиса) и фториды. Защитные группы TIPS также были изобретены Кори и обеспечивают повышенную селективность защиты первичного спирта по сравнению с защитой вторичного и третичного спирта. Простые эфиры TIPS более стабильны в кислых и основных условиях, недостатком этой защитной группы по сравнению с простыми эфирами TBS является то, что эта группа менее лабильна для снятия защиты. Наиболее распространенные реагенты, используемые для расщепления, используют те же условия, что и эфир TBS, но обычно требуется более длительное время реакции.

Обычно простые эфиры TBS разделяются TBAF, но затрудненный эфир TBS, указанный выше, выживает в условиях реакции после удаления первичного TIPS (схема 5). Защитная группа MEM была впервые описана Кори в 1976 году. Эта защитная группа аналогична по реакционной способности и стабильности другим алкоксиметиловым эфирам в кислых условиях. Расщепление защитных групп MEM обычно осуществляется в кислых условиях, но координация с галогенидами металлов значительно увеличивает лабильность за счет вспомогательного расщепления (схема 6).


pKa дитианов составляет примерно 30, что позволяет депротонировать с помощью алкиллитиевого реагента, обычно н-бутиллития. Реакция с дитианами и альдегидами теперь известна как реакция Кори-Зеебаха. Депротонированный дитиан служит ацил-анионом, используемым для атаки входящих электрофилов. После снятия защиты с дитиана, обычно с помощью HgO, наблюдается образование кетонового продукта из замаскированного ацилдитиан-аниона. Использование таких реакций расширило область органического синтеза, позволив химикам-синтетикам использовать разобщения Umpolung в полном синтезе (схема 8). 1,3-дитианы также используются в качестве защитных групп для карбонильных соединений, выражая универсальность и полезность этой функциональной группы.

Несколько реакций, разработанных в лаборатории Кори, стали обычным явлением в современной синтетической органической химии. С 1950 года в группе Кори было разработано не менее 302 метода. Несколько реакций были названы в его честь:

Позже Кори продемонстрировал, что замещенные бораны легче приготовить и намного стабильнее. Механизм восстановления начинается с того, что оксазоборолидин является лишь слегка основным по [азоту], координируясь со стехиометрическим бораном бор-аминного комплекса (схема 10). Отсутствие донорства азота в бор увеличивает его кислотность по Льюису, обеспечивая координацию с кетоновым субстратом. Комплексообразование субстрата происходит из наиболее доступной неподеленной пары кислорода, что приводит к ограниченному вращению вокруг связи BO из-за стерически соседней фенильной группы.
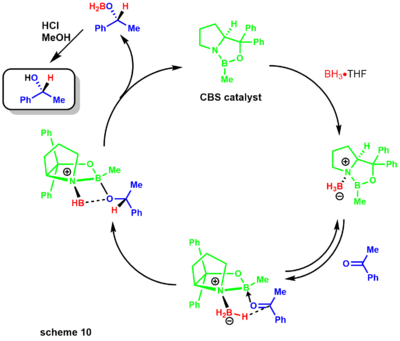
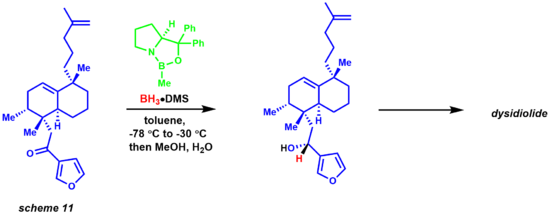
Миграция гидрида из борана в электрофильный кетон центр возникает через переходное состояние 6-членного кольца, что приводит к промежуточному образованию четырехчленного кольца, в конечном итоге обеспечивающему хиральный продукт и регенерацию катализатора. Реакция также оказалась очень полезной для химиков, занимающихся натуральными продуктами (схема 11). Синтез дисидиолида Кори и соавторами был достигнут посредством энантиоселективного восстановления CBS с использованием комплекса боран-диметилсульфид.

При обработке двумя эквивалентами n-buLi галогеновый обмен лития и депротонирование дает соединение ацетилида лития, которое подвергается гидролизу с образованием концевого алкинового продукта (схема 12). Совсем недавно был разработан однореакторный синтез с использованием модифицированной процедуры. Это синтетическое преобразование было доказано успешным в полном синтезе (+) - тейлориона У. Дж. Керром и сотрудниками (схема 13).


Соль алкоксисульфония депротонируется в альфа-положении с триэтиламином с получением окисленного продукта. Реакция включает широкий спектр функциональных групп, но аллильные и бензильные спирты обычно превращаются в аллильные и бензильные хлориды. Его применение в синтезе основано на мягких условиях протокола и совместимости функциональных и защитных групп. В полном синтезе ингенола Куваджима и его сотрудники использовали окисление Кори-Кима путем селективного окисления менее затрудненного вторичного спирта (схема 15).


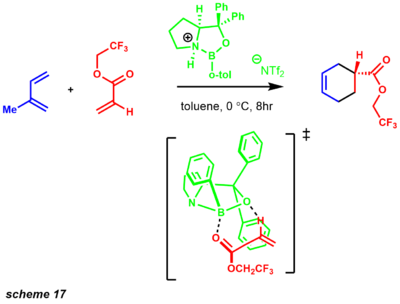
Это переходное состояние, вероятно, происходит из-за благоприятного пи-стэкинга с фенильным заместителем. Энантиоселективности процесса способствует приближение диена к диенофилу с противоположной стороны фенильного заместителя. Реакция Дильса-Альдера - одно из самых мощных преобразований в синтетической химии. Синтез природных продуктов с использованием реакции Дильса-Альдера в качестве преобразования был применен, в частности, к образованию шестичленных колец (схема 18).

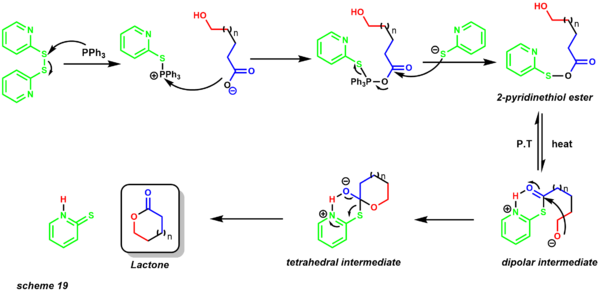
Реакция протекает в присутствии 2,2'-дипиридилдисульфида и трифенилфосфина. Реакцию обычно кипятят с обратным холодильником в неполярном растворителе, таком как бензол. Механизм начинается с образования эфира 2-пиридинтиола (схема 19). Перенос протона обеспечивает диполярный промежуточный продукт, в котором алкоксид нуклеофил атакует электрофильный карбонильный центр, обеспечивая тетраэдрический промежуточный продукт, который дает макролактоновый продукт. Один из первых примеров этого протокола был применен к общему синтезу зеараленона (схема 20).

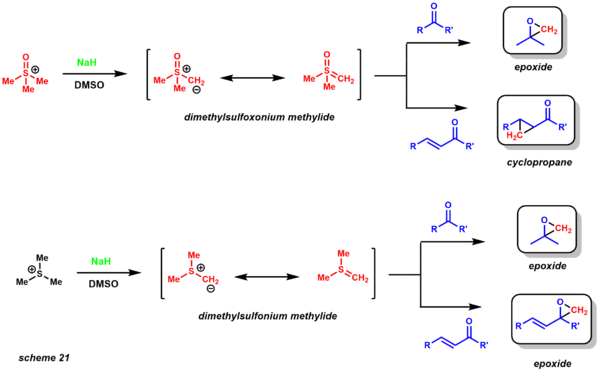
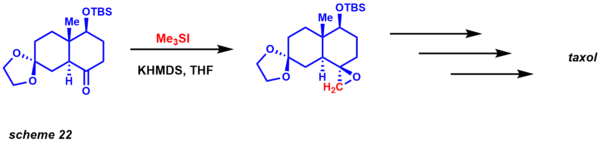
Основываясь на их реакционной способности, еще одним явным преимуществом этих двух вариантов является то, что кинетически они обеспечивают разницу в диастереоселективности. Реакция очень хорошо изучена, также были получены энантиоселективные варианты (каталитические и стехиометрические). С точки зрения ретросинтетического анализа, эта реакция представляет собой разумную альтернативу обычным реакциям эпоксидирования алкенами (схема 22). Данишефский использовал эту методологию для синтеза таксола. Диастереоселективность устанавливается 1,3-взаимодействиями в переходном состоянии, необходимом для закрытия эпоксида.
E. Дж. Кори и его исследовательская группа выполнили много полных синтезов. С 1950 года в группе Кори было синтезировано по меньшей мере 265 соединений.
Его общий синтез нескольких простагландинов в 1969 году считается классикой. В частности, синтез простагландина F 2α представляет несколько проблем. Присутствие цис- и транс-олефинов, а также пяти асимметричных атомов углерода делает молекулу желаемой проблемой для химиков-органиков. Ретросинтетический анализ Кори выделяет несколько ключевых разрывов, которые приводят к упрощенным предшественникам (схема 23).

Молекулярное упрощение началось сначала с разъединения обеих углеродных цепей с помощью реакции Виттига и модификации Хорнера-Уодсворта-Эммонса. Реакция Виттига дает цис-продукт, в то время как реакция Хорнера-Уодсворта Эммонса дает транс-олефин. Опубликованный синтез показывает смесь диастереомеров 1: 1 восстановления карбонила с использованием боргидрида цинка. Однако спустя годы Кори и его сотрудники установили сокращение CBS. Одним из примеров, иллюстрирующих этот протокол, был промежуточный продукт в синтезе простагландина, показывающий смесь 9: 1 желаемого диастереомера (схема 24).
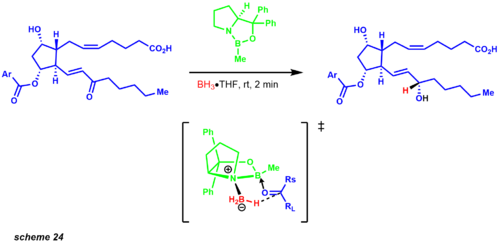
Трансформация йодолактонизации дает аллиловый спирт, ведущий к ключевому промежуточному продукту Байера-Виллигера. Это окисление региоселективно вставляет атом кислорода между кетоном и наиболее богатым электронами участком. Ключевой промежуточный продукт приводит к прямому преобразованию в структурную цель Дильса-Альдера, которая обеспечивает углеродный каркас для функционализированного циклопентанового кольца. Позже Кори разработал асимметричную реакцию Дильса-Альдера с использованием хирального оксазоборолидина, что значительно упростило путь синтеза простагландинов.
Другие известные синтезы:
EJ У Кори более 1100 публикаций. В 2002 году Американское химическое общество (ACS) признало его «Самым цитируемым автором по химии». В 2007 году он получил первую награду ACS Publications Division «Цикл передового опыта за высокоэффективный участник» и был признан химиком номер один с точки зрения результатов исследований по индексу Хирша (h-index ). Среди его книг:
Джейсон Алтом, один из учеников Кори, покончил жизнь самоубийством в 1998 году. Самоубийство Алтома вызвало споры, потому что он прямо обвинял Кори, своего научного консультанта, за его самоубийство. В своей прощальной записке в 1998 году Алтом назвал «оскорбительные научные руководители» одной из причин покушения на его жизнь. Предсмертная записка Алтома также содержала четкие инструкции о том, как изменить отношения между студентами и их руководителями.
В то время как Алтом был вторым самоубийцей за столько лет в лаборатории Кори, Кори был сбит с толку и сбит с толку смертью своего ученика. Кори сказал: «В этом письме нет смысла. В конце концов, Джейсон, должно быть, был в высшей степени бредовым или иррациональным». Кори также утверждал, что никогда не подвергал сомнению интеллектуальный вклад Алтома. «Я делал все возможное, чтобы направлять Джейсона, как горный гид, чтобы направлять кого-то, кто поднимается на гору. Я делал все возможное на каждом этапе пути», - говорит Кори. «Моя совесть чиста. Все, что сделал Джейсон, было результатом нашего сотрудничества. У нас никогда не было ни малейших разногласий». Американский фонд предотвращения самоубийств (AFSP) процитировал статью The New York Times о самоубийстве Альтома как пример проблемного освещения, утверждая, что у Альтома были предупреждающие признаки депрессии и суицидальных мыслей, и что в статье был назван козлом отпущения Кори, несмотря на отсутствие вторичных доказательств того, что поведение советника усугубило страдания Алтома. Согласно The Boston Globe, студенты и профессора заявили, что Альтом фактически сохранил поддержку Кори.
В результате смерти Альтома химический факультет принял предложение, позволяющее аспирантам запрашивать еще два преподавателей, которые будут играть небольшую консультативную роль при подготовке диссертации.
.
По состоянию на 2010 год членами Corey Group были около 700 человек. База данных о 580 бывших членах и их нынешних членах была разработана к 80-летию Кори в июле 2008 года.
Когда в 2004 году была присуждена медаль Пристли, Э.Дж. Кори вызвал споры. с его заявлением о том, что он вдохновил Роберта Бернса Вудворда до разработки правил Вудворда – Хоффмана. Кори писал:
«4 мая 1964 года я предложил своему коллеге Р. Б. Вудворду простое объяснение, включающее симметрию возмущенных (ВЗМО) молекулярных орбиталей для стереоселективного циклобутена → 1,3-бутадиена и 1, Превращения 3,5-гексатриен → циклогексадиен, которые послужили основой для дальнейшего развития этих идей в то, что стало известно как правила Вудворда-Хоффмана ».
Это было первое публичное заявление Кори по поводу его утверждения, что начиная с мая 5, 1964 Вудворд выдвинул объяснение Кори как свою собственную мысль без упоминания Кори и разговора 4 мая. Кори обсуждал свое утверждение в частном порядке с Хоффманном и близкими коллегами с 1964 года. Кори упоминает, что он сделал заявление Пристли, «так что историческое запись будет правильной ".
Заявление и вклад Кори были публично опровергнуты Роальдом Хоффманном в журнале Angewandte Chemie. В опровержении Хоффманн заявляет, что в ходе долгого обсуждения этого вопроса он спросил Кори, почему Кори не обнародовал этот вопрос. Кори ответил, что, по его мнению, такое публичное разногласие нанесет вред Гарварду и что он «не станет« делать что-либо против Гарварда, которому я был и так предан ». Кори также надеялся, что сам Вудворд исправит исторические записи, «когда станет старше, более внимательным и более чувствительным к собственной совести». Вудворд внезапно умер во сне от сердечного приступа в 1979 году.
Э.Дж. Кори получил более 40 крупных наград, включая Премию Линуса Полинга (1973), Медаль Франклина (1978), Приз Тетраэдра (1983), Премия Вольфа по химии (1986), Национальная медаль науки (1988), Премия Японии (1989), Нобелевская премия по химии (1990), Золотая пластина Американской академии достижений (1991), премия Роджера Адамса (1993) и медаль Пристли (2004). Он был введен в Зал славы Alpha Chi Sigma в 1998 году. По состоянию на 2008 год он получил 19 почетных степеней университетов по всему миру, включая Оксфордский университет (Великобритания), Кембриджский университет (Великобритания) и Национальный университет Чунг Ченг. В 2013 году журнал E.J. Институт биомедицинских исследований Кори (CIBR) открыт в Цзянъине, провинция Цзянсу, Китай.
Кори был избран иностранным членом Королевского общества (ForMemRS) в 1998 году.
| Викискладе есть медиафайлы, связанные с EJ Кори. |
| В Викицитатнике есть цитаты, связанные с: Элиасом Джеймсом Кори |