 | |
 | |
| Имена | |
|---|---|
| Название IUPAC Медь (II) гидроксид | |
| Другие названия Гидроксид меди | |
| Идентификаторы | |
| Номер CAS | |
| 3D-модель (JSmol ) | |
| ChemSpider | |
| ECHA InfoCard | 100.039.817 |
| KEGG | |
| PubChem CID | |
| UNII | |
| CompTox Dashboard (EPA ) | |
InChI
| |
УЛЫБКА
| |
| Свойства | |
| Химическая формула | Cu (OH) 2 |
| Молярная масса | 97,561 г / моль |
| Внешний вид | Синее или сине-зеленое твердое вещество |
| Плотность | 3,368 г / см, твердое вещество |
| Температура плавления | 80 ° C (176 ° F; 353 K) (разлагается на CuO ) |
| Растворимость в вода | незначительно |
| произведение растворимости (Ksp) | 2,20 x 10 |
| Solubi лити | не растворим в этаноле ;. растворим в NH4OH |
| Магнитная восприимчивость (χ) | + 1170,0 · 10 см / моль |
| Термохимия | |
| Стандартная молярная. энтропия (S 298) | 108 Дж · моль · K |
| Стандартная энтальпия образования. (ΔfH298) | −450 кДж · моль |
| Опасности | |
| Основные опасности | Кожа, глаза и дыхательные пути Раздражающий |
| Паспорт безопасности | http://www.sciencelab.com/xMSDS-Cupric_Hydroxide-9923594 |
| NFPA 704 (огненный алмаз) |  0 2 0 0 2 0 |
| Температура вспышки | Не- легковоспламеняющийся |
| Смертельная доза или концентрация (LD, LC): | |
| LD50(средняя доза ) | 1000 мг / кг (перорально, крыса) |
| NIOSH (пределы воздействия на здоровье в США): | |
| PEL (Допустимо) | TWA 1 мг / м (для Cu) |
| REL (Рекомендуется) | TWA 1 мг / м (для Cu) |
| IDLH ( Непосредственная опасность) | TWA 100 мг / м (в виде Cu) |
| Родственные соединения | |
| Другие анионы | Оксид меди (II). Карбонат меди (II). Медь (II) сульфат. хлорид меди (II) |
| Другие катионы | гидроксид никеля (II). гидроксид цинка. гидроксид железа (II). гидроксид кобальта |
| родственные соединения | С Оксид оппера (I). Хлорид меди (I) |
| Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки в информационном окне | |
Гидроксид меди (II) - это гидроксид из меди с химическая формула Cu (OH) 2. Это бледно-зеленовато-синее или голубовато-зеленое твердое вещество. Некоторые формы гидроксида меди (II) продаются как «стабилизированный» гидроксид меди (II), хотя они, вероятно, состоят из смеси карбоната меди (II) и гидроксида. Гидроксид меди - слабое основание.
Гидроксид меди (II) известен с тех пор, как плавление меди началось около 5000 г. до н.э., хотя алхимики, вероятно, были первыми, кто изготовил его, смешав растворы щелока (гидроксид натрия или калия) и медного купороса (сульфата меди (II)). Источники обоих соединений были доступны еще в древности.
Он производился в промышленных масштабах в 17-18 веках для использования в пигментах, таких как синий вердитер и бременский зеленый. Эти пигменты использовались в керамике и окраске.
Гидроксид меди (II) может быть получен добавлением гидроксида натрия к разбавленному раствору. раствор сульфата меди (II) (CuSO 4 · 5H 2 O). Однако полученный таким образом осадок часто содержит воду и заметное количество примеси гидроксида натрия. Более чистый продукт может быть получен, если к раствору заранее добавить хлорид аммония. В качестве альтернативы гидроксид меди легко получить электролизом воды (содержащей небольшое количество электролита, такого как сульфат натрия или сульфат магния ) с медь анод.
Минерал формулы Cu (OH) 2 называется спертиниит. Гидроксид меди (II) редко встречается как несвязанный минерал, потому что он медленно реагирует с диоксидом углерода из атмосферы с образованием основного карбоната меди (II). Таким образом, медь медленно приобретает матово-зеленый налет во влажном воздухе по реакции:
Необработанный материал в принципе представляет собой мольную смесь 1: 1 Cu (OH) 2 и CuCO 3. Эта патина образует бронзу и другие статуи из медного сплава, такие как Статуя Свободы.
Структура Cu (OH) 2 определено с помощью рентгеновской кристаллографии. Медный центр имеет квадратно-пирамидальную форму. Четыре расстояния Cu-O в плоскости составляют 1,96 Å, а аксиальное расстояние Cu-O составляет 2,36 Å. Гидроксидные лиганды в плоскости являются либо дважды мостиковыми, либо тройными мостиковыми.
Он стабилен примерно до 100 ° C.
Медь ( II) гидроксид реагирует с раствором аммиака с образованием темно-синего раствора тетрамминмеди [Cu (NH 3)4]комплексный ион. Он катализирует окисление растворов аммиака в присутствие дикислорода, приводящего к образованию нитритов аммиака меди, таких как Cu (NO 2)2(NH 3)n.
Гидроксид меди (II) слабо амфотерный. Он слегка растворяется в концентрированной щелочи, образуя [Cu (OH) 4].
.
Гидроксид меди (II) играет довольно специализированную роль в органическом синтезе. Часто, когда он используется для этой цели, его получают in situ путем смешивания растворимой соли меди (II) и гидроксида калия.
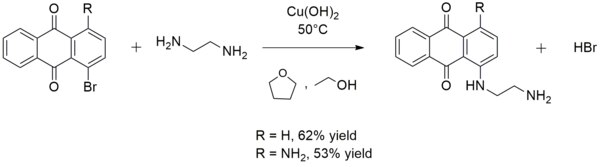
. Иногда его используют в синтезе арил аминов. Например, гидроксид меди (II) катализирует реакцию этилендиамина с 1-бромо антрахинон или 1-амино-4-бромантрахинон с образованием 1 - ((2-аминоэтил) амино) антрахинона или 1-амино-4 - ((2-аминоэтил) амино) антрахинона соответственно:
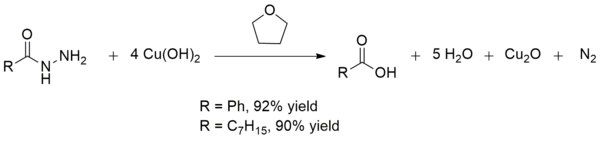
гидроксид меди (II) превращает кислоты гидразиды в карбоновые кислоты при комнатной температуре. Это превращение полезно при синтезе карбоновых кислот в присутствии других хрупких функциональных групп. Выходы обычно превосходны, как в случае с производством бензойной кислоты и октановой кислоты :
гидроксид меди (II) в растворе аммиака, известный как Реагент Швейцера обладает интересной способностью растворять целлюлозу. Это свойство привело к его использованию в производстве вискозы, целлюлозного волокна.
. Оно также широко используется в аквариумной промышленности благодаря своей способности уничтожать внешних паразитов у рыб, включая сосальщиков, морской их, ручей и морской бархат, не убивая рыбу. Хотя другие водорастворимые соединения меди могут быть эффективными в этой роли, они обычно приводят к высокой смертности рыб.
Гидроксид меди (II) использовали в качестве альтернативы бордоской смеси, фунгициду и нематициду. К таким продуктам относится Kocide 3000, производимый Kocide L.L.C. Гидроксид меди (II) также иногда используется в качестве керамического красителя..
Гидроксид меди (II) объединяют с латексной краской, создавая продукт, предназначенный для контроля роста корней у горшечных растений. Вторичные и боковые корни разрастаются и разрастаются, в результате чего корневая система становится плотной и здоровой. Он продавался под названием Spin Out, которое впервые было представлено Griffin L.L.C. Теперь права принадлежат SePRO Corp. Теперь он продается как Microkote либо в растворе, который вы применяете самостоятельно, либо в виде обработанных горшков.
 Химическая структура азурита, одного из многих гидроксидов меди (II) (цветовой код: красный = O, зеленый = Cu, серый = C, белый = H).
Химическая структура азурита, одного из многих гидроксидов меди (II) (цветовой код: красный = O, зеленый = Cu, серый = C, белый = H). Вместе с другими компонентами гидроксиды меди (II) многочисленны. Некоторые содержащие медь (II) минералы содержат гидроксид. Известные примеры включают азурит, малахит, антлерит и брошантит. Азурит (2CuCO 3 · Cu (OH) 2) и малахит (CuCO 3 · Cu (OH) 2) являются гидрокси- карбонаты, тогда как антлерит (CuSO 4 · 2Cu (OH) 2) и брошантит (CuSO 4 · 3Cu (OH) 2) представляют собой гидрокси- сульфаты.
Многие синтетические производные гидроксида меди (II) были исследованы.
| На Викискладе есть материалы, связанные с гидроксидом меди (II). |