| Атерома | |
|---|---|
| Другие названия | атеромата ( множественное число), атеромы (множественное число) |
 | |
| Атеросклеротическая бляшка из образца каротидной эндартерэктомии. Здесь показано разделение общей на внутреннюю и внешнюю сонную артерии. | |
| Speciality | Cardiology |
| Complications | Thrombosis, эмболия |
атерома или атероматозная бляшка («бляшка») - это аномальное скопление материала во внутреннем слое стенки артерия.
Материал состоит в основном из клеток макрофага или обломков, содержащих липиды, кальций и различное количество волокнистой соединительной ткани. Накопленный материал образует набухание в стенке артерии, которое может проникать в просвет артерии, сужая и ограничивая кровоток. Атерома является патологической основой заболевания атеросклероз, подтип артериосклероза.
У большинства людей первые симптомы возникают в результате прогрессирования атеромы в сердечных артериях, что чаще всего приводит к сердечный приступ и последующая слабость. Сердечные артерии трудно отследить, потому что (а) они маленькие (от 5 мм до микроскопических), (б) они спрятаны глубоко в грудной клетке и (в) они никогда не перестают двигаться. Кроме того, все массовые клинические стратегии сосредоточены как на (а) минимальной стоимости, так и (б) на общей безопасности процедуры. Таким образом, существующие диагностические стратегии для обнаружения атеромы и отслеживания реакции на лечение были чрезвычайно ограничены. Наиболее часто используемые методы - симптомы пациента и кардиологическое стресс-тестирование - не обнаруживают никаких симптомов проблемы до тех пор, пока атероматозное заболевание не станет очень распространенным, поскольку артерии увеличиваются, а не сужаются в ответ на увеличение атеромы. Это разрывы бляшек, образующие мусор и сгустки, которые препятствуют кровотоку ниже по течению, иногда также локально (как видно на ангиограммах ), которые уменьшают / останавливают кровоток. Однако эти события происходят внезапно и не обнаруживаются заранее ни стресс-тестированием, стресс-тестом, или ангиограммой.
Здоровая эпикардиальная коронарная артерия. состоит из трех слоев: tunica intima, media и adventitia. Атерома и изменения в стенке артерии обычно приводят к небольшим аневризмам (увеличению), достаточно большим, чтобы компенсировать дополнительную толщину стенки без изменения диаметра просвета. Однако в конечном итоге, как правило, в результате разрыва уязвимых бляшек и сгустков в просвете над бляшкой в некоторых областях развивается стеноз (сужение) сосуда. Реже артерия увеличивается настолько, что приводит к сильному аневризматическому увеличению артерии. Все три результата часто наблюдаются в разных местах у одного и того же человека.
Со временем атеромы обычно увеличиваются в размере и толщине и вызывают развитие окружающей мышечной центральной области ( media) артерии для растяжения, называемого ремоделированием, как правило, достаточно, чтобы компенсировать их размер, так что калибр отверстия артерии (просвет ) остается без изменений до тех пор, пока более 50% площади поперечного сечения стенки артерии не будет состоять из атероматозной ткани.
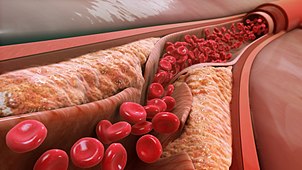 Суженный артериальный кровеносный сосуд, заблокированный антеромой.
Суженный артериальный кровеносный сосуд, заблокированный антеромой. Если увеличение мышечной стенки в конечном итоге не поспевает за увеличением атеромы объем, или сгусток образуется и организуется над бляшкой, тогда просвет артерии сужается в результате повторяющихся разрывов, сгустков и фиброза тканей, отделяющих атерому от кровотока. Это сужение становится все более распространенным после десятилетий жизни и становится все более частым после того, как людям от 30 до 40 лет.
эндотелий (клеточный монослой внутри сосуда) и покрывающая ткань, называемая фиброзный колпачок, отделяют атерому от крови в просвете. Если происходит разрыв (см. уязвимая бляшка ) эндотелия и фиброзного колпачка, то и (а) поток мусора из бляшки в сочетании с (б) реакцией тромбоцитов и свертывания крови (как на мусор, так и на фиброзный колпачок). в месте разрыва) происходит за доли секунды.
Разрыв приводит как к (а) ливню обломков, перекрывающих меньшие сосуды, расположенные ниже по потоку (обломки размером более 5 микрометров слишком велики для прохождения через капилляры) ) в сочетании с (b) накопление тромбоцитов и сгустка над разрывом (реакция на повреждение / восстановление), приводящее к сужению, а иногда и к закрытию просвета.
повреждение ткани ниже по потоку происходит из-за (а) закрытия нижестоящего микроваскуляра и / или (б) закрытие просвета в месте разрыва, что приводит к потере кровотока в нижерасположенную капиллярную микрососудистую сеть. Это основной механизм инфаркта миокарда, инсульта или других связанных сердечно-сосудистых заболеваний проблем.
Хотя сгустки в месте разрыва обычно со временем сжимаются в объеме, часть сгустка может организовываться в фиброзную ткань, что приводит к сужению артерии просвет ; сужения, иногда наблюдаемые при ангиографии, если они достаточно серьезны. Поскольку методы ангиографии могут выявить только большие просветы, обычно более 200 микрометров, ангиография после сердечно-сосудистого события обычно не показывает, что произошло.
Если увеличение мышечной стенки слишком велико с течением времени, то в результате происходит грубое увеличение артерии, обычно в течение десятилетий жизни. Это менее распространенный результат. Атерома в увеличении аневризмы (выпуклость сосуда) также может разорвать и спустить остатки атеромы и сгусток вниз по течению. Если увеличение артерии в 2–3 раза больше обычного диаметра, стенки часто становятся настолько слабыми, что даже при напряжении пульса может произойти нарушение целостности стенки, что приведет к внезапному кровоизлиянию (кровотечению), основные симптомы и слабость; часто быстрая смерть. Основным стимулом к образованию аневризмы является атрофия давлением структурной опоры мышечных слоев. Основными структурными белками являются коллаген и эластин. Это приводит к истончению и увеличению стенок пузырей, что является обычным явлением в брюшной области аорты.
Накопление (набухание) всегда происходит в оболочке интима, между выстилкой эндотелия и гладкомышечным средним слоем стенки артерии.
Хотя ранние стадии, основанные на внешнем виде, патологи традиционно называли жировыми полосами, они состоят не из жировых клеток, а из скоплений лейкоциты, особенно макрофаги, которые поглотили окисленный липопротеин низкой плотности (ЛПНП).
После того, как они накапливают большое количество цитоплазматических мембран (с соответствующим высоким содержанием холестерина), их называют пенистыми клетками. Когда пенистые клетки умирают, их содержимое высвобождается, что привлекает больше макрофагов и создает внеклеточное липидное ядро около центра к внутренней поверхности каждой атеросклеротической бляшки.
И наоборот, внешние, более старые части бляшки со временем становятся более кальцифицированными, менее метаболически активными и более физически жесткими.
В венах не развиваются атеромы, потому что они не подвергаются такому же воздействию. гемодинамическое давление, которое имеют артерии, если хирургическим путем не перемещать их для работы в качестве артерии, как при операции шунтирования.
 Иллюстрация сравнения нормального кровеносного сосуда и частично заблокированного сосуда из-за атеросклеротической бляшки. Обратите внимание на увеличение и отсутствие значительного сужения просвета.
Иллюстрация сравнения нормального кровеносного сосуда и частично заблокированного сосуда из-за атеросклеротической бляшки. Обратите внимание на увеличение и отсутствие значительного сужения просвета. Поскольку стенки артерий увеличиваются в местах с атеромой, обнаружение атеромы до смерти и вскрытия в лучшем случае долгое время было проблематичным. Большинство методов сосредоточено на открытии артерий; очень актуально, но совершенно не учитывает атерому в стенках артерии.
Исторически, фиксация артериальной стенки, окрашивание и шлифование были золотым стандартом для обнаружения и описания атеромы после смерти и вскрытия. При специальном окрашивании и исследовании микрокальцификаты могут быть обнаружены, как правило, в гладкомышечных клетках артериальной среды рядом с жировыми полосами в течение года или двух после образования жировых полос.
Интервенционные и неинтервенционные методы выявления атеросклероза, в частности уязвимой бляшки (неокклюзионной или мягкой бляшки), сегодня широко используются в исследованиях и клинической практике.
Каротид Толщина интима-медиа Сканирование (CIMT может быть измерено с помощью УЗИ в B-режиме) было рекомендовано Американской кардиологической ассоциацией как наиболее полезный метод для выявлять атеросклероз и теперь вполне может быть золотым стандартом для обнаружения.
ВСУЗИ - самый чувствительный в настоящее время метод обнаружения и измерения более прогрессивной атеромы у живых людей, хотя он обычно не используется до тех пор, пока атерома не начнет формироваться из-за к стоимости и инвазивности организма.
КТ с использованием современной спирали с более высоким разрешением или аппараты с более высокой скоростью EBT были наиболее эффективным методом обнаружения кальциноза, присутствующего в зубном налете. Однако атерома должна быть достаточно развитой, чтобы иметь внутри себя относительно большие области кальцификации, чтобы создать достаточно большие области размером ~ 130 единиц Хаунсфилда, которые программное обеспечение компьютерного томографа может распознать в отличие от других окружающих тканей. Обычно такие области начинают возникать в сердечных артериях примерно через 2–3 десятилетия после начала развития атеромы. Наличие более мелких пятнистых бляшек может быть более опасным для прогрессирования острого инфаркта миокарда.
УЗИ артерий, особенно сонных артерий, с измерением толщины стенки артерии. способ частично отследить прогрессирование болезни. По состоянию на 2006 год толщина, обычно называемая IMT для интимы-медиальной толщины, не измеряется клинически, хотя некоторые исследователи использовали ее с середины 1990-х годов для отслеживания изменений в стенках артерий. Традиционно клиническое ультразвуковое исследование сонных артерий оценивает только степень ограничения просвета крови, стеноз, как результат очень запущенного заболевания. Национальный институт здравоохранения провел пятилетнее исследование стоимостью 5 миллионов долларов, возглавляемое медицинским исследователем Кеннетом Уриэлем, для изучения внутрисосудистых ультразвуковых методов в отношении атеросклеротических бляшек. Более прогрессивные клиницисты начали использовать измерение ТИМ как способ количественной оценки и отслеживания прогрессирования или стабильности заболевания у отдельных пациентов.
Ангиография с 1960-х годов была традиционным способом оценки атеромы. Однако ангиография - это только движущиеся или неподвижные изображения красителя, смешанного с кровью, с артериальным просветом и никогда не выявляют атеромы; стенки артерий, в том числе атеромы с артериальной стенкой, остаются незаметными. Ограниченное исключение из этого правила состоит в том, что при очень развитой атероме с обширной кальцификацией внутри стены у большинства пожилых людей можно увидеть галообразное кольцо радиоплотности, особенно когда артериальные просветы визуализируются в конце. На cine-floro кардиологи и радиологи обычно ищут эти тени кальцификации, чтобы распознать артерии, прежде чем вводить какой-либо контрастный агент во время ангиограммы.
Многие подходы были рекламируются как методы уменьшения или обращения вспять прогрессирования атеромы:
В развитых странах с улучшенным общественным здоровьем, Инфекционный контроль и увеличение продолжительности жизни, атеромные процессы становятся все более важной проблемой и бременем для общества. Атеромы продолжают оставаться основной причиной инвалидности и смерти, несмотря на тенденцию к постепенному улучшению с начала 1960-х годов (с поправкой на возраст пациента). Таким образом, предпринимаются все более активные усилия по лучшему пониманию, лечению и профилактике этой проблемы.
По данным США, 2004 г., у 65% мужчин и 47% женщин первый симптом сердечно-сосудистым заболеванием является инфаркт миокарда (сердечный приступ) или внезапная смерть (смерть в течение одного часа с момента появления симптомов).
Значительная часть событий, нарушающих кровоток в артериях, происходит на местах с менее чем 50% сужением просвета. Кардиологический стресс-тест, традиционно наиболее часто применяемый неинвазивный метод тестирования на ограничение кровотока, обычно выявляет только сужение просвета на ~ 75% или больше, хотя некоторые врачи рекомендуют методы ядерного стресса, которые иногда могут обнаружить всего 50 %.
Внезапный характер осложнений ранее существовавшей атеромы, уязвимой бляшки (неокклюзионной или мягкой бляшки), с 1950-х годов привел к развитию интенсивной терапии отделения и комплексные лечебно-хирургические вмешательства. Ангиография и позже кардиологическое стресс-тестирование было начато для визуализации или косвенного выявления стеноза. Затем последовало шунтирование, трансплантация отвесом вены, иногда артерий, вокруг стенозов и, совсем недавно, ангиопластика, теперь включая стенты, самые последние стенты с лекарственным покрытием, для более открытого растяжения стенозов.
Тем не менее, несмотря на эти медицинские достижения, с успехом в уменьшении симптомов стенокардии и уменьшении крови flow, события разрыва атеромы остаются основной проблемой и все еще иногда приводят к внезапной инвалидности и смерти, несмотря на даже самое быстрое, массовое и квалифицированное медицинское и хирургическое вмешательство, доступное где-либо сегодня. Согласно некоторым клиническим испытаниям, операция шунтирования и процедуры ангиопластики в лучшем случае оказали минимальное влияние на общую выживаемость, если таковые имели место. Как правило, смертность от операций шунтирования составляет от 1 до 4%, от ангиопластики от 1 до 1,5%.
Кроме того, эти сосудистые вмешательства часто проводятся только после того, как у человека появятся симптомы, часто уже частично нетрудоспособны, в результате болезнь. Также очевидно, что и ангиопластика, и шунтирование не предотвращают будущего сердечного приступа.
Старые методы понимания атеромы, относящиеся к периоду до Второй мировой войны, основывались на данных вскрытия. Данные вскрытия уже давно показали появление жировых полос в более позднем детстве с медленным бессимптомным прогрессированием на протяжении десятилетий.
Один из способов увидеть атерому - это очень инвазивное и дорогостоящее ВСУЗИ УЗИ технологии; он дает нам точный объем внутренней интимы плюс центральные слои media длиной около 25 мм (1 дюйм) длины артерии. К сожалению, он не дает информации о прочности конструкции артерии. Ангиография не визуализирует атерому; он только делает видимым кровоток внутри кровеносных сосудов. Альтернативные методы, которые не являются или менее физически инвазивными и менее дорогими для каждого отдельного теста, использовались и продолжают развиваться, например, с использованием компьютерной томографии (CT; во главе с электронно-лучевой томографией, учитывая его большую скорость) и магнитно-резонансной томографии (МРТ). Самым многообещающим с начала 1990-х годов была EBT, обнаруживающая кальциноз в атероме до того, как у большинства людей начнутся клинически распознаваемые симптомы и слабость. Терапия статинами (для снижения холестерина) не замедляет скорость кальцификации, как определено с помощью компьютерной томографии. МРТ-визуализация стенки коронарного сосуда, хотя в настоящее время ограничивается научными исследованиями, продемонстрировала способность обнаруживать утолщение стенки сосуда у бессимптомных лиц с высоким риском. В качестве неинвазивного метода без ионизирующего излучения методы на основе МРТ могут найти применение в будущем для мониторинга прогрессирования и регресса заболевания. Большинство методов визуализации используется в исследованиях, они не являются широко доступными для большинства пациентов, имеют значительные технические ограничения, не получили широкого признания и, как правило, не покрываются медицинскими страховыми компаниями.
Судя по клиническим испытаниям на людях, он имеет становится все более очевидным, что более эффективным направлением лечения является замедление, остановка и даже частичное обращение вспять процесса роста атеромы. Существует несколько проспективных эпидемиологических исследований, включая исследование Риск атеросклероза в сообществах (ARIC) и Исследование здоровья сердечно-сосудистой системы (CHS), которые подтвердили прямую корреляцию между каротидом Intima- толщина среды (CIMT) с инфарктом миокарда и риском инсульта у пациентов без сердечно-сосудистых заболеваний в анамнезе. Исследование ARIC было проведено с участием 15 792 человек в возрасте от 5 до 65 лет в четырех различных регионах США в период с 1987 по 1989 год. Измеряли исходный CIMT, и измерения повторялись с 4-7-летними интервалами с помощью ультразвукового исследования сонной артерии в режиме B в эта учеба. Увеличение CIMT коррелировало с повышенным риском ИБС. CHS была начата в 1988 году, и связь CIMT с риском инфаркта миокарда и инсульта была исследована у 4476 пациентов в возрасте 65 лет и младше. По прошествии приблизительно шести лет наблюдения измерения CIMT были коррелированы с сердечно-сосудистыми событиями.
Paroi artérielle et Risque Cardiovasculaire в Азии, Африке / на Ближнем Востоке и в Латинской Америке (PARC-AALA) - еще один важный крупный план. Масштабное исследование, в котором приняли участие 79 центров из стран Азии, Африки, Ближнего Востока и Латинской Америки, а также изучалось распределение CIMT по разным этническим группам и его связь с оценкой сердечно-сосудистой системы Фрамингема. Мультилинейный регрессионный анализ показал, что повышенная оценка сердечно-сосудистой системы по Фрамингему была связана с CIMT и каротидной бляшкой независимо от географических различий.
Cahn et al. проспективно наблюдали 152 пациента с ишемической болезнью сердца в течение 6–11 месяцев с помощью ультразвукового исследования сонной артерии и отметили 22 сосудистых события (инфаркт миокарда, транзиторная ишемическая атака, инсульт и коронарная ангиопластика) за этот период времени. Они пришли к выводу, что атеросклероз сонных артерий, измеренный этим неинтервенционным методом, имеет прогностическое значение у пациентов с коронарной артерией.
В Роттердамском исследовании, Bots et al. наблюдали за 7 983 пациентами старше 55 лет в течение среднего периода 4,6 года и сообщили о 194 случаях инфаркта миокарда за этот период. CIMT был значительно выше в группе инфаркта миокарда по сравнению с другой группой. Demircan et al. обнаружили, что CIMT у пациентов с острым коронарным синдромом был значительно выше по сравнению с пациентами со стабильной стенокардией.
В другом исследовании сообщалось, что максимальное значение CIMT 0,956 мм имело чувствительность 85,7% и специфичность 85,1%. для прогнозирования ангиографической ИБС. Основную группу составили пациенты, поступившие в кардиологическое отделение поликлиники с симптомами стабильной стенокардии. Исследование показало, что CIMT был выше у пациентов со значительной ИБС, чем у пациентов с некритическими коронарными поражениями. Регрессионный анализ показал, что утолщение среднего комплекса интима-медиа более чем на 1.0 было предиктором значительных ИБС у наших пациентов. Наблюдалось постепенное значительное увеличение CIMT с увеличением количества вовлеченных коронарных сосудов. В соответствии с литературными данными было обнаружено, что CIMT был значительно выше при наличии CAD. Кроме того, CIMT увеличивался по мере увеличения количества вовлеченных сосудов, и самые высокие значения CIMT были отмечены у пациентов с поражением главной левой коронарной артерии. Однако клинические испытания на людях не позволяют получить клинические и медицинские доказательства, отчасти потому, что бессимптомный характер атером делает их особенно трудными для изучения. Обнадеживающие результаты были получены при сканировании толщины интимы-медиа сонной артерии (ТИМТ можно измерить с помощью УЗИ в режиме В), витаминов группы В, которые уменьшают коррозию белка, гомоцистеин и уменьшают шейку сонную артерию объем и толщина бляшки на артериях, а также инсульт даже на поздних стадиях заболевания.
Кроме того, понимание того, что движет развитием атеромы, является сложным с множеством вовлеченных факторов, только некоторые из которых, такие как липопротеины и, что более важно, анализ подкласса липопротеинов, уровень сахара в крови и гипертония наиболее известны и исследованы. В последнее время некоторые из сложных паттернов иммунной системы, которые стимулируют или ингибируют врожденные процессы запуска воспалительных макрофагов, участвующие в прогрессировании атеромы, постепенно лучше выясняются на животных моделях атеросклероза. 178>
| Классификация | D |
|---|