 Расположение гена MT-ATP8 в митохондриальном геноме человека. MT-ATP8 - один из двух митохондриальных генов АТФ-синтазы (красные прямоугольники).
Расположение гена MT-ATP8 в митохондриальном геноме человека. MT-ATP8 - один из двух митохондриальных генов АТФ-синтазы (красные прямоугольники). 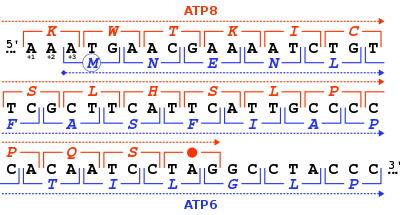 46 нуклеотидов перекрываются в рамках считывания митохондриальных генов человека MT-ATP8 и MT-ATP6. Для каждого триплета нуклеотидов (квадратные скобки) дается соответствующая аминокислота (однобуквенный код) либо в рамке +1 для MT-ATP8 (красным), либо в рамке +3 для MT-ATP6 (синим цветом)..
46 нуклеотидов перекрываются в рамках считывания митохондриальных генов человека MT-ATP8 и MT-ATP6. Для каждого триплета нуклеотидов (квадратные скобки) дается соответствующая аминокислота (однобуквенный код) либо в рамке +1 для MT-ATP8 (красным), либо в рамке +3 для MT-ATP6 (синим цветом).. | Белок АТФ-синтазы 8 (метазоа) | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Идентификаторы | |||||||||
| Условное обозначение | ATP-synt_8 | ||||||||
| Pfam | PF00895 | ||||||||
| Клан пфам | CL0255 | ||||||||
| ИнтерПро | IPR001421 | ||||||||
| |||||||||
| Субъединица 8 F0 растительной АТФ-синтазы | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Идентификаторы | |||||||||
| Условное обозначение | YMF19 | ||||||||
| Pfam | PF02326 | ||||||||
| Клан пфам | CL0255 | ||||||||
| ИнтерПро | IPR003319 | ||||||||
| |||||||||
| Грибковый белок АТФ-синтазы 8 (A6L) | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Идентификаторы | |||||||||
| Условное обозначение | Fun_ATP-synt_8 | ||||||||
| Pfam | PF05933 | ||||||||
| Клан пфам | CL0255 | ||||||||
| ИнтерПро | IPR009230 | ||||||||
| |||||||||
MT-ATP8 (или ATP8) представляет собой митохондриальный ген с полным названием «митохондриально кодируемая субъединица мембраны АТФ-синтазы 8», который кодирует субъединицу митохондриальной АТФ-синтазы, субъединицу 8 АТФ-синтазы F o (или субъединицу A6L). Эта субъединица принадлежит к комплексу F o большой трансмембранной АТФ-синтазы F-типа. Этот фермент, также известный как комплекс V, отвечает за заключительную стадию окислительного фосфорилирования в цепи переноса электронов. В частности, один сегмент АТФ-синтазы позволяет положительно заряженным ионам, называемым протонами, проходить через специализированную мембрану внутри митохондрий. Другой сегмент фермента использует энергию, создаваемую этим потоком протонов, для преобразования молекулы, называемой аденозиндифосфатом (АДФ), в АТФ. Субъединица 8 отличается в последовательности между Metazoa, растениями и грибами.
Белок синтазы АТФ 8 человека и других млекопитающих кодируется в митохондриального генома по МТ-ATP8 гена. Когда полный человеческий митохондриальный геном был впервые опубликован, МТ-ATP8 ген был описан как неустановленной рамки считывания ЕФД A6L. Необычной особенностью гена MT-ATP8 является его 46-нуклеотидное перекрытие с геном MT-ATP6. Что касается рамки считывания (+1) MT-ATP8, ген MT-ATP6 начинается на рамке считывания +3.
Белок MT-ATP8 весит 8 кДа и состоит из 68 аминокислот. Белок является субъединицей F 1 F o АТФазы, также известной как Комплекс V, который состоит из 14 ядерных и 2 митохондриальных субъединиц. АТФазы F-типа состоят из двух структурных доменов, F 1, содержащего внемембранное каталитическое ядро, и F o, содержащего мембранный протонный канал, связанных между собой центральным стержнем и периферическим стержнем. Как субъединица A, MT-ATP8 содержится в некаталитической трансмембранной F o части комплекса, включающего протонный канал. Каталитическая часть митохондриальной АТФ-синтазы состоит из 5 различных субъединиц (альфа, бета, гамма, дельта и эпсилон), собранных со стехиометрией 3 альфа, 3 бета и одного представителя остальных 3. Протонный канал состоит из трех основные субъединицы (а, б, в). Этот ген кодирует дельта-субъединицу каталитического ядра. Были идентифицированы альтернативно сплайсированные варианты транскриптов, кодирующие ту же изоформу.
МТ-ATP8 ген кодирует субъединицу митохондриальных АТФ - синтазы, расположенную внутри тилакоидов мембраны и внутренней митохондриальной мембраны. Митохондриальной АТФ - синтаза катализирует синтез АТФ с использованием в качестве электрохимического градиента из протонов через внутреннюю мембрану в процессе окислительного фосфорилирования. Область F o вызывает вращение F 1, который имеет водорастворимый компонент, гидролизующий АТФ, и вместе F 1 F o создает путь для движения протонов через мембрану.
Эта белковая субъединица, по-видимому, является неотъемлемым компонентом стебля статора дрожжевых митохондриальных F-АТФаз. Стержень статора закреплен в мембране и предотвращает бесполезное вращение субъединиц АТФазы относительно ротора во время связанного синтеза / гидролиза АТФ. Эта субъединица может выполнять аналогичную функцию у Metazoa.
Номенклатура фермента имеет длинную историю. Фракция F 1 получила свое название от термина «Фракция 1», а F o (написанная как нижняя буква «o», а не «ноль») получила свое название от фракции связывания олигомицина, типа природного антибиотика. который способен ингибировать F o- звено АТФ-синтазы. Область F o АТФ-синтазы представляет собой протонную пору, встроенную в митохондриальную мембрану. Он состоит из трех основных субъединиц A, B и C и (у человека) шести дополнительных субъединиц, d, e, f, g, MT-ATP6 (или F6) и MT-ATP8 (или A6L). Трехмерная структура гомолога этой субъединицы E. coli была смоделирована на основании данных электронной микроскопии (цепь M PDB : 1c17 ). Он образует трансмембранный 4-α-пучок.
Мутации MT-ATP8 и других генов, влияющих на окислительное фосфорилирование в митохондриях, были связаны с множеством нейродегенеративных и сердечно-сосудистых заболеваний, включая дефицит митохондриального комплекса V, наследственную оптическую невропатию Лебера (LHON), митохондриальную энцефаломиопатию с инсультоподобными эпизодами ( MELAS )., синдром Ли и NARP синдром. Большинство клеток организма содержат тысячи митохондрий, каждая из которых имеет одну или несколько копий митохондриальной ДНК. Тяжесть некоторых митохондриальных нарушений связана с процентным содержанием митохондрий в каждой клетке, имеющей определенное генетическое изменение. Люди с синдромом Ли из-за мутации гена MT-ATP6, как правило, имеют очень высокий процент митохондрий с мутацией (от более 90 процентов до 95 процентов). Менее серьезные особенности NARP являются результатом более низкого процента митохондрий с мутацией, обычно от 70 до 90 процентов. Поскольку эти два состояния являются результатом одних и тех же генетических изменений и могут возникать у разных членов одной семьи, исследователи полагают, что они могут представлять собой спектр перекрывающихся признаков вместо двух различных синдромов.
Дефицит митохондриального комплекса V проявляется гетерогенными клиническими проявлениями, включая невропатию, атаксию, гипертрофическую кардиомиопатию. Гипертрофическая кардиомиопатия может проявляться от незначительной до крайней гипертрофии, от минимального до обширного фиброза и дисбаланса миоцитов, отсутствовать при тяжелой обструкции выходного тракта левого желудочка и выраженных контурах / морфологиях перегородки с чрезвычайно различным клиническим течением.
Митохондриальной комплекс V дефицит дефицит (дефицит) или потерю функции в комплексной V в цепи переноса электронов, которые могут вызвать широкий спектр признаков и симптомов, влияющих на многие органы и системы организма, особенно нервной системы и сердца. Расстройство может быть опасным для жизни в младенчестве или раннем детстве. У больных могут быть проблемы с кормлением, медленный рост, низкий мышечный тонус ( гипотония ), крайняя утомляемость ( вялость ) и задержка в развитии. У них обычно повышается уровень молочной кислоты в крови ( лактоацидоз ), что может вызвать тошноту, рвоту, слабость и учащенное дыхание. Высокий уровень аммиака в крови ( гипераммонемия ) также может возникать у пораженных людей и в некоторых случаях приводить к нарушению функции мозга ( энцефалопатия ) и повреждению других органов. Атаксия, микроцефалия, задержка развития и умственная отсталость наблюдались у пациентов с мутацией сдвига рамки считывания в MT-ATP6. Это вызывает вставку C в положение 8612, что приводит к усеченному белку длиной всего 36 аминокислот и двум однонуклеотидным полиморфизмам Tgt; C в положениях 8610 и 8614, которые приводят к гомополимерному цитозиновому участку.
Гипертрофическая кардиомиопатия, общая черта дефицита митохондриального комплекса V, характеризуется утолщением ( гипертрофией ) сердечной мышцы, что может привести к сердечной недостаточности. Мутация m.8528Tgt; C возникает в перекрывающейся области генов MT-ATP6 и MT-ATP8 и была описана у нескольких пациентов с детской кардиомиопатией. Эта мутация изменяет кодон инициации в MT-ATP6 на треонин, а также заменяет триптофан на аргинин в положении 55 MT-ATP8. У людей с дефицитом митохондриального комплекса V также могут быть характерные черты лица, в том числе высокий лоб, изогнутые брови, внешние углы глаз, направленные вниз (наклонные глазные щели ), выступающая переносица, низко посаженные уши и т. Д. тонкие губы и маленький подбородок ( микрогнатия ).
Детская гипертрофическая кардиомиопатия (CMHI) также вызывается мутациями, затрагивающими различные генетические локусы, включая MT-ATP6 и MT-ATP8. Детская форма гипертрофической кардиомиопатии, сердечного заболевания, характеризующегося гипертрофией желудочков, которая обычно асимметрична и часто затрагивает межжелудочковую перегородку. Симптомы включают одышку, обморок, коллапс, сердцебиение и боль в груди. Их легко спровоцировать упражнения. Заболевание имеет внутрисемейную и внутрисемейную изменчивость, от доброкачественных до злокачественных форм с высоким риском сердечной недостаточности и внезапной сердечной смерти.
Эта статья включает текст из Национальной медицинской библиотеки США, который находится в общественном достоянии.
Эта статья включает текст из общественного достояния Pfam и InterPro : IPR001421