Генетическая структура H5N1 - это молекулярная структура РНК вируса H5N1 .
H5N1 является подтипом вируса гриппа A. Эксперты считают, что он может мутировать в форму, которая легко передается от человека к человеку. Если такая мутация произойдет, она может остаться подтипом H5N1 или сместить подтипы, как это произошло с H2N2, когда он превратился в штамм Hong Kong Flu H3N2.
H5N1. мутировал через антигенный дрейф в десятки высоко патогенных разновидностей, но все они в настоящее время принадлежат генотипу Z вируса птичьего гриппа H5N1. Генотип Z возник в результате перегруппировки в 2002 году из более ранних высоко патогенных генотипов H5N1, которые впервые появились в Китае в 1996 году у птиц и Гонконг в 1997 г. в человек. «Вирусы H5N1 от инфекций человека и близкородственные вирусы птиц, выделенные в 2004 и 2005 гг., Принадлежат к одному генотипу, часто называемому генотипом Z».
Это заражение людей совпало с эпизоотией (эпидемией у животных) гриппа H5N1 в популяции домашней птицы Гонконга. Вспышка этой панзоотической болезни (болезни, поражающей животных многих видов, особенно на обширных территориях) была остановлена за счет гибели всей популяции домашней птицы на территории. Название H5N1 относится к подтипам поверхностных антигенов, присутствующих в вирусе : гемагглютинин тип 5 и нейраминидаза тип 1.
Генотип Z H5N1 теперь является доминантным генотипом H5N1. Генотип Z является эндемическим для птиц Юго-Восточной Азии и представляет собой долгосрочную угрозу пандемии.
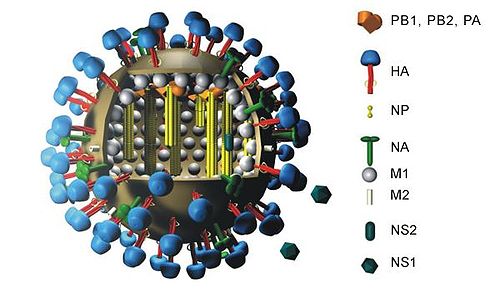
Вирусы гриппа A имеют 11 генов на восьми отдельных РНК молекулах [1] :
Двумя наиболее важными молекулами РНК являются HA и PB1. HA создает поверхностный антиген, который особенно важен для трансмиссивности. PB1 создает молекула вирусной полимеразы, которая особенно важна для вирулентности.
Молекула HA РНК содержит ген HA, который кодирует гемагглютинин, который является антигенный гликопротеин обнаружен на поверхности вирусов гриппа и отвечает за связывание вируса с клеткой, которая является быть инфицированным. Hemag глутинин образует шипы на поверхности вирусов гриппа, которые прикрепляют вирусы к клеткам. Это прикрепление требуется для эффективного переноса генов вируса гриппа в клетки, процесса, который может быть заблокирован антителами, связывающимися с белками гемагглютинина.
Одним из генетических факторов различения вирусов гриппа человека и вирусов птичьего гриппа является то, что НА птичьего гриппа связывает альфа-2–3 рецепторы сиаловой кислоты, а НА гриппа человека связывает альфа 2-6 рецепторы сиаловой кислоты.. Вирусы свиного гриппа обладают способностью связывать оба типа рецепторов сиаловой кислоты. У людей есть рецепторы птичьего типа с очень низкой плотностью, а у цыплят есть рецепторы человеческого типа с очень низкой плотностью. Было обнаружено, что некоторые изоляты, взятые от инфицированного H5N1 человека, имеют мутации HA в положениях 182, 192, 223, 226 или 228, и было показано, что эти мутации влияют на избирательное связывание вируса с ранее упомянутыми сиаловой кислотой птиц и / или или рецепторы на поверхности клеток человека. Это типы мутаций, которые могут превратить вирус птичьего гриппа в вирус пандемического гриппа.
Исследование 2008 вирулентности, в ходе которого в лаборатории был скрещен вирус птичьего гриппа H5N1, который циркулировал в Таиланде в 2004 году. и вирус человеческого гриппа H3N2, выделенный в Вайоминг в 2003 г., дал 63 вируса, представляющих различные потенциальные комбинации генов вируса гриппа A человека и птиц .. Одна из пяти была смертельной для мышей при низких дозах. Вирус, который наиболее близко соответствовал вирусу H5N1 по вирулентности, был вирусом с гемагглютинином (HA), нейраминидазой (NA) и молекулами РНК вируса птичьего гриппа PB1 с их генами, объединенными с остальными пять молекул РНК (PB2, PA, NP, M и NS) с их генами из вируса человеческого гриппа. Оба вируса из пандемии 1957 года и пандемии 1968 года несли ген PB1 вируса птичьего гриппа. Авторы предполагают, что получение гена PB1 вируса птичьего гриппа может быть критическим шагом в потенциальном пандемическом вирусе гриппа, возникающем в результате перегруппировки."
кодов PB1 для белка PB1 и белка PB1-F2.. Белок PB1 является критическим компонентом вирусной полимеразы. Белок PB1-F2 кодируется альтернативной открытой рамкой считывания сегмента РНК PB1 и «взаимодействует с 2 компонентами комплекса пор перехода митохондриальной проницаемости, ANT3 и VDCA1, [сенсибилизируя] клетки к апоптозу. [...] PB1-F2, вероятно, способствует вирусной патогенности и может играть важную роль в определении степени тяжести пандемического гриппа ». Это было обнаружено Ченом и др. и сообщается в Nature. «После сравнения вирусов, вызванных вспышкой H5N1 в Гонконге в 1997 году, в последовательности PB1-F2 в положении 66 было обнаружено одно аминокислотное изменение (N66S), которое коррелировало с патогенностью. Такое же аминокислотное изменение (N66S) было также обнаружено в PB1- Белок F2 пандемического вируса A / Brevig Mission / 18 1918 г. "
Семейство ортомиксовирусов состоит из 5 родов: Influenzavirus A, Influenzavirus B, Influenzavirus C, Isavirus и Thogotovirus.
«РНК-вирусы» включают «вирусы оцРНК с отрицательным смыслом», которые включают семейство «Orthomyxoviridae», которое содержит пять родов, классифицированных по вариациям. в антигенах нуклеопротеина (NP и M). Одним из них является род «Influenzavirus A», который состоит из одного вида, называемого «вирус гриппа A »; один из его подтипов - H5N1..
H5N1 (как и другие вирусы птичьего гриппа) имеет штаммы, называемые «высокопатогенными» (HP) и «низкопатогенными» (LP). Вирусы птичьего гриппа, вызывающие HPAI, очень вирулентны, а уровень смертности в зараженных стадах часто приближается к 100%. Вирусы LPAI обычно имеют более низкую вирулентность, но эти вирусы могут служить предшественниками вирусов HPAI. Нынешний штамм H5N1, ответственный за гибель домашних птиц в Азии, представляет собой штамм HPAI; другие штаммы H5N1, встречающиеся в других странах мира, менее вирулентны и поэтому классифицируются как штаммы LPAI. Все штаммы HPAI, идентифицированные на сегодняшний день, включают подтипы H5 и H7. Различие касается патогенности у домашней птицы, а не у человека. Обычно высокопатогенный птичий вирус не является высокопатогенным ни для людей, ни для птиц, не относящихся к домашней птице. Этот нынешний штамм H5N1 необычен тем, что является смертельным для многих видов.
И «грипп» (означающий грипп), и «А» (означающий вид типа А) могут использоваться как прилагательные к существительному «вирус», что приводит к существительной фразе «вирус гриппа А»; которое, если оно написано с заглавной буквы, является существительным собственным вирусом гриппа A, которое является названием вида, к которому также относится существительное словосочетание.
A Вирус - это один из типов микроскопических паразитов, инфицирующих клетки в биологических организмах.
Orthomyxoviridae представляют собой семейство РНК-вирусов, которые инфицируют позвоночных. Он включает те вирусы, которые вызывают грипп. Вирусы этого семейства содержат от 7 до 8 сегментов линейной одноцепочечной РНК с отрицательным смыслом.
«Вирус гриппа» относится к подмножеству Orthomyxoviridae, которые создают грипп. Эта таксономическая категория не основана на филогенетике.
Вирусы гриппа A имеют 10 генов на восьми отдельных молекулах РНК, которые по указанным причинам выше обозначены PB2, PB1, PA, HA, NP, NA, M и NS. HA, NA и M определяют структуру белков, которые являются наиболее значимыми с медицинской точки зрения в качестве мишеней для противовирусных препаратов и антител. (Одиннадцатый недавно открытый ген, называемый PB1-F2, иногда создает белок, но отсутствует в некоторых изолятах вируса гриппа.) Эта сегментация генома гриппа способствует генетической рекомбинации путем перегруппировки сегментов у хозяев. которые заражены двумя разными вирусами гриппа одновременно. Вирус гриппа A является единственным видом в Influenzavirus A рода семейства Orthomyxoviridae и представляет собой одноцепочечные, сегментированные РНК-вирусы с отрицательным смыслом.
«РНК-полимераза вируса гриппа представляет собой многофункциональный комплекс, состоящий из трех вирусных белков PB1, PB2 и PA, которые вместе с вирусным нуклеопротеином NP образуют минимальный комплемент, необходимый для синтеза и репликации вирусной мРНК».
Вирусы гриппа имеют относительно высокую скорость мутаций, что характерно для РНК-вирусы. Сегментация генома гриппа облегчает генетическую рекомбинацию путем перегруппировки сегментов у хозяев, которые инфицированы двумя разными вирусами гриппа одновременно. Вирусы H5N1 могут реассортировать гены с другими штаммами, которые совместно инфицируют организм-хозяин, такой как свинья, птица или человек, и мутировать в форму, которая может легко передаваться среди людей. Это один из многих возможных путей к пандемии.
Способность различных штаммов гриппа проявлять видовую селективность в значительной степени обусловлена вариациями в генах гемагглютинина. Генетические мутации в гене гемагглютинина, вызывающие одиночные замены аминокислот, могут значительно изменить способность вирусных белков гемагглютинина связываться с рецепторами на поверхности клеток-хозяев. Такие мутации в вирусах птичьего гриппа H5N1 могут изменить штаммы вирусов с неэффективных для инфицирования клеток человека на столь же эффективные в отношении инфицирования человека, как и более распространенные типы вирусов гриппа человека. Это не означает, что замена одной аминокислоты может вызвать пандемию, но это означает, что замена одной аминокислоты может привести к тому, что вирус птичьего гриппа, не являющийся патогенным для человека, станет патогенным для человека.
H3N2 («свиной грипп ») эндемичен для свиней в Китае и был обнаружен у свиней во Вьетнаме, что усиливает опасения по поводу появления новых вариантных штаммов. Доминирующим штаммом вируса однолетнего гриппа в январе 2006 г. был H3N2, который теперь устойчив к стандартным противовирусным препаратам амантадин и римантадин. Возможность обмена генами H5N1 и H3N2 посредством реассортации вызывает серьезную озабоченность. Если произойдет реассортировка H5N1, он может остаться подтипом H5N1 или может сместить подтипы, как это произошло с H2N2, когда он превратился в штамм гонконгского гриппа H3N2.
Оба H2N2 и H3N2 пандемические штаммы содержали сегменты РНК вируса птичьего гриппа . «В то время как пандемические вирусы гриппа человека 1957 г. (H2N2) и 1968 г. (H3N2) явно возникли в результате перегруппировки вирусов человека и птиц, вирус гриппа, вызвавший« испанский грипп »в 1918 г., по всей видимости, полностью произошел от птичьего источника».
В июле 2004 г. исследователи во главе с Х. Дэном из Харбинского института ветеринарных исследований, Харбин, Китай и профессором Робертом Г. Вебстером из Св. Детская исследовательская больница Джуд, Мемфис, Теннесси, сообщила о результатах экспериментов, в которых мыши подвергались воздействию 21 изолята подтвержденного штамма H5N1, полученного от уток в Китае в период с 1999 по 2002 год. Они обнаружили «четкую временную закономерность прогрессивно возрастающей патогенности». Результаты, представленные доктором Вебстером в июле 2005 года, показывают дальнейшее прогрессирование патогенности у мышей и более длительное выделение вируса утками.
Азиатская линия HPAI A (H5N1) разделена на две антигенные клады. «В кладу 1 входят изоляты человека и птицы из Вьетнама, Таиланда и Камбоджи, а также изоляты птиц из Лаоса и Малайзии. Вирусы Clade 2 были впервые идентифицированы в изолятах птиц из Китая, Индонезии, Японии и Южной Кореи, а затем распространились на запад в Ближний Восток, Европа и Африка. Вирусы 2-го класса в первую очередь ответственны за инфицирование человека H5N1, которое произошло в конце 2005 и 2006 гг. ВОЗ. Генетический анализ выявил шесть субкладов клады 2, три из которых имеют четкое географическое распространение и были вовлечены в инфицирование людей: Карта
Исследование 2007 года, посвященное субкладу EMA, пролило дополнительный свет на мутации EMA. «36 новых изолятов, представленных здесь, значительно расширяют объем данных о последовательностях полных геномов, доступных для недавних изолятов птичьего гриппа (H5N1). До нашего проекта GenBank содержал только 5 других полных геномов из Европы за период 2004–2006 годов, и он содержал нет полных геномов с Ближнего Востока или Северной Африки. Наш анализ показал несколько новых результатов. Во-первых, все европейские, ближневосточные и африканские образцы попадают в кладу, отличную от других современных азиатских клад, все из которых имеют общее происхождение с оригинальный гонконгский штамм 1997 года. Филогенетические деревья, построенные на каждом из 8 сегментов, демонстрируют последовательную картину трех линий, как показано на дереве HA, показанном на рисунке 1. Две из клад содержат исключительно вьетнамские изоляты; меньшая из них, с 5 Мы маркируем изоляты V1; более крупная клада с 9 изолятами - это V2. Все остальные 22 изолята попадают в третью, четко различимую кладу, обозначенную EMA, которая включает образцы из Европы, Средней Азии. ле Восток и Африка. Деревья для остальных 7 сегментов имеют аналогичную топологию, с четко разделенными кладами V1, V2 и EMA в каждом случае. Анализ всех доступных полных геномов гриппа (H5N1) и 589 последовательностей HA позволил выделить кладу EMA в отличие от основных клад, циркулирующих в Китайской Народной Республике, Индонезии и Юго-Восточной Азии ».
См. https : //web.archive.org/web/20090709040039/http: //who.int/csr/disease/avian_influenza/H5CompleteTree.pdf для генетического дерева 1342 вирусов H5N1 на основе их гена HA с указанием их клады