Рибосомный сдвиг рамки, также известный как трансляционный сдвиг рамки или трансляционное перекодирование, - это биологический феномен, который возникает во время трансляции, что приводит к производству множества уникальных белков из одной мРНК. Процесс может быть запрограммирован нуклеотидной последовательностью мРНК и иногда зависит от вторичной трехмерной структуры мРНК. Он был описан главным образом в вирусах (особенно ретровирусах ), ретротранспозонах и бактериальных вставных элементах, а также в некоторых клеточных генах.
Белки транслируются путем считывания тринуклеотидов на цепи мРНК, также известных как кодоны, от одного конца мРНК к другому (от 5 'до 3' конца), начиная с аминокислоты метионина в качестве начала (инициация). кодон AUG. Каждый кодон переводится в одну аминокислоту. Сам код считается вырожденным, что означает, что конкретная аминокислота может определяться более чем одним кодонами. Однако сдвиг любого числа нуклеотидов, которое не делится на 3 в рамке считывания, приведет к тому, что последующие кодоны будут считываться по-разному. Это эффективно изменяет рамку считывания рибосом.
В этом примере следующее предложение со словами из трех букв имеет смысл при чтении с начала:
|Start|THE CAT AND THE MAN ARE FAT... |Start|123 123 123 123 123 123 123...
Однако, если рамка считывания сдвинута на одну букву между T и H первого слова (фактически сдвиг кадра +1, если рассматривать позицию 0 как начальную позицию T),
T|Start|HEC ATA NDT HEM ANA REF AT... -|Start|123 123 123 123 123 123 12...
тогда предложение читается иначе, не имея смысла.
В этом примере следующая последовательность представляет собой область митохондриального генома человека с двумя перекрывающимися генами MT-ATP8 и MT-ATP6. При чтении с самого начала эти кодоны имеют смысл для рибосомы и могут быть переведены в аминокислоты (АА) под митохондриальным кодом позвоночных :
|Start|AAC GAA AAT CTG TTC GCT TCA... |Start|123 123 123 123 123 123 123... | AA | N E N L F A S...
Однако давайте изменим рамку считывания, начав один нуклеотид ниже по течению (фактически «сдвиг рамки +1», если рассматривать позицию 0 как начальную позицию A):
A|Start|ACG AAA ATC TGT TCG CTT CA... -|Start|123 123 123 123 123 123 12... | AA | T K I C S L...
Теперь из-за сдвига кадра на +1 последовательность ДНК читается по-другому. Следовательно, разные рамки считывания кодонов дают разные аминокислоты.
В случае трансляции рибосомы сдвиг рамки может привести либо к бессмыслице (преждевременный стоп-кодон) после сдвига рамки, либо к созданию совершенно нового белка после сдвига рамки. В случае, когда сдвиг рамки приводит к бессмыслице, путь NMD ( nonsense-опосредованный распад мРНК ) может разрушить транскрипт мРНК, поэтому сдвиг рамки может служить методом регулирования уровня экспрессии связанного гена.
В вирусах это явление может быть запрограммировано на то, чтобы возникать в определенных местах, и позволяет вирусу кодировать несколько типов белков из одной и той же мРНК. Известные примеры включают ВИЧ-1 (вирус иммунодефицита человека), RSV ( вирус саркомы Рауса ) и вирус гриппа (грипп), которые все полагаются на сдвиг рамки считывания для создания надлежащего соотношения 0-кадра (нормальная трансляция) и «транс-кадра». (кодируется последовательностью со сдвигом рамки считывания) белков. Его использование в вирусах в первую очередь предназначено для сжатия большего количества генетической информации в меньший объем генетического материала.
У эукариот он, по-видимому, играет роль в регуляции уровней экспрессии генов, генерируя преждевременные остановки и производя нефункциональные транскрипты.
Наиболее распространенный тип сдвига кадра - это -1 сдвиг кадра или запрограммированный -1 рибосомный сдвиг кадра (-1 PRF). Другие, более редкие типы сдвига кадра включают сдвиг кадра +1 и -2. Считается, что сдвиг кадра -1 и +1 управляется разными механизмами, которые обсуждаются ниже. Оба механизма управляются кинетически.
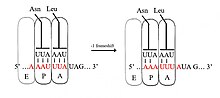 Тандемное проскальзывание 2 тРНК на скользкой последовательности вируса саркомы Рауса. После сдвига рамки считывания новые пары оснований правильны в первом и втором нуклеотидах, но неверны в положении вобуляции. Указаны участки рибосомы E, P и A. Расположение растущей полипептидной цепи не указано на изображении, потому что еще нет единого мнения о том, происходит ли проскальзывание -1 до или после того, как полипептид переносится с тРНК P-сайта на тРНК A-сайта (в данном случае от тРНК Asn к тРНК Leu тРНК).
Тандемное проскальзывание 2 тРНК на скользкой последовательности вируса саркомы Рауса. После сдвига рамки считывания новые пары оснований правильны в первом и втором нуклеотидах, но неверны в положении вобуляции. Указаны участки рибосомы E, P и A. Расположение растущей полипептидной цепи не указано на изображении, потому что еще нет единого мнения о том, происходит ли проскальзывание -1 до или после того, как полипептид переносится с тРНК P-сайта на тРНК A-сайта (в данном случае от тРНК Asn к тРНК Leu тРНК). При сдвиге -1 кадра рибосома сдвигается на один нуклеотид назад и продолжает трансляцию в кадре -1. Обычно есть три элемента, которые составляют сигнал сдвига кадра -1: скользкая последовательность, спейсерная область и вторичная структура РНК. Скользкая последовательность соответствует мотиву X_XXY_YYH, где XXX - любые три идентичных нуклеотида (хотя бывают некоторые исключения), YYY обычно представляет UUU или AAA, а H - A, C или U. Поскольку структура этого мотива содержит 2 смежных 3-нуклеотида. Повторы полагают, что сдвиг рамки -1 описывается тандемной моделью проскальзывания, в которой рибосомный антикодон тРНК P-сайта восстанавливает пары с XXY на XXX, а антикодон A-сайта восстанавливает пары с YYH на YYY одновременно. Эти новые пары идентичны парам с нулевым кадром, за исключением их третьих позиций. Это различие не оказывает существенного неблагоприятного воздействия на связывание антикодона, поскольку третий нуклеотид в кодоне, известный как положение вобуляции, имеет более слабую антикодонную специфичность связывания тРНК, чем первый и второй нуклеотиды. В этой модели структура мотива объясняется тем фактом, что первая и вторая позиции антикодонов должны иметь возможность идеально сочетаться как в 0, так и в -1 кадрах. Следовательно, нуклеотиды 2 и 1 должны быть идентичными, а нуклеотиды 3 и 2 также должны быть идентичными, что приводит к требуемой последовательности из 3 идентичных нуклеотидов для каждой скользящей тРНК.
 +1 сдвиг рамки считывания происходит, когда рибосома и тРНК Р-сайта останавливаются в ожидании прибытия редкой аргининовой тРНК. Кодон A-сайта в новой рамке спаривается с антикодоном более распространенной тРНК глицина, и трансляция продолжается.
+1 сдвиг рамки считывания происходит, когда рибосома и тРНК Р-сайта останавливаются в ожидании прибытия редкой аргининовой тРНК. Кодон A-сайта в новой рамке спаривается с антикодоном более распространенной тРНК глицина, и трансляция продолжается. Скользкая последовательность для сигнала сдвига рамки +1 не имеет такого же мотива, и вместо этого, по-видимому, функционирует путем приостановки рибосомы в последовательности, кодирующей редкую аминокислоту. Рибосомы не транслируют белки с постоянной скоростью, независимо от последовательности. Некоторым кодонам требуется больше времени для трансляции, потому что в цитозоле нет равных количеств тРНК этого конкретного кодона. Из-за этого запаздывания существуют небольшие участки последовательностей кодонов, которые контролируют скорость сдвига рамки рибосом. В частности, рибосома должна остановиться, чтобы дождаться прибытия редкой тРНК, и это увеличивает кинетическую благоприятность рибосомы и связанной с ней тРНК, скользящей в новый каркас. В этой модели изменение рамки считывания вызвано одним проскальзыванием тРНК, а не двумя.
Рибосомный сдвиг рамки считывания может контролироваться механизмами, обнаруженными в последовательности мРНК (цис-действие). Обычно это относится к скользкой последовательности, вторичной структуре РНК или к тому и другому. Сигнал сдвига рамки -1 состоит из обоих элементов, разделенных спейсерной областью, как правило, длиной 5–9 нуклеотидов. Сдвиг рамки также может быть вызван другими молекулами, которые взаимодействуют с рибосомой или мРНК (транс-действующие).
 Это графическое представление сигнала сдвига рамки HIV1. Сдвиг рамки -1 в области скользкой последовательности приводит к трансляции pol вместо области, кодирующей белок gag, или открытой рамки считывания (ORF). Белки gag и pol необходимы для обратной транскриптазы, которая необходима для репликации ВИЧ1.
Это графическое представление сигнала сдвига рамки HIV1. Сдвиг рамки -1 в области скользкой последовательности приводит к трансляции pol вместо области, кодирующей белок gag, или открытой рамки считывания (ORF). Белки gag и pol необходимы для обратной транскриптазы, которая необходима для репликации ВИЧ1. Скользкие последовательности потенциально могут заставить считывающую рибосому «проскальзывать» и пропускать ряд нуклеотидов (обычно только 1) и после этого считывать совершенно другой кадр. При запрограммированном сдвиге рамки рибосомы -1 скользкая последовательность соответствует мотиву X_XXY_YYH, где XXX - любые три идентичных нуклеотида (хотя бывают некоторые исключения), YYY обычно представляет UUU или AAA, а H - A, C или U. В случае + 1 со сдвигом рамки считывания скользкая последовательность содержит кодоны, для которых соответствующая тРНК встречается реже, и сдвиг рамки считывания предпочтителен, поскольку кодон в новой рамке имеет более общую ассоциированную тРНК. Одним из примеров скользкой последовательности является полиА на мРНК, которая, как известно, вызывает проскальзывание рибосом даже в отсутствие каких-либо других элементов.
Эффективный сдвиг рамки рибосом обычно требует наличия вторичной структуры РНК для усиления эффектов скользкой последовательности. Считается, что структура РНК (которая может быть стержневой петлей или псевдоузлом ) приостанавливает рибосому на скользком участке во время трансляции, заставляя ее перемещаться и продолжать репликацию из положения -1. Считается, что это происходит потому, что структура физически блокирует движение рибосомы, застревая в туннеле мРНК рибосомы. Эта модель подтверждается тем фактом, что сила псевдоузла положительно коррелировала с уровнем сдвига рамки для ассоциированной мРНК.
Ниже приведены примеры предполагаемых вторичных структур для элементов сдвига рамки, показанных для стимуляции сдвига рамки у различных организмов. Большинство показанных структур представляют собой стержневые петли, за исключением структуры псевдоузла ALIL (апикальная петля-внутренняя петля). На этих изображениях большие и неполные круги мРНК представляют линейные области. Вторичные структуры «стебель-петля», где «стебли» образованы областью спаривания оснований мРНК с другой областью на той же цепи, показаны выступающими из линейной ДНК. Линейная область сигнала сдвига рамки считывания рибосом ВИЧ содержит высококонсервативную скользящую последовательность UUU UUU A; многие другие предсказанные структуры также содержат кандидатов на скользкие последовательности.
Последовательности мРНК на изображениях можно прочитать в соответствии с набором рекомендаций. Хотя A, T, C и G обозначают конкретный нуклеотид в позиции, есть также буквы, которые обозначают неоднозначность, которые используются, когда в этом положении может встречаться более одного вида нуклеотидов. Правила Международного союза теоретической и прикладной химии ( IUPAC ) следующие:
| Условное обозначение | Описание | Представленные базы | Дополнение | ||||
|---|---|---|---|---|---|---|---|
| А | Денин | А | 1 | Т | |||
| C | C ytosine | C | грамм | ||||
| грамм | G uanine | грамм | C | ||||
| Т | T hymine | Т | А | ||||
| U | U racil | U | А | ||||
| W | W ЕАК | А | Т | 2 | W | ||
| S | S Чонг | C | грамм | S | |||
| M | М ино | А | C | K | |||
| K | K eto | грамм | Т | M | |||
| р | пу R ине | А | грамм | Y | |||
| Y | p Y римидин | C | Т | р | |||
| B | не A ( B идет после A) | C | грамм | Т | 3 | V | |
| D | не C ( D идет после C) | А | грамм | Т | ЧАС | ||
| ЧАС | не G ( H идет после G) | А | C | Т | D | ||
| V | не T ( V идет после T и U) | А | C | грамм | B | ||
| N | любой N ucleotide (не пробел) | А | C | грамм | Т | 4 | N |
| Z | Z ero | 0 | Z | ||||
Эти символы также действительны для РНК, за исключением того, что U (урацил) заменяет T (тимин).
Было обнаружено, что небольшие молекулы, белки и нуклеиновые кислоты стимулируют уровни сдвига рамки. Например, механизм отрицательной обратной связи в пути синтеза полиамина основан на уровнях полиамина, стимулирующих увеличение сдвига рамки на +1, что приводит к выработке ингибирующего фермента. Также было показано, что определенные белки, которые необходимы для распознавания кодонов или которые непосредственно связываются с последовательностью мРНК, модулируют уровни сдвига рамки считывания. Молекулы микроРНК (миРНК) могут гибридизоваться со вторичной структурой РНК и влиять на ее прочность.