| триозофосфат-изомераза | |||||||||
|---|---|---|---|---|---|---|---|---|---|
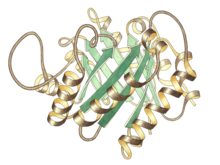 Вид сбоку мономера триозо-P-изомеразы, активный центр вверху в центре Вид сбоку мономера триозо-P-изомеразы, активный центр вверху в центре | |||||||||
| Идентификаторы | |||||||||
| Номер ЕС | 5.3.1.1 | ||||||||
| Номер CAS | 9023 -78-3 | ||||||||
| Базы данных | |||||||||
| IntEnz | Представление IntEnz | ||||||||
| BRENDA | Запись BRENDA | ||||||||
| ExPASy | Представление NiceZyme | ||||||||
| KEGG | Запись KEGG | ||||||||
| MetaCyc | метаболический путь | ||||||||
| PRIAM | профиль | ||||||||
| PDB структуры | RCSB PDB PDBe PDBsum | ||||||||
| Онтология гена | AmiGO / QuickGO | ||||||||
| |||||||||
Триозофосфатизомераза (TPI или TIM ) представляет собой фермент (EC 5.3.1.1 ), который катализирует обратимое взаимное превращение триоза фосфата изомеры дигидроксиацетонфосфат и D- глицеральд гид-3-фосфат.
| дигидроксиацетонфосфат | триозофосфат-изомераза | D-глицеральдегид-3-фосфат | |
 |  | ||
 | |||
| триозофосфат-изомераза | |||
соединение C00111 в базе данных пути KEGG Фермент 5.3.1.1 в KEGG База данных путей. Соединение C00118 в KEGG База данных путей.
TPI играет важную роль в гликолизе и необходим для эффективного производства энергии. TPI был обнаружен почти во всех организмах, в которых проводился поиск фермента, включая животных, таких как млекопитающие и насекомые, а также в грибах, растениях и бактерии. Однако у некоторых бактерий, не осуществляющих гликолиз, таких как уреаплазма, отсутствует TPI.
У людей дефицит TPI связан с прогрессирующим тяжелым неврологическим расстройством, называемым дефицитом триозофосфатизомеразы. Дефицит триозофосфат-изомеразы характеризуется хронической гемолитической анемией. Хотя существуют различные мутации, вызывающие это заболевание, большинство из них включает мутацию глутаминовой кислоты в положении 104 в аспарагиновую кислоту.
Триозофосфат-изомераза является высокоэффективным ферментом, выполняющим миллиарды реакций раз быстрее, чем это происходило бы в растворе. Реакция настолько эффективна, что считается каталитически совершенной : она ограничена только скоростью, с которой субстрат может диффундировать в активный центр фермента и из него.
Механизм включает промежуточное образование "эндиола «. Относительная свободная энергия каждого основного состояния и переходного состояния была определена экспериментально и показана на рисунке.

Структура TPI облегчает преобразование между дигидроксиацетонфосфатом (DHAP) и глицеральдегид-3-фосфатом (GAP). Остаток нуклеофильного глутамата 165 TPI депротонирует субстрат, а электрофильный остаток гистидина 95 отдает протон с образованием промежуточного эндиола. При депротонировании ендиолат затем коллапсирует и, отрывая протон от протонированного глутамата 165, образует продукт GAP. Катализ обратной реакции протекает аналогично, образуя тот же ендиол, но с коллапсом ендиолата из кислорода при C2.
TPI ограничен диффузией. С точки зрения термодинамики, образование DHAP в соотношении 20: 1 предпочтительнее образования GAP. Однако при гликолизе использование GAP на последующих этапах метаболизма вызывает реакцию, направленную на его производство. TPI ингибируется ионами сульфата, фосфата и арсената, которые связываются с активным центром. Другие ингибиторы включают 2-фосфогликолят, аналог переходного состояния, и D-глицерин-1-фосфат, аналог субстрата.
 Вид сбоку димера триозофосфатизомеразы.
Вид сбоку димера триозофосфатизомеразы. | Триозофосфатизомераза | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Идентификаторы | |||||||||
| Символ | TIM | ||||||||
| Pfam | PF00121 | ||||||||
| Pfam клан | CL0036 | ||||||||
| InterPro | IPR000652 | ||||||||
| ПРОФИЛЬ | PDOC00155 | ||||||||
| SCOPe | 1tph / SUPFAM | ||||||||
| |||||||||
Триозофосфатизомераза представляет собой димер идентичных субъединиц, каждая из которых состоит примерно из 250 аминокислотных остатков. Трехмерная структура субъединицы содержит восемь α-спиралей снаружи и восемь параллельных β-тяжей внутри. На иллюстрации ленточный остов каждой субъединицы окрашен от синего до красного от N-конца к C-концу. Этот структурный мотив называется αβ-стволом или TIM-стволом, и на сегодняшний день он является наиболее часто наблюдаемой белковой складкой. активный сайт этого фермента находится в центре цилиндра. Остаток глутаминовой кислоты и гистидин участвуют в каталитическом механизме. Последовательность вокруг остатков активного сайта сохраняется во всех известных триозофосфат-изомеразах.
Структура триозофосфатизомеразы способствует ее функции. Помимо точно размещенных остатков глутамата и гистидина для образования эндиола, цепь TPI из десяти или одиннадцати аминокислот действует как петля для стабилизации промежуточного продукта. Петля, образованная остатками с 166 по 176, замыкается и образует водородную связь с фосфатной группой субстрата. Это действие стабилизирует промежуточное соединение эндиола и другие переходные состояния на пути реакции.
В дополнение к тому, что реакция становится кинетически возможной, петля TPI изолирует реакционноспособный промежуточный эндиол, чтобы предотвратить разложение до метилглиоксаль и неорганический фосфат. Водородная связь между ферментом и фосфатной группой субстрата делает такое разложение стереоэлектронно невыгодным. Метилглиоксаль является токсином и, если он образуется, удаляется через систему глиоксалазы. Потеря высокоэнергетической фосфатной связи и субстрата для остальной части гликолиза делает образование метилглиоксаля неэффективным.
Исследования показывают, что лизин, расположенный рядом с активным центром (в положении 12), также имеет решающее значение для функции фермента. Лизин, протонированный при физиологическом pH, может помочь нейтрализовать отрицательный заряд фосфатной группы. Когда этот лизин превращается в нейтральную аминокислоту, TPI теряет все функции, но мутанты с другой положительно заряженной аминокислотой сохраняют некоторую функцию.
.