 Это изображение описывает последнюю стадию митоза, телофазу.
Это изображение описывает последнюю стадию митоза, телофазу. 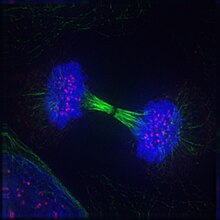 Флуоресцентная микрофотография человеческой клетки в телофазе, показывающая хромосомы (ДНК) в синий, микротрубочки зеленого цвета и кинетохоры розового
Флуоресцентная микрофотография человеческой клетки в телофазе, показывающая хромосомы (ДНК) в синий, микротрубочки зеленого цвета и кинетохоры розового Телофаза (от греческого τέλος (телос), «конец» и φάσις (фазис), «стадия») является заключительной стадией в обоих мейоз и митоз в эукариотической клетке. Во время телофазы эффекты профазы и прометафазы (разрушение ядрышка и ядерной мембраны) меняются местами. Когда хромосомы достигают полюсов клетки, ядерная оболочка повторно собирается вокруг каждого набора хроматид, снова появляются ядрышки и хромосомы начинают деконденсироваться обратно в расширенный хроматин, который присутствует во время интерфазы. митотическое веретено разбирается, а оставшиеся веретено микротрубочки деполимеризуются. Телофаза составляет примерно 2% от продолжительности клеточного цикла .
Цитокинез обычно начинается до поздней телофазы и по завершении разделяет два дочерних ядра между парой отдельных дочерних клеток.
Телофаза в основном управляется дефосфорилированием митотических циклин-зависимых киназ (Cdk) субстратов.
фосфорилирование белков-мишеней M-Cdks (митотических циклин-зависимых киназ) управляет сборкой веретена, конденсацией хромосом и разрушением ядерной оболочки в раннем митозе. Дефосфорилирование тех же субстратов вызывает разборку веретена, деконденсацию хромосом и реформацию дочерних ядер в телофазе. Установление степени дефосфорилирования, допускающего телофазные события, требует как инактивации Cdks, так и активации фосфатаз.
. Инактивация Cdk в первую очередь является результатом разрушения связанного с ним циклина. Циклины нацелены на протеолитическую деградацию с помощью комплекса, стимулирующего анафазу (APC), также известного как циклосома, убиквитин-лигаза. Активный CDC20 -связанный APC (APC / C) нацелен на митотические циклины для деградации, начиная с анафазы. Экспериментальное добавление нерасщепляемого М-циклина к клеткам вызывает остановку клеточного цикла в пост-анафазном / пре-телофазном состоянии с конденсированными хромосомами, сегрегированными по полюсам клеток, неповрежденным митотическим веретеном и отсутствием реформации ядерной оболочки. Это было показано на яйцах лягушек (Xenopus ), плодовых мушках (Drosophilla melanogaster ), почковании (Saccharomyces cerevisiae ) и делении (Schizosaccharomyces pombe ) дрожжей и в нескольких линиях клеток человека.
Требование активации фосфатазы можно увидеть у почкующихся дрожжей, которые не имеют избыточных фосфатаз для выхода из митоза и полагаются на фосфатазу cdc14. Блокирование активации cdc14 в этих клетках приводит к той же фенотипической остановке, что и блокирование деградации М-циклина.
Исторически считалось, что анафаза и телофаза - это события, которые происходят пассивно после удовлетворения веретена. Контрольная точка сборки (SAC), которая определяет переход метафаза-анафаза. Однако существование дифференциальных фаз для активности cdc14 между анафазой и телофазой наводит на мысль о дополнительных, неисследованных поздних контрольных точках митоза. Cdc14 активируется путем его высвобождения в ядро, секвестрации в ядрышке и последующего экспорта в цитоплазму. Путь раннего высвобождения анафазы Cdc-14, который стабилизирует веретено, также высвобождает cdc14 из ядрышка, но ограничивает его ядром. Полное высвобождение и поддерживаемая активация cdc14 достигается отдельным путем Mitotic Exit Network (MEN) в достаточной степени (для запуска разборки веретена и сборки ядерной оболочки) только после поздней анафазы.
Cdc14-опосредованное дефосфорилирование активируется нижестоящие регуляторные процессы, уникальные для телофазы. Например, дефосфорилирование CDH1 позволяет APC / C связывать CDH1. APC / C нацеливается на CDC20 для протеолиза, что приводит к переключению клеток с активности APC / C на активность APC / C. Убиквитинирование митотических циклинов продолжается вместе с APC / C-специфическими мишенями, такими как компонент митотического веретена дрожжей, Ase1 и cdc5, деградация которых требуется для возврата клеток в фазу G1.
Сдвиг в профиле цельноклеточных фосфопротеинов - это только самый широкий из многих регуляторных механизмов, способствующих возникновению отдельных телофазных событий.
 Стадии поздней М фазы в клетке позвоночных
Стадии поздней М фазы в клетке позвоночных Разрушение митотического веретена является общим для завершения митоза у всех эукариот и является событием, наиболее часто используемым для определения перехода от анафазы-B к телофазе, хотя инициация повторной сборки ядра имеет тенденцию предшествовать разборке веретена.
Разборка веретена - это необратимый процесс, который должен влиять не на окончательную деградацию, а на реорганизацию составляющих микротрубочек; микротрубочки отделяются от кинетохор и полюсных тел веретена и возвращаются в свои межфазные состояния.
Деполимеризация шпинделя во время телофазы происходит с положительного конца и, таким образом, является обращением сборки шпинделя. Последующая сборка массива микротрубочек, в отличие от сборки поляризованного веретена, является интерполярной. Это особенно очевидно в клетках животных, которые должны немедленно, после разборки митотического веретена, установить антипараллельный пучок микротрубочек, известный как центральное веретено, чтобы регулировать цитокинез. АТФаза p97 необходима для создания относительно стабильных и длинных интерфазных массивов микротрубочек после разборки высокодинамичных и относительно коротких митотических микротрубочек.
Сборка веретена хорошо изучена и охарактеризована как процесс, в котором предварительные структуры назначаются SAC, молекулярная основа разборки веретена не понимается в сопоставимых деталях. Поздний митотический каскад дефосфорилирования субстратов M-Cdk посредством MEN широко считается ответственным за разборку веретена. Состояния фосфорилирования стабилизирующих и дестабилизирующих факторов микротрубочек, а также нуклеаторов микротрубочек являются ключевыми регуляторами их активности. Например, NuMA представляет собой сшивающий белок на минус-конце и субстрат Cdk, диссоциация которого от микротрубочек происходит за счет его дефосфорилирования во время телофазы.
Общая модель разборки веретена у дрожжей состоит в том, что три функционально перекрывающихся подпроцесса веретена разъединение, дестабилизация и деполимеризация в первую очередь осуществляются APC / C, киназами, специфичными для стабилизации микротрубочек, и деполимеразами микротрубочек, направленными на плюс-конец, соответственно. Известно, что эти эффекторы высоко консервативны у дрожжей и высших эукариот. APC / C нацелен на сшивание белков, связанных с микротрубочками (NuMA, Ase1, Cin1 и др.). AuroraB (дрожжевой IpI1) фосфорилирует связанный с веретено стабилизирующий белок EB1 (дрожжевой Bim1), который затем отделяется от микротрубочек, и дестабилизатор She1, который затем связывается с микротрубочками. Кинезин8 (дрожжевой Kip3), АТФ-зависимая деполимераза, ускоряет деполимеризацию микротрубочек на положительном конце. Было показано, что одновременное нарушение этих механизмов, но не любого из них, приводит к резкой гиперстабильности веретена во время телофазы, что свидетельствует о функциональном перекрытии, несмотря на разнообразие механизмов.
Основными компонентами ядерной оболочки являются двойная мембрана, комплексы ядерных пор и ядерная пластинка, расположенная внутри внутренней ядерной мембраны. Эти компоненты разбираются во время профазы и прометафазы и реконструируются во время телофазы, когда ядерная оболочка восстанавливается на поверхности разделенных сестринских хроматид. Ядерная мембрана фрагментируется и частично абсорбируется эндоплазматическим ретикулумом во время прометафазы, а нацеливание ER везикул, содержащих белок внутренней ядерной мембраны, на хроматин происходит во время телофазы в обратном направлении этого процесса.. Мембранообразующие везикулы агрегируются непосредственно на поверхности хроматина, где они сливаются латерально в непрерывную мембрану.
Ran-GTP необходим для ранней сборки ядерной оболочки на поверхности хромосом: он высвобождает компоненты оболочки, секвестрированные импортином β во время раннего митоза. Ran-GTP локализуется рядом с хромосомами на протяжении митоза, но не запускает диссоциацию белков ядерной оболочки от importin β до тех пор, пока мишени M-Cdk не дефосфорилируются в телофазе. Эти компоненты оболочки включают несколько компонентов ядерных пор, наиболее изученным из которых является каркасный белок ядерных пор ELYS, который может распознавать участки ДНК, богатые парами оснований A: T (in vitro), и поэтому может напрямую связываться к ДНК. Однако эксперименты с экстрактами яиц Xenopus пришли к выводу, что ELYS не может связываться с голой ДНК и связывает только димеры и нуклеосомы гистонов напрямую. После связывания с хроматином ELYS рекрутирует другие компоненты каркаса ядерных пор и трансмембранные белки ядерных пор. Комплекс ядерной поры собирается и интегрируется в ядерную оболочку организованным образом, последовательно добавляя Nup107-160, POM121 и FG Nups.
Спорный механизм ядерной мембраны повторная сборка включает начальную сборку ядерных пор и последующее рекрутирование мембранных везикул вокруг пор или, если ядерная оболочка формируется в основном из протяженных цистерн ER, предшествующих сборке ядерных пор:
Оболочка сглаживается и расширяется после того, как она охватывает целое. хроматидный набор. Это, вероятно, происходит из-за импорта в ядерные поры ламина, который может удерживаться внутри сплошной мембраны. Ядерные оболочки экстрактов яиц Xenopus не смогли сгладиться, когда ядерный импорт ламина был ингибирован, оставаясь морщинистыми и тесно связанными с конденсированными хромосомами. Однако в случае латеральной экспансии ER ядерный импорт инициируется до завершения повторной сборки ядерной оболочки, что приводит к временному внутриядерному градиенту белка между дистальным и медиальным аспектами формирующегося ядра.
Субъединицы ламина. разобранные в профазе, инактивируются и секвестрируются во время митоза. Повторная сборка ламината запускается дефосфорилированием ламина (и дополнительно метил- этерификацией остатков COOH на ламине-B ). Ламин-B может воздействовать на хроматин уже в середине анафазы. Во время телофазы, когда ядерный импорт восстанавливается, ламин-A входит в ядро реформирования, но продолжает медленно собираться в периферическую пластинку в течение нескольких часов на протяжении фазы G1.
Экстракты яиц Xenopus и Линии раковых клеток человека были основными моделями, используемыми для изучения повторной сборки ядерной оболочки.
Дрожжи не имеют ламинов; их ядерная оболочка остается неповрежденной на протяжении митоза, а ядерное деление происходит во время цитокинеза.
Деконденсация хромосомы (также известная как релаксация или деконденсация) в расширенный хроматин необходима для возобновления клеткой межфазных процессов, и происходит параллельно со сборкой ядерной оболочки во время телофазы у многих эукариот. Опосредованное MEN дефосфорилирование Cdk необходимо для деконденсации хромосом.
У позвоночных деконденсация хромосом начинается только после восстановления ядерного импорта. Если транспорт ламина через ядерные поры предотвращается, хромосомы остаются конденсированными после цитокинеза, и клетки не могут повторно войти в следующую S-фазу. У млекопитающих лицензирование ДНК для S фазы (ассоциация хроматина с множеством белковых факторов, необходимых для его репликации) также происходит одновременно со созреванием ядерной оболочки во время поздней телофазы. Это может быть связано с восстановлением механизма ядерного импорта интерфазных ядерных и цитоплазматических белков во время телофазы.