| Ядерная пора | |
|---|---|
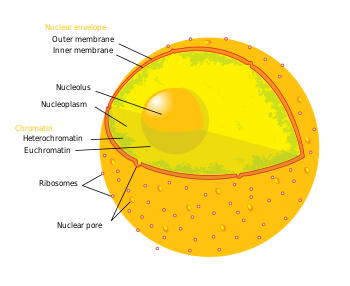 Схема ядра клетки человека. Ядерная пора обозначена слева внизу Схема ядра клетки человека. Ядерная пора обозначена слева внизу | |
 Ядерная пора. Вид сбоку. 1. Ядерная оболочка. 2. Наружное кольцо. 3. Спицы. 4. Корзина. 5. Нити. (Рисунок основан на изображениях, полученных с помощью электронной микроскопии) Ядерная пора. Вид сбоку. 1. Ядерная оболочка. 2. Наружное кольцо. 3. Спицы. 4. Корзина. 5. Нити. (Рисунок основан на изображениях, полученных с помощью электронной микроскопии) | |
| Подробности | |
| Идентификаторы | |
| латинский | Порус ядерный |
| MeSH | D022022 |
| TH | H1.00.01.2.01005 |
| FMA | 63148 |
| Анатомическая терминология [ редактировать в Викиданных ] | |
Ядерные пор является частью большого комплекса белков, известным как поровый комплекс ядерным, который охватывает ядерную оболочку, которая является двойной мембраной, окружающей эукариотического ядро клетки. В ядерной оболочке клетки позвоночного имеется около 1000 комплексов ядерных пор (NPC), но это зависит от типа клетки и стадии жизненного цикла. Комплекс ядерных пор человека (hNPC) имеет структуру 110 мегадальтон (МДа). Белки, составляющие комплекс ядерных пор, известны как нуклеопорины ; каждый NPC содержит по крайней мере 456 отдельных белковых молекул и состоит из 34 различных белков нуклеопоринов. Около половины нуклеопоринов обычно содержат соленоидные белковые домены - либо альфа-соленоид, либо бета-пропеллерную складку, или в некоторых случаях оба как отдельные структурные домены. Другая половина демонстрирует структурные характеристики, типичные для «естественно развернутых» или внутренне неупорядоченных белков, то есть они являются очень гибкими белками, у которых отсутствует упорядоченная третичная структура. Эти неупорядоченные белки являются FG нуклеопориными, так называемой, потому что их аминокислотная последовательность содержит много фенилаланина - глицин повторы.
Комплексы ядерных пор позволяют транспортировать молекулы через ядерную оболочку. Этот транспорт включает РНК и рибосомные белки, перемещающиеся из ядра в цитоплазму, и белки (такие как ДНК-полимераза и ламины ), углеводы, сигнальные молекулы и липиды, перемещающиеся в ядро. Примечательно, что комплекс ядерных пор (NPC) может активно проводить 1000 транслокаций за комплекс в секунду. Хотя более мелкие молекулы просто диффундируют через поры, более крупные молекулы могут распознаваться с помощью определенных сигнальных последовательностей, а затем диффундировать с помощью нуклеопоринов в ядро или из него. Недавно было показано, что эти нуклеопорины обладают специфическими эволюционно консервативными особенностями, закодированными в их последовательностях, которые дают представление о том, как они регулируют транспорт молекул через ядерную пору. Нуклеопорин-опосредованный транспорт напрямую не требует энергии, но зависит от градиентов концентрации, связанных с циклом RAN. Каждая из восьми белковых субъединиц, окружающих настоящую пору (внешнее кольцо), проецирует белок в форме спицы над каналом поры. Часто кажется, что центр поры содержит структуру, похожую на пробку. Пока неизвестно, соответствует ли это реальной пробке или это просто груз, пойманный в пути.
У позвоночных весь комплекс ядерных пор имеет диаметр около 120 нанометров. Диаметр канала колеблется от 5,2 нм у человека до 10,7 нм у лягушки Xenopus laevis, а его глубина составляет примерно 45 нм. мРНК, которая является одноцепочечной, имеет толщину примерно от 0,5 до 1 нм. Молекулярная масса от NPC млекопитающих составляет около 124 megadaltons (МД) и она содержит около 30 различных белковых компонентов, каждый из которых в большом количестве копий. Напротив, дрожжи Saccharomyces cerevisiae меньше по размеру и имеют массу всего 66 МДа.
 Цикл Ран-ГТФ, ядерный импорт и ядерный экспорт
Цикл Ран-ГТФ, ядерный импорт и ядерный экспорт  Ядерные поры, пластинка и хроматин
Ядерные поры, пластинка и хроматин Мелкие частицы (до 30–60 кДа ) способны проходить через комплекс ядерных пор путем пассивной диффузии. Более крупные частицы также способны пассивно диффундировать через поры большого диаметра со скоростью, которая постепенно уменьшается с молекулярной массой. Для эффективного прохождения через комплекс требуются несколько белковых факторов и, в частности, ядерные транспортные рецепторы, которые связываются с молекулами груза и опосредуют их перемещение через NPC либо в ядро ( импортины ), либо из него ( экспортины ). Самым большим семейством ядерных транспортных рецепторов являются кариоферины, включающие десятки импортинов и экспортинов; это семейство далее подразделяется на подсемейства кариоферин-α и кариоферин-β. Другие рецепторы ядерного транспорта включают NTF2 и некоторые NTF2-подобные белки.
Для объяснения механизма транслокации были предложены три модели:
Любой груз с обнаруженным сигналом ядерной локализации (NLS) будет предназначен для быстрой и эффективной транспортировки через поры. Известно несколько последовательностей NLS, обычно содержащих консервативную последовательность с основными остатками, такими как PKKKRKV. Любой материал с NLS будет приниматься импортинами в ядро.
Классическая схема импорта NLS-белка начинается с первого связывания импортина-α с последовательностью NLS, которая затем действует как мост для прикрепления импортина-β. Комплекс импортинβ-импортинα-груз затем направляется к ядерной поре и диффундирует через нее. Как только комплекс оказывается в ядре, RanGTP связывается с Importin-β и вытесняет его из комплекса. Затем клеточный белок предрасположенности к апоптозу (CAS), экспортин, который в ядре связан с RanGTP, вытесняет Importin-α из груза. Таким образом, белок NLS свободен в нуклеоплазме. Комплекс Importinβ-RanGTP и Importinα-CAS-RanGTP диффундирует обратно в цитоплазму, где GTP гидролизуются до GDP, что приводит к высвобождению импортинаβ и Importinα, которые становятся доступными для нового раунда импорта NLS-белка.
Хотя груз проходит через пору с помощью белков-шаперонов, перемещение через пору не зависит от энергии. Однако весь цикл импорта требует гидролиза 2 ГТФ и, таким образом, зависит от энергии и должен рассматриваться как активный транспорт. Цикл импорта приводится в действие нуклео-цитоплазматическим градиентом RanGTP. Этот градиент возникает из-за исключительной ядерной локализации RanGEFs, белков, которые обменивают GDP на GTP на молекулах Ran. Таким образом, в ядре наблюдается повышенная концентрация RanGTP по сравнению с цитоплазмой.
Некоторые молекулы или макромолекулярные комплексы необходимо экспортировать из ядра в цитоплазму, как и субъединицы рибосом и информационные РНК. Таким образом, существует механизм экспорта, аналогичный механизму импорта.
В классической схеме экспорта белки с ядерной экспортной последовательностью (NES) могут связываться в ядре с образованием гетеротримерного комплекса с экспортином и RanGTP (например, экспортином CRM1). Затем комплекс может диффундировать в цитоплазму, где гидролизуется GTP и высвобождается NES-белок. CRM1-RanGDP распространяется обратно в ядро, где GDP обменивается на GTP с помощью RanGEF. Этот процесс также зависит от энергии, поскольку он потребляет один GTP. Экспорт с помощью exportin CRM1 может подавляться лептомицином B.
Существуют разные пути экспорта через NPC для каждого существующего класса РНК. Экспорт РНК также опосредуется сигналом (NES); NES находится в РНК-связывающих белках (за исключением тРНК, у которой нет адаптера). Примечательно, что все вирусные РНК и клеточные РНК ( тРНК, рРНК, U-мяРНК, микроРНК ), за исключением мРНК, зависят от RanGTP. Консервированные факторы экспорта мРНК необходимы для ядерного экспорта мРНК. Факторами экспорта являются Mex67 / Tap (большая субъединица) и Mtr2 / p15 (малая субъединица). Считается, что у высших эукариот экспорт мРНК зависит от сплайсинга, который, в свою очередь, привлекает белковый комплекс TREX к сплайсированным сообщениям. TREX функционирует как адаптер для TAP, который является очень плохим связывающим РНК белком. Однако существуют альтернативные пути экспорта мРНК, которые не зависят от сплайсинга для специализированных сообщений, таких как гистоны. Недавние работы также подтверждают взаимодействие между зависимым от сплайсинга экспортом и одним из этих альтернативных путей экспорта мРНК для секреторных и митохондриальных транскриптов.
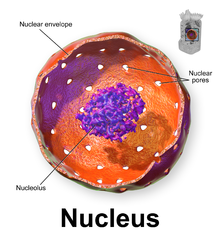 Ядро клетки с порами.
Ядро клетки с порами. Поскольку NPC контролирует доступ к геному, важно, чтобы он существовал в больших количествах на стадиях клеточного цикла, где необходима большая транскрипция. Например, циклически повторяющиеся клетки млекопитающих и дрожжей удваивают количество NPC в ядре между фазами G1 и G2 клеточного цикла, а ооциты накапливают большое количество NPC, чтобы подготовиться к быстрому митозу, который существует на ранних стадиях развития. Межфазные клетки также должны поддерживать уровень генерации NPC, чтобы поддерживать постоянный уровень NPC в клетке, поскольку некоторые из них могут быть повреждены. Некоторые клетки могут даже увеличивать количество NPC из-за повышенной потребности в транскрипции.
Есть несколько теорий относительно того, как собираются NPC. Поскольку иммунное истощение определенных белковых комплексов, таких как комплекс Nup 107–160, приводит к образованию беспористых ядер, кажется вероятным, что комплексы Nup участвуют в слиянии внешней мембраны ядерной оболочки с внутренней, а не то, что сплавление мембраны начинает образование поры. Есть несколько способов, которыми это может привести к формированию полноценного NPC.
Во время митоза NPC, кажется, разбирается поэтапно. Периферические нуклеопорины, такие как Nup 153, Nup 98 и Nup 214, отделяются от NPC. Остальные, которые можно рассматривать как каркасные белки, остаются стабильными в виде комплексов цилиндрических колец внутри ядерной оболочки. Эта разборка периферических групп NPC в значительной степени считается управляемой фосфатом, поскольку некоторые из этих нуклеопоринов фосфорилируются на стадиях митоза. Однако фермент, участвующий в фосфорилировании, in vivo неизвестен. У многоклеточных животных (которые претерпевают открытый митоз) NE быстро деградирует после потери периферических Nups. Причина этого может быть связана с изменением архитектуры NPC. Это изменение может сделать NPC более проницаемым для ферментов, участвующих в деградации NE, таких как цитоплазматический тубулин, а также сделать возможным проникновение ключевых белков-регуляторов митоза. У организмов, которые претерпевают полуоткрытый митоз, таких как мицелиальный гриб Aspergillus nidulans, 14 из 30 нуклеопоринов отделяются от основной структуры каркаса за счет активации киназ NIMA и Cdk1, которые фосфорилируют нуклеопорины и открывают ядерные поры, тем самым расширяя ядерная пора и позволяет входить митотическим регуляторам.
Было показано, что у грибов, которые претерпевают закрытый митоз (где ядро не разбирается), изменение барьера проницаемости NE происходит из-за изменений внутри NPC и это то, что позволяет входить митотическим регуляторам. В Aspergillus nidulans на состав NPC, по-видимому, влияет митотическая киназа NIMA, возможно, за счет фосфорилирования нуклеопоринов Nup98 и Gle2 / Rae1. Это ремоделирование, по-видимому, позволяет белковому комплексу cdc2 / cyclinB проникать в ядро, а также многим другим белкам, таким как растворимый тубулин. Каркас NPC остается неповрежденным на протяжении всего закрытого митоза. Похоже, что это сохраняет целостность NE.