 . Ион метапериодата . Ион метапериодата | |
 . Ион ортопериодата . Ион ортопериодата | |
| Имена | |
|---|---|
| Систематическое название IUPAC тетраоксойодат ( 1-). гексаоксойодат (5-) | |
| Идентификаторы | |
| Номер CAS |
|
| 3D-модель (JSmol ) |
|
| ChemSpider | |
| PubChem CID | |
| UNII |
|
InChI
| |
УЛЫБКИ
| |
| Свойства | |
| Химическая формула | IO4или IO 6 |
| Конъюгат кислота | Периодическая кислота |
| Родственные соединения | |
| Другие анионы | Перхлорат. Пербромат. Перманганат |
| Если не указано иное, данные для материалов приведены в их стандарте состояние (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на информационное окно | |
Periodate - это анион состоит из йода и кислорода. Он является одним из ряда оксианионов йода и является самым высоким в ряду, причем йод существует в степени окисления +7. В отличие от других пергалогенатов, таких как перхлорат, он может существовать в двух формах: метапериодат IO. 4и ортопериодат IO. 6. В этом отношении он сопоставим с ионом теллурата из соседней группы группы. Он может объединяться с рядом противоионов с образованием периодатов, которые также можно рассматривать как соли периодической кислоты.
Периодаты были обнаружены Генрихом Густав Магнус и К.Ф. Аммермюллер; кто первым синтезировал периодную кислоту в 1833 году.
Классически периодат чаще всего производился в форме гидроперидата натрия (Na 3H2IO6). Он коммерчески доступен, но также может быть получен окислением йодатов с помощью хлора и гидроксида натрия. Или, аналогично, из иодидов окислением бромом и гидроксидом натрия:
Современное промышленное производство включает электрохимическое окисление йодатов на аноде PbO 2 со следующим стандартным электродным потенциалом :
Метапериодаты являются обычно получают путем дегидратации гидропериодата натрия с помощью азотной кислоты или путем дегидратации ортопериодной кислоты путем ее нагревания до 100 ° C в вакууме.
Их также можно получить непосредственно из иодатов путем обработки другими сильными окислителями, такими как гипохлориты :
Периодат может существовать в различных формах в водной среде, при этом pH является контролирующим фактором. Ортопериодат имеет ряд констант кислотной диссоциации.
| H5IO6 | ⇌ | H. 4IO. 6 | + H pK a = 3,29 |
| H. 4IO. 6 | ⇌ | H. 3IO. 6 | + H pK a = 8,31 |
| H. 3IO. 6 | ⇌ | H. 2IO. 6 | + H pK a = 11.60 |
Орто- и метапериодатные формы также существуют в равновесии.
По этой причине ортопериодат иногда называют ди гидратом метапериодата, обозначаемым IO. 4· 2H 2 O; однако это описание не является строго точным, поскольку рентгеновская кристаллография H 5IO6показывает 5 эквивалентных групп I – OH.
При экстремальных значениях pH могут образовываться дополнительные частицы. В основных условиях может происходить реакция дегидратации с образованием дипериодата (иногда называемого мезопериодатом).
В сильнокислых условиях периодическая кислота может протонироваться с образованием катиона.
Как в орто-, так и в метапериодате йод гипервалентен, поскольку он образует больше облигаций, чем обычно допускается. Это было объяснено с помощью дативных связей, подтверждающих отсутствие двойной связи в этих молекулах.
Точные структуры различаются в зависимости от противоионов, однако в среднем ортопериодаты принимают слегка деформированную октаэдрическую геометрию. с дифракцией рентгеновских лучей, показывающей длину связи I – O 1,89 Å. Метапериодаты имеют искаженную тетраэдрическую геометрию со средним расстоянием I – O 1,78 Å.
Периодаты могут расщеплять углерод-углеродные связи на различных участках., 2-дифункциональные алканы. Наиболее распространенным примером этого является расщепление диола, которое также было обнаружено первым (реакция Малапрада ). Помимо диолов, периодаты могут расщеплять 1,2-гидроксикетоны, 1,2-дикетоны, α-кетокислоты, α-гидроксикислоты, аминокислоты, 1,2-аминоспирты, 1,2-диамины и эпоксиды с образованием альдегидов, кетонов и карбоновых кислот.

Алкены также могут окисляться и расщепляться при окислении Лемье – Джонсона. При этом используется каталитическая загрузка тетроксида осмия, который регенерируется in situ периодатом. Общий процесс эквивалентен процессу озонолиза.
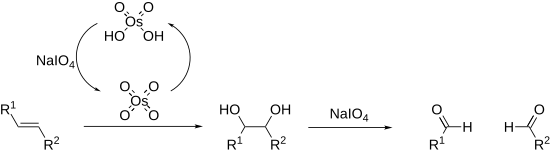
Реакции расщепления протекают через циклический промежуточный продукт, называемый сложным эфиром периодата. На его образование могут влиять pH и температура, но наиболее сильно на него влияет геометрия субстрата, при этом цис -диолы реагируют значительно быстрее, чем транс -диолы. Реакции экзотермические и обычно проводятся при 0 ° C. Поскольку соли периодата легко растворимы в воде, реакции обычно проводят в водной среде. Если растворимость является проблемой, может использоваться периодическая кислота, так как она растворима в спиртах; катализаторы межфазного переноса также эффективны в двухфазных реакционных смесях. В крайних случаях периодат можно заменить на тетраацетат свинца, который реагирует аналогичным образом и растворим в органических растворителях (окисление Криджи ).

Расщепление периодатом часто используется в молекулярной биохимии с целью модификации сахаридных колец, поскольку многие пяти- и шестичленные сахара содержат вицинальные диолы. Исторически его также использовали для определения структуры моносахаридов.
Расщепление периодатом может быть выполнено в промышленных масштабах с образованием диальдегидного крахмала, который используется в производстве бумаги.
Периодаты - сильные окислители. Они могут окислять катехол до 1,2-бензохинон и гидрохинон до 1,4-бензохинон. Сульфиды может быть эффективно окислен до сульфоксидов. Периодаты обладают достаточной эффективностью для образования других сильных неорганических окислителей, таких как перманганат, четырехокись осмия и четырехокись рутения.
Периодаты являются высокоселективными травителями для некоторых оксидов на основе рутения.
Некоторые окрашивающие агенты, используемые в микроскопии, основаны на периодате (например, периодическая кислота – Шифф Пятно и пятно Джонса )
Периодаты также использовались в качестве окислителей для использования в пиротехнике. В 2013 году Армия США объявила, что заменит экологически вредные химические вещества нитрат бария и перхлорат калия с метапериодатом натрия для использования в их трассирующих боеприпасах.
Периодат является частью ряда оксианионов, в которых йод может принимать степени окисления, равные -1, +1, +3, +5 или +7. Число нейтральных также известны оксиды йода.
| Стат. окисления йода e | −1 | +1 | +3 | +5 | +7 |
|---|---|---|---|---|---|
| Имя | йодид | гипойодит | йодит | йодат | периодат |
| Формула | I | IO | IO. 2 | IO. 3 | IO. 4или IO. 6 |
| Структура |  |