Палладийорганический химия - это раздел металлоорганической химии, имеющий дело с органическим палладием соединения и их реакции. Палладий часто используется в качестве катализатора при восстановлении алкенов и алкинов с помощью водорода. Этот процесс включает образование ковалентной связи палладий-углерод . Палладий также играет важную роль в реакциях сочетания углерод-углерод , как показано в тандемных реакциях.
 Образец PdCl 2 (1,5-циклооктадиен).
Образец PdCl 2 (1,5-циклооктадиен).В отличие от Ni (II), но аналогичен Pt (II), Pd ( II) галогениды образуют множество алкеновых комплексов. Первым примером является дихлор (1,5-циклооктадиен) палладий. В этом комплексе диен легко замещается, что делает его предпочтительным предшественником катализаторов. В промышленно важном процессе Wacker этилен превращается в ацетальдегид посредством нуклеофильной атаки гидроксида на промежуточное соединение Pd (II) -этилен с последующим образованием комплекса винилового спирта. Фуллереновые лиганды также связываются с палладием (II).
 Каталитический цикл для промышленно значимого процесса Wacker для окисления этилена до ацетальдегида.
Каталитический цикл для промышленно значимого процесса Wacker для окисления этилена до ацетальдегида. Ацетат палладия (II) и родственные соединения являются общими реагентами, поскольку карбоксилаты являются хорошими уходящими группами с основными свойствами. Например, было продемонстрировано, что трифторацетат палладия эффективен при ароматическом декарбоксилировании :
Знаковым комплексом в этой серии является димер хлорида аллилпалладия (APC). Аллильные соединения с подходящими уходящими группами реагируют с солями палладия (II) с образованием пи-аллильных комплексов, имеющих тактильность 3. Эти промежуточные соединения также реагируют с нуклеофилами, например, карбанионы, полученные из малонатов или с аминами при аллильном аминировании, как показано ниже.

Промежуточные соединения аллилпалладия также присутствуют в Асимметричное аллильное алкилирование Троста и перегруппировка Кэрролла и оксовариант в окислении Саэгуса.
Различные органические группы могут связываться в палладий и образуют стабильные сигма-связанные комплексы. Стабильность связей с точки зрения энергии диссоциации связи следует тенденции: Pd-Alkynyl>Pd-Vinyl ≈ Pd-Aryl>Pd-Alkyl, и длина связи металл-углерод изменяется в противоположном направлении: Pd-Alkynyl < Pd-Vinyl ≈ Pd-Aryl < Pd-Alkyl.
Неровалентные соединения Pd (0) включают трис (дибензилиденацетон) дипалладий (0) и тетракис (трифенилфосфин) палладий (0). Эти комплексы реагируют с галогенуглеродом R-X в окислительном присоединении к промежуточным соединениям R-Pd-X с ковалентными связями Pd-C. Эта химия составляет основу большого класса органических реакций, называемых реакциями сочетания (см. реакции сочетания, катализируемые палладием ). Примером является реакция Соногашира :

Первое палладиевое соединение (IV) было описано в 1986 году. Этот комплекс представляет собой Me 3 Pd (IV) (I) bpy (bpy = бидентатный 2,2'-бипиридин лиганд) Он был синтезирован окислительным добавлением метилиодида к Me 2 Pd (II) bpy.
Своей реакционной способностью соединения палладия обязаны легкости взаимного превращения между промежуточными соединениями Pd (0) и палладия (II). Однако нет убедительных доказательств участия превращений Pd (II) в Pd (IV) в металлоорганических реакциях, опосредованных палладием. Одна реакция, вызывающая такой механизм, была описана в 2000 году и касалась реакции Хека. Эта реакция сопровождалась 1,5-водородным сдвигом в присутствии аминов:

Предполагалось, что гидридный сдвиг происходит через металлацикл Pd (IV) :
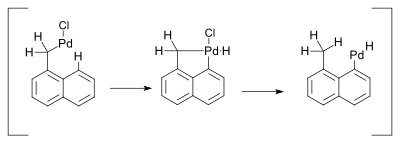
В связанной работе промежуточное соединение, связанное с гидридный сдвиг остается Pd (II):

и в другой работе (новый синтез индолов с двумя миграциями Pd) постулируются равновесия между различными палладациклами:

и в синтетическая ценность определенных внутримолекулярных взаимодействий была продемонстрирована независимо от степени окисления:
