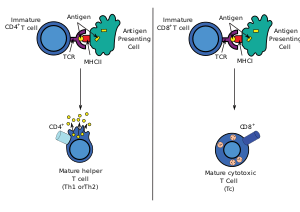
 Стимулирует презентацию антигена Т-клетки становятся либо «цитотоксическими» CD8 + -клетками, либо «вспомогательными» CD4 + -клетками.
Стимулирует презентацию антигена Т-клетки становятся либо «цитотоксическими» CD8 + -клетками, либо «вспомогательными» CD4 + -клетками.A цитотоксическими Т-клетками (также известными как TC, цитотоксические Т-лимфоциты, CTL, Т-киллерные клетки, цитолитические Т-клетки, CD8 + Т-клетки или киллерные Т-клетки ) представляют собой Т-лимфоциты (тип лейкоцитов ), которые убивают раковые клетки, клетки, инфицированные (в частности, вирусы ), или клетки, поврежденные другими
Большинство цитотоксических Т-клеток экспрессируют Т-клеточные рецепторы (TCR), которые могут распознавать специфический антиген. Антиген - это молекула, способная стимулировать иммунный ответ, и часто вырабатывается раковыми клетками или вирусами. Антигены внутри клетки связаны с молекулами MHC класса I и выносятся на поверхность клетки молекулой MHC класса I, где они могут распознаваться Т-клеткой. Если TCR специфичен для этого антигена, он связывается с комплексом молекулы MHC класса I и антигена, и Т-клетка разрушает клетку.
Чтобы TCR мог связываться с молекулой MHC класса I, первый должен сопровождаться гликопротеином, называемым CD8, который связывается с постоянной частью молекула MHC класса I. Следовательно, эти Т-клетки называются CD8 + Т-клетками .
Аффинность между CD8 и молекулой MHC удерживает Т C клетку и целевую клетку тесно связанными друг с другом во время антигена. -специфическая активация. CD8 + Т-клетки распознаются как Т С клетки, когда они становятся активированными, и обычно классифицируются как имеющие заранее определенную цитотоксическую роль в иммунной системе. Однако CD8 + Т-клетки также обладают способностью вырабатывать некоторые цитокины.
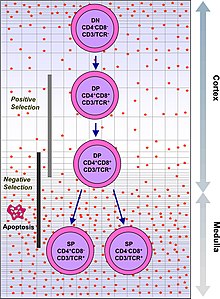 Развитие одиночных положительных Т-клеток в тимусе
Развитие одиночных положительных Т-клеток в тимусе Иммунная система должна распознавать миллионы потенциальных антигенов. В организме человека менее 30 000 генов, поэтому невозможно иметь один ген для каждого антигена. Вместо этого ДНК в миллионах лейкоцитов в костном мозге перетасовывается, чтобы создать клетки с уникальными рецепторами, каждый из которых может связываться с разными антигенами. Некоторые рецепторы связываются с тканями в самом организме человека, поэтому, чтобы организм не атаковал сам себя, эти самореактивные белые кровяные тельца разрушаются во время дальнейшего развития в тимусе, в котором йод необходим для его развития и деятельности.
TCR состоит из двух частей, обычно альфа и бета цепи. (Некоторые TCR имеют гамма- и дельта-цепь.) Гематопоэтические стволовые клетки в костном мозге мигрируют в тимус, где подвергаются V ( D) J-рекомбинация их бета-цепи TCR ДНК с образованием онтогенетической формы белка TCR, известной как пре-TCR. Если эта перестройка успешна, клетки затем перестраивают свою ДНК TCR альфа-цепи для создания функционального комплекса альфа-бета TCR. Этот высоко вариабельный продукт генетической перестройки в генах TCR помогает создавать миллионы различных Т-клеток с разными TCR, помогая иммунной системе организма реагировать практически на любой белок захватчика. Подавляющее большинство Т-клеток экспрессируют альфа-бета TCR (αβ Т-клетки), но некоторые Т-клетки в эпителиальных тканях (например, кишечнике) экспрессируют гамма-дельта TCR (гамма-дельта Т-клетки ), которые распознают небелковые антигены.
Т-клетки с функционально стабильными TCR экспрессируют как CD4, так и CD8 корецепторы и поэтому называются «дважды-положительными» (DP) Т-клетки (CD4 + CD8 +). Двойные положительные Т-клетки подвергаются воздействию широкого спектра аутоантигенов в тимусе и проходят два критерия отбора:
. Положительно отобраны только те Т-клетки, которые слабо связываются с комплексами МНС-аутоантиген. Те клетки, которые переживают положительный и отрицательный отбор, дифференцируются в одноположительные Т-клетки (CD4 + или CD8 +), в зависимости от того, распознает ли их TCR антиген, представленный MHC класса I (CD8), или MHC класса II - представлен антиген (CD4). Именно CD8 + Т-клетки созревают и превращаются в цитотоксические Т-клетки после их активации антигеном, ограниченным классом I.
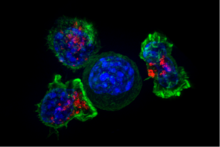 На этом иммунофлуоресцентном изображении группа Т-киллеров (внешние три) взаимодействует с раковыми клетками (одна в центре). Участок сигнальных молекул (розовый), который собирается в месте межклеточного контакта, указывает на то, что CTL идентифицировали цель. Литические гранулы (красные), содержащие цитотоксические компоненты, затем перемещаются вдоль цитоскелета микротрубочек (зеленые) к месту контакта и секретируются, таким образом убивая мишень.
На этом иммунофлуоресцентном изображении группа Т-киллеров (внешние три) взаимодействует с раковыми клетками (одна в центре). Участок сигнальных молекул (розовый), который собирается в месте межклеточного контакта, указывает на то, что CTL идентифицировали цель. Литические гранулы (красные), содержащие цитотоксические компоненты, затем перемещаются вдоль цитоскелета микротрубочек (зеленые) к месту контакта и секретируются, таким образом убивая мишень. За исключением некоторых типов клеток, таких как не- ядерных клетки (включая эритроциты ), MHC класса I экспрессируется всеми клетками-хозяевами. Когда эти клетки инфицированы вирусом (или другим внутриклеточным патогеном ), клетки разлагают чужеродные белки посредством процессинга антигена. В результате образуются пептидные фрагменты, некоторые из которых представлены MHC Class I Т-клеточному антигенному рецептору (TCR) на CD8 + Т-клетках.
Активация цитотоксических Т-клеток зависит от нескольких одновременных взаимодействий между молекулами, экспрессируемыми на поверхности Т-клетки, и молекулами на поверхности антигенпрезентирующей клетки (APC). Например, рассмотрим двухсигнальную модель для активации ячейки T C.
| Сигнал | Т-клетка | APC | Описание |
| Первый сигнал | TCR | связанный с пептидом MHC класса I молекула | Есть второе взаимодействие между корецептором CD8 и молекулой MHC класса I для стабилизации этого сигнала. |
| Второй сигнал | молекула CD28 на Т-клетке | либо CD80, либо CD86 (также называемые B7-1 и B7-2) | CD80 и CD86 известны как костимуляторы активации Т-клеток. Этому второму сигналу можно помочь (или заменить) путем стимуляции Т С клетки цитокинами, высвобождаемыми Т-хелперами. |
Простая активация наивных Т-клеток CD8 требует взаимодействия с профессиональным антигеном - представляющие клетки, в основном созревшие дендритные клетки. Чтобы генерировать долговечные Т-клетки памяти и обеспечить возможность повторной стимуляции цитотоксических Т-клеток, дендритные клетки должны взаимодействовать как с активированными CD4, так и с CD8 Т-клетками. Во время этого процесса CD4-хелперные Т-клетки «лицензируют» дендритные клетки для передачи мощного активирующего сигнала наивным CD8-Т-клеткам.
Кроме того, созревание CD8 + Т-клеток опосредуется CD40 сигнализация. Как только наивная CD8 + Т-клетка связывается с инфицированной клеткой, инфицированная клетка запускается для высвобождения CD40. Это высвобождение CD40 с помощью хелперных Т-клеток будет запускать дифференцировку наивных CD8 + Т-клеток в зрелые CD8 + Т-клетки.
Хотя в большинстве случаев активация зависит от распознавания антигена TCR, альтернативные пути активации были описаны. Например, было показано, что цитотоксические Т-клетки активируются под действием других Т-лимфоцитов CD8, что приводит к толеризации последних.
После активации Т С клетка подвергается клональной экспансии с помогает цитокин интерлейкин-2 (IL-2), который является фактором роста и дифференцировки Т-клеток. Это увеличивает количество клеток, специфичных для целевого антигена, которые затем могут путешествовать по телу в поисках антиген-положительных соматических клеток.
При воздействии инфицированных / дисфункциональных соматических клеток T C клетки выделяют цитотоксины перфорин, гранзимы и гранулизин. Под действием перфорина гранзимы проникают в цитоплазму клетки-мишени, и их функция сериновой протеазы запускает каскад каспазы, который представляет собой серию цистеиновых протеаз, которые в конечном итоге приводят к апоптоз (запрограммированная гибель клеток).
Второй способ вызвать апоптоз - это взаимодействие клеточной поверхности между T C и инфицированной клеткой. Когда T C активируется, он начинает экспрессировать поверхностный белок лиганд FAS (FasL) (Apo1L) (CD95L), который может связываться с Fas (Apo1) (CD95) экспрессируются на клетке-мишени. Однако считается, что это взаимодействие Fas-Fas-лиганд более важно для удаления нежелательных Т-лимфоцитов во время их развития или для литической активности определенных T H клеток, чем для цитолитическая активность эффекторных клеток Т 59 С 100. Взаимодействие Fas с FasL позволяет рекрутировать сигнальный комплекс, индуцированный смертью (DISC). Связанный с Fas домен смерти (FADD) перемещается вместе с DISC, позволяя рекрутировать прокаспазы 8 и 10. Эти каспазы затем активируют эффекторные каспазы 3, 6 и 7, что приводит к расщеплению субстратов смерти, таких как ламин A, ламин B1, ламин B2, PARP (поли-АДФ-рибозная полимераза ) и ДНК-PKcs (ДНК-активированная протеинкиназа). Конечным результатом является апоптоз клетки, экспрессирующей Fas.
Предполагается, что фактор транскрипции эомезодермин играет ключевую роль в функции CD8 + Т-клеток, действуя как регуляторный ген в адаптивном иммунном ответе. Исследования, изучающие эффект потери функции эомезодермина, показали, что снижение экспрессии этого фактора транскрипции привело к снижению количества перфорина, продуцируемого CD8 + Т-клетками.
Во время инфекция вируса гепатита B (HBV) цитотоксические Т-клетки убивают инфицированные клетки и продуцируют противовирусные цитокины, способные очищать HBV от жизнеспособных гепатоцитов. Они также играют важную патогенную роль, внося свой вклад почти во все повреждения печени, связанные с инфекцией HBV. Было показано, что тромбоциты способствуют накоплению вирусоспецифичных цитотоксических Т-клеток в инфицированной печени.
Цитотоксические Т-клетки участвовали в прогрессировании артрита : истощение коленного сустава хряща макромолекул, таких как гликозаминогликаны, цитотоксическими Т-клетками и макрофаги наблюдались в модели заболевания на крысах.
CD8 + Т-клетки, как было обнаружено, играют роль в ВИЧ инфекции. Со временем ВИЧ разработал множество стратегий, позволяющих уклоняться от иммунной системы клетки-хозяина. Например, ВИЧ обладает очень высокой частотой мутаций, что позволяет им избежать распознавания CD8 + Т-клетками. Они также способны подавлять экспрессию поверхностных белков MHC класса I инфицированных ими клеток, чтобы избежать разрушения CD8 + Т-клетками. Если CD8 + T-клетки не могут найти, распознать и связаться с инфицированными клетками, вирус не будет уничтожен и продолжит расти.
Кроме того, недавно было обнаружено, что CD8 + Т-клетки играют критическую роль в диабете 1 типа. Ранее считалось, что это аутоиммунное заболевание контролируется исключительно клетками CD4 +, но недавние исследования на модели мышей с диабетом показали, что CD8 + T-клетки также участвуют в разрушении инсулин-продуцирующих клеток поджелудочной железы.
Интересно, что CD8 + T клетки могут быть необходимы для устранения периферической нейропатии, вызванной химиотерапией (CIPN). У мышей без CD8 + Т-клеток наблюдается более продолжительный CIPN по сравнению с нормальными мышами, а инъекция образованных CD8 + T-клеток разрешает или предотвращает CIPN.