 | |
 | |
| Клинические данные | |
|---|---|
| Торговые наименования | Eliquis, другие |
| Другие имена | BMS-562247-01 |
| AHFS / Drugs.com | Монография |
| MedlinePlus | a613032 |
| Данные лицензии | |
| Беременность. категория |
|
| Способы введения. | Устно |
| Код УВД | |
| Правовой статус | |
| Правовой статус | |
| Фармакокинетические данные | |
| Биодоступность | ~ 50% |
| Связывание с белками | ~ 87% |
| Метаболизм | CYP3A4, CYP3A5, CYP1A2 и другие |
| Период полувыведения | 9–14 часов |
| Экскреция | Желчь (75%), почка (25%) |
| Идентификаторы | |
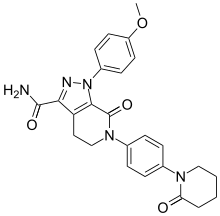
наименование IUPAC
| |
| Номер CAS | |
| PubChem CID | |
| IUPHAR / BPS | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| ChEMBL |
|
| Панель управления CompTox <4180>Dashboard (<4180>EPA | |
| ECHA InfoCard | 100.167.332 |
| Химические и физические данные | |
| Формула | C25H25N5O4 |
| Молярная масса | 459,506 г · моль |
| 3D-модель (JSmol ) | |
УЛЫБКИ
| |
InChI
| |
Апиксабан, продаваемый, среди прочего, под торговой маркой Eliquis, является антикоагулянтным лекарством, используемым для лечения и профилактики тромбы и для предотвращения инсульта у людей с неклапанной мерцательной аритмией. В частности, он используется для предотвращения образования тромбов после замены бедра или коленного сустава, а также у пациентов, у которых в анамнезе уже были сгустки. Он используется как альтернатива варфарину и не требует контроля с помощью анализов крови. Принимается внутрь.
Общие побочные эффекты включают кровотечение и тошноту. Другие побочные эффекты могут включать кровотечение вокруг позвоночника и аллергические реакции. Не рекомендуется использовать во время беременности или грудного вскармливания. Использование кажется относительно безопасным для людей с легкими проблемами почек. По сравнению с варфарином он меньше взаимодействует с другими лекарствами. Это прямой ингибитор фактора Ха..
Апиксабан был одобрен для медицинского применения в Европейском Союзе в мае 2011 года и в США в декабре 2012 года. В 2017 году это был 93-й по популярности препарат в США. Штаты с более чем восемью миллионами рецептов. В декабре 2019 г. дженерики были одобрены в США.
Апиксабан показан в следующих случаях:
В ЕС апиксабан показан для профилактики венозных тромбоэмболических осложнений (ВТЭ) у взрослых, перенесших плановую операцию по замене тазобедренного или коленного сустава, для профилактики инсульта и системной эмболии у взрослых с неклапанной болезнью сердца. фибрилляция предсердий (NVAF) с одним или несколькими факторами риска, для лечения тромбоза глубоких вен (DVT) и тромбоэмболии легочной артерии (PE) у взрослых, а также для профилактики рецидивов DVT и PE у взрослых.
Апиксабан рекомендован Национальным институтом здравоохранения и клинического мастерства для профилактики инсульта и системной эмболии у людей с неклапанной фибрилляцией предсердий и по крайней мере одним из следующих факторов риска : перенесенный инсульт или транзиторная ишемическая атака, возраст 75 лет и старше, d сахарный диабет или симптоматическая сердечная недостаточность.
Апиксабан и другие антикоагулянты (дабигатран, эдоксабан и ривароксабан ) одинаково эффективны, как варфарин. в профилактике негеморрагического инсульта у людей с фибрилляцией предсердий и связаны с более низким риском внутричерепного кровотечения.
Хотя апиксабан может использоваться у людей с сильно сниженной функцией почек и находящихся на гемодиализе, он не изучался в этих группы. Можно использовать полную дозу апиксабана (5 мг [два раза в день]), если не применяются по крайней мере две из следующих характеристик: возраст пациента 80 лет и старше, масса тела 60 кг или меньше и креатинин сыворотки 1,5 мг / дл или выше., в этом случае показано снижение дозы до 2,5 мг 2 раза в день.
Апиксабан может увеличить риск кровотечения, которое может быть серьезным и потенциально смертельным. Одновременное применение с другими лекарствами, влияющими на свертываемость крови, может еще больше повысить этот риск. Сюда входят лекарства, такие как другие антикоагулянты, гепарин, аспирин, антитромбоцитарные препараты, селективные ингибиторы обратного захвата серотонина, ингибиторы обратного захвата серотонина и норэпинефрина и нестероидные противовоспалительные препараты (
Andexanet alfa - одобренный Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) антидот для апиксабана у людей с неконтролируемыми и опасными для жизни кровотечениями.
После спинномозговой анестезии или пункции люди, получающие антитромботические препараты, имеют более высокий риск развития гематомы, которая может вызвать длительный или необратимый паралич. Риск этого может быть увеличен при использовании эпидуральных или интратекальных катетеров после хирургической операции или при одновременном применении лекарственных средств, влияющих на гемостаз.
Апиксабан представляет собой высокоселективный, перорально биодоступный и обратимый прямой ингибитор свободного и связанного со сгустком фактора Ха. Фактор Ха катализирует превращение протромбина в тромбин, последний фермент в каскаде свертывания, который отвечает за образование сгустка фибрина. Апиксабан не оказывает прямого действия на агрегацию тромбоцитов, но, ингибируя фактор Ха, он косвенно снижает образование сгустков, вызванное тромбином.
Апиксабан был одобрен для медицинского применения в Европейский Союз в мае 2011 года.
A Заявка на новый препарат (NDA) на одобрение апиксабана была подана в Управление по контролю за продуктами и лекарствами (FDA) США Bristol-Myers Squibb (BMS) и Pfizer совместно после завершения клинического исследования ARISTOTLE в 2011 году. Апиксабан был одобрен для профилактики инсульта у людей с фибрилляцией предсердий 28 декабря 2012 года. 13 марта 2014 года, он был одобрен в качестве дополнительного показания для предотвращения тромбоза глубоких вен и тромбоэмболии легочной артерии у людей, недавно перенесших замену коленного или тазобедренного сустава. 21 августа 2014 г. FDA одобрило апиксабан в качестве дополнительного показания для лечения рецидивирующего тромбоза глубоких вен и тромбоэмболии легочной артерии. Во время разработки препарат был известен как БМС-562247-01. К концу 2019 года продажи продукта BMS составили тридцать процентов их квартальной выручки. В декабре 2019 года FDA США одобрило универсальную версию, созданную совместно Mylan и.