β2агонисты адренорецепторов - группа препаратов, которые избирательно действуют на β 2 -рецепторы в легких, вызывающие бронходилатацию. β 2 -агонисты используются для лечения астмы и ХОБЛ, заболеваний, вызывающих обструкцию дыхательных путей. До их открытия использовался неселективный бета-агонист изопреналин. Целью разработки лекарств на протяжении многих лет было минимизировать побочные эффекты, добиться селективности и большей продолжительности действия. Механизм действия хорошо изучен и облегчил разработку. Структура сайта связывания и природа связывания также хорошо известны, как и взаимосвязь между структурой и активностью.
Β 2 -селективные агонисты были разработаны в 20 веке и представляют собой очень ценный класс лекарственных средств. В 1901 году Юкичи Такамине выделил гормон адреналин, также известный как адреналин. В 1890 году адреналин впервые стали вводить больным астмой перорально. Он имел незначительный эффект или не имел никакого эффекта, потому что он метаболизируется в пищеварительном тракте и дезактивируется. В 1930 году адреналин впервые был введен подкожно, и было обнаружено его положительное влияние на астму. При подкожном введении адреналин влияет на все тело, вызывая различные побочные эффекты и тем самым снижая ценность этого лечения. Позднее был опробован ингаляционный путь, который дал гораздо меньше побочных эффектов, но все же имел неудобные побочные эффекты, такие как страх, беспокойство, беспокойство, головная боль, головокружение и сердцебиение.
В 1940 году изопротеренол (изопреналин ) был открыт. Это соединение имело такое же действие, как и адреналин, но было обнаружено меньше побочных эффектов. В 1949 году изопротеренол в основном использовался для лечения пациентов с астмой, давали сублингвально или вдыхали. Первый дозирующий ингалятор под давлением был представлен в 1956 году. Он был намного удобнее для пациентов, чем ранее использовавшиеся ингаляторы с выдавливаемой грушей. Ингалятор с отмеренными дозами под давлением быстро развивался в 1970-х годах.
В 1967 году было показано, что β 2 -рецептор отвечает за бронходилатацию, и это привело к разработке более селективных лекарств. В 1961 году был обнаружен орципреналин, β 2 -агонист длительного действия, но он был не таким сильным, как изопротеренол. Орципреналин не имеет структуры катехол, что является причиной более длительного времени действия. В середине 1960-х годов был открыт альбутерол или сальбутамол, а несколько лет спустя последовали трибуталин и фенотерол. Альбутерол и тербуталин вызывали меньше побочных эффектов, таких как учащение пульса, чем изопротеренол. Фармацевтическая компания Glaxo открыла салметерол, β 2 -агонист длительного действия, который проявлял бронходилатационную активность в течение до 12 часов. Он поступил в продажу в 1990 году. Вскоре после этого появился на рынке формотерол, еще один β 2 -агонист длительного действия. Такая длительная продолжительность действия сделала лечение тяжелой астмы и ХОБЛ более удобным для пациентов, так как его вдыхают дважды в день. В 2013 г. появился на рынке бета 2 -агонист сверхдлительного действия, вилантерол. Его продолжительность действия составляет 24 часа, что должно улучшить комплаентность пациентов и сделать лечение более удобным.
β2-агонисты используются для лечения астмы, воспалительное заболевание дыхательных путей. Воспаление делает бронхи чувствительными к некоторым факторам окружающей среды, что вызывает сужение бронхов. Когда это сужение происходит, дыхательные пути сужаются, что вызывает такие симптомы, как хрипы, стеснение в груди, одышка и кашель. Мышцы в дыхательных путях сжимаются, и клетки в дыхательных путях начинают производить больше слизи, чем обычно, что еще больше сужает дыхательные пути. Симптомы часто проявляются в детстве, но могут начаться в любом возрасте.
Используются β 2 -агонисты как короткого, так и длительного действия. для лечения хронической обструктивной болезни легких. ХОБЛ вызывает ограничение воздушного потока в легких из-за воспаления. Курение является основным фактором риска, но вдыхание токсичных и вредных частиц и газов также может вызвать заболевание. Симптомами являются аномальное образование слизи, вздутие легких, вызывающее ограничение воздушного потока, аномальный газообмен и легочная гипертензия. ХОБЛ чаще всего встречается у людей старше пятидесяти лет, давно курящих. Сначала симптомы легкие, но со временем ухудшаются.
Существует два типа β 2 -агонистов: длительного и короткого действия. Их как вдыхают, так и вводят с помощью устройств для доставки аэрозолей. Β 2 -агонисты длительного действия часто назначают в комбинации с кортикостероидами для лечения астмы. Β 2 -агонисты короткого действия используются для лечения астмы, вызванной физической нагрузкой, и для пациентов, страдающих астмой, для быстрого облегчения симптомов. Их принимают за 10–15 минут до тренировки. Бронходилатация начинается через несколько минут после вдыхания β 2 -агонистов короткого действия и длится от 4 до 8 часов. При лечении острой астмы, вызванной физической нагрузкой, длительно действующие β 2 -агонисты не рекомендуются, поскольку их постоянное применение может маскировать плохо контролируемую астму.
Кинетика расслабления гладкой мускулатуры дыхательных путей, в зависимости от начала и продолжительности бронходилатации у пациентов с астмой, отражается в различии в механизме взаимодействия короткие- (SABA) и длинные β2-агонисты (LABA) и β 2 -рецептор. Существует множество составов селективных β 2 -агонистов; ингаляция является предпочтительным путем, поскольку он наиболее быстро эффективен и связан с минимальными побочными эффектами. Сульфатные конъюгаты являются основными метаболитами ; связывание с белками довольно слабое, и только незначительные взаимодействия были обнаружены с другими лекарствами. Основными ферментами, регулирующими метаболизм хатехоламинов, являются COMT и MAO. Коммерческие SABA, сальбутамол и тербуталин устойчивы к COMT, но медленно метаболизируются MAO, в то время как LABA устойчивы как к COMT, так и к MAO. Кроме того, большая продолжительность действия салметерола связана с повышенной липофильностью молекул, что позволяет ему дольше оставаться в легких. β 2 -агонисты в основном элиминируются почечным процессом после парентерального введения, тогда как после перорального введения более выраженный метаболический клиренс (высокий эффект первого прохождения) отвечает за низкую биодоступность. Выведение после ингаляции не изучалось, но профиль, вероятно, находится где-то между тем, что мы наблюдаем после парентерального и перорального введения.
 Рисунок 1: Кристаллическая структура активированного β 2 -адренорецептор в комплексе с G s(PDB вход 3SN6 ). Рецептор окрашен в красный цвет, Gα зеленый, Gβ голубой и Gγ желтый. С-конец Gα расположен в полости, созданной движением наружу цитоплазматических частей TM5 и 6.
Рисунок 1: Кристаллическая структура активированного β 2 -адренорецептор в комплексе с G s(PDB вход 3SN6 ). Рецептор окрашен в красный цвет, Gα зеленый, Gβ голубой и Gγ желтый. С-конец Gα расположен в полости, созданной движением наружу цитоплазматических частей TM5 и 6. β-рецепторы представляют собой мембраносвязанные рецепторы, связанные с G-белками. С помощью молекулярной фармакологии идентифицированы три типа β-рецепторов. β1рецепторы составляют до 75% всех бета-рецепторов и преимущественно расположены в сердце. β2рецепторы обнаружены в гладких мышцах сосудов и бронхов. β3рецепторы, которые предположительно участвуют в метаболизме жирных кислот, расположены в адипоцитах.
 Рисунок 2: цикл GPCR
Рисунок 2: цикл GPCR рецепторы, связанные с G-белком, состоят из одного полипептидные цепи из 300-600 аминокислот и семь раз покрывают плазматическую мембрану. Имеется три внеклеточных петли, одна из которых является аминоконцом, и три внутриклеточные петли с карбокси-концом. Гидрофильный карман образован внутри мембраны семью альфа-спиральными трансмембранными доменами. лиганд связывается с гидрофильным карманом в рецепторном белке и активирует рецептор, вызывая клеточный эффект.
Когда β 2 -агонист связывается и активируется На внутриклеточную передачу сигналов β 2 -адренорецептора в значительной степени влияет циклический аденозинмонофосфат (цАМФ ) и протеинкиназа A (PKA ). На связывание β 2 -рецептора с аденилатциклазой влияет тримерный Gs-белок, как показано на фиг.2, состоящий из α-субъединицы ( который стимулирует аденилатциклазу) и βγ-субъединицы (которые передают другие сигналы). Аденилатциклаза катализирует превращение аденозинтрифосфата в цАМФ, который является вторым мессенджером, тем самым увеличивая внутриклеточные уровни цАМФ, что приводит к расслаблению гладких мышц. Уровни цАМФ регулируются посредством активности изоферментов / изоформ фосфодиэстеразы, которая расщепляет его до 5'-AMP. Механизм, с помощью которого цАМФ вызывает расслабление гладкомышечных клеток дыхательных путей, полностью не изучен. Считается, что цАМФ катализирует активацию PKA, которая, в свою очередь, фосфорилирует ключевые регуляторные белки, участвующие в контроле мышечного тонуса. цАМФ также играет роль в ингибировании высвобождения иона кальция (Ca) из внутриклеточных запасов, секвестрации внутриклеточного Ca и снижении проникновения Ca через мембраны, что приводит к расслаблению гладких мышц дыхательных путей.
 Рисунок 3 : Связывание норэфинефрина с сайтом связывания
Рисунок 3 : Связывание норэфинефрина с сайтом связывания Связывание норэфинефрина с сайтом связывания состоит из одной ионной связи, трех водородных связей и ван дер Ваальс взаимодействие в двух местах. Ионная связь образуется между протонированным амином и Asp-113 в спирали 3. Водородные связи образуются из гидроксильных групп, связанных с катехольным кольцом, с Ser-204 и Ser-207 в спирали 5. Это связывание ограничивает конфигурацию и свободу вращения. Силы Ван-дер-Ваальса между ароматическим катехиновым кольцом и Phe-290 в остатке спирали 6 и Val-114 в остатке спирали 3 усиливают связывание. Считается, что N-алкильные заместители помещаются в гидрофобный карман, образованный между остатками спирали 6 и 7. Бета-углерод хиральный и должен иметь R-конфигурацию, чтобы бета-гидроксильная группа была ориентированы к остатку Asn-293 в спирали 6 с образованием водородной связи, необходимой для связывания с рецептором бета-2.
Две теории объясняют долгое время действия LABA. Первый объяснил длительное действие предполагаемым «экзозитом » или «экзоцептором», отличным от β 2 -адренорецептора, с которым длинный алифатический хвост салметерола связывается с высоким сродством. Это позволяет активной салигениновой головке поворачиваться и отклоняться от рецептора, чтобы активировать его многократно. Формотерол не имеет длинной боковой цепи, как у салметерола, для связывания с «экзосайтом», поэтому эта теория подвергается сомнению. В 1994 году Андерсон. и другие. представил теорию диффузионной микрокинетики плазмалеммы, объясняя, что происходит с β 2 - агонистом в липидном бислое клеточной мембраны и в водной биофазе, ближайшей к сайту связывания β 2 -адренорецептора. Предполагается, что липидный бислой плазмалеммы гладких мышц дыхательных путей действует как депо для агонистов β 2 -адренорецепторов. Агонисты β 2 -адренорецепторов остаются доступными для взаимодействия с активным сайтом β 2 -адренорецепторов после разделения в липидный бислой.
Основным фармакофором для всех адренергических агонистов является замещенный фенэтиламин, который увеличивает продолжительность действия.
адренергических агонистов, которые являются селективными в отношении подтипа β 2, вызывают расширение бронхов и, как можно ожидать, снимут бронхоспазм у астматика. атака. Неселективные β-агонисты обладают стимулирующим действием на сердце и поэтому имеют ограниченное применение у кардиологических пациентов с астмой.
Введение более высоких доз β 2 -агонистов короткого действия увеличивает продолжительность действия, но также увеличивает побочные эффекты, такие как сердечные эффекты. Один из подходов, позволяющих избежать этих побочных эффектов, заключается в использовании различных по структуре свойств, которые могут минимизировать абсорбцию в системный кровоток. Например, можно использовать лекарства, которые превращаются в неактивные метаболиты при попадании в системный кровоток.
Заместители на фармакофор влияют на то, будет ли аналог иметь прямое или непрямое действие или их смесь. Это также влияет на специфичность подтипов β-рецепторов. Аналог прямого действия связывает β-адренорецепторы напрямую и вызывает симпатический ответ. Аналог непрямого действия вызывает агонистический эффект, но без прямого связывания с β-адренергическим рецептором, например, стимулируя высвобождение норэпинефрина (NE) с пресинаптического конца или ингибируя обратный захват высвобожденного NE.
 Рисунок 4: Примеры фенильных колец, используемых для β 2 -агонистов
Рисунок 4: Примеры фенильных колец, используемых для β 2 -агонистов На фиг. 4 показаны фенильные кольца, которые используются для β 2 -агонистов. Их называют резорциновым кольцом, салициловым спиртом или м-формамидной группой. На рис. 5 показано, где разные заместители в фенилэтиламине занимают места, отмеченные разными R-группами.
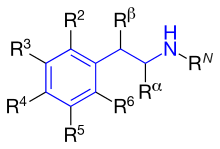 Фигура 5: Замещение R-групп на фенилэтиламине
Фигура 5: Замещение R-групп на фенилэтиламине Различие между заместителями R1-R5 описано ниже. Все продаваемые β 2 -агонисты имеют гидроксильную группу в положении R3 и чаще всего в положении R5.
R: Эта группа определяет селективность α- или β-рецептора. Чем больше заместитель, тем выше селективность в отношении β-рецептора. Если трет-бутил расположен в позиции R, он показывает высокое сродство к β 2 -рецептору. Длинный фенилбутоксигексильный заместитель в этом положении дает высокую β 2 -селективность, а также высокую липофильность и, следовательно, более длительную продолжительность действия.
R: Заместители, отличные от водорода, дадут увеличенную продолжительность действия. действие. Группа этил повысила бы селективность в отношении β 2 -рецептора. Однако этильная группа, по-видимому, вызывает усиление побочных эффектов и низкую активность β 2 -рецептора по сравнению с другими β 2 -селективными агонистами.
R: гидроксильная группа оказывает прямое действие на β-рецептор. Как отмечалось ранее, все продаваемые β 2 -агонисты имеют гидроксильную группу в этом положении, которое делает соединение хиральным, и активным, когда оно имеет (R) -конфигурацию.
R или R : гидроксильная группа, размещенная на углеродном номере 5 или 3 (мета-положение ), оказывает прямое действие на β-адренергический рецептор.
R: либо гидроксильная группа, либо водородная группа в этом положении оказывает прямое действие на β-рецептор.
Обобщение нескольких агонистов β 2 -адренорецепторов и их структурной активности показывает, как они действуют по-разному в отношении эффективности, селективности, аффинности и продолжительности действия ( см. таблицу 1 ):
| Химическая структура | Название | Описание |
|---|---|---|
 | Эпинефрин (адреналин) | Комбинация ядра катехина, β-гидроксильной группы и N-метильной группы. Эти качества обеспечивают прямое действие и сильное сродство ко всем адренергическим рецепторам. |
 | Тербуталин | Комбинация N-трет-бутила и фенильного кольца резорцина, придающая активность β2-рецептору. |
 | Альбутерол (сальбутамол) | Имеет фенильное кольцо из N-трет-бутила и салицилового спирта, что придает ему оптимальную β2-селективность. Сальбутамол является β2-агонистом короткого действия, но имеет быстрое начало действия. Начало его при вдыхании - в течение 5 минут. Гидроксильная группа на β-углероде представляет собой смесь S- и R-изомеров, где R-изомер является активным. Другой препарат, левалбутерол, имеет точно такую же структуру. он содержит только R-изомер альбутарола и, следовательно, гораздо более активен, и доза для левалбутерола будет в четыре раза меньше, чем для альбутарола. |
 | Салметерол | Имеет N-фенилбутоксигексильный заместитель, β-гидроксильную группу и салицилфенильное кольцо, которое придает активность и прямую селективность в отношении β2-рецептора. Оптимальное положение кислорода простого эфира в цепи салметерола как по активности, так и по продолжительности составляет шесть атомов углерода от основного азота. |
 | Формотерол | Имеет N-изопропил-пара-метоксифенильную группу, которая дает прямую действие на β-рецепторы. Форметерол также имеет м-формамидное и п-гидроксифенильное кольцо, которое придает селективность β2-рецепторам. Начало действия форметерола составляет около 20 минут, а продолжительность действия - 12 часов. Если сравнивать форметерол с салметеролом, то он обладает большей растворимостью в воде, что позволяет ему быстрее добраться до рецепторных участков, а липофильность дольше удерживает его в легких. Форметерол имеет два асимметричных центра. Сообщается, что R, R-энантиомер в 1000 раз более активен, чем S, S-энантиомер. |
 | Вилантерол | Последний препарат на рынке. Он имеет структуру, аналогичную салметеролу, но также имеет 2,6-дихлорбензил и две алкокси группы на N-цепи. Он продемонстрировал селективность, аналогичную сальметеролу, в отношении β2-рецептора, но большую селективность по сравнению со всеми другими протестированными агонистами. Было показано, что собственная активность выше, чем у салметерола. Вилантерол очень эффективен и обладает высокой эффективностью. Обладает быстрым началом действия и длительным действием. Включение дополнительной алкоксигруппы в боковую цепь дает мощный β2-агонист, который быстро метаболизируется в печени человека. 2,6-дихлорбензил, по-видимому, дает большую эффективность, селективность, быстрое начало действия, длительную продолжительность действия и быстрое обновление. |
β 2 -агонисты, которые используются в клинической практике, представляют собой все замещенные β-фенэтиламин (см. рис. 5), и они имеют три вида фенильных колец, показанных на рис. 4. Они называются кольцом резорцина, кольцом салицилового спирта или кольцом N- формамидное кольцо. Спиртовые заместители в фенильном кольце реакционноспособны и усложняют синтез β 2 -агонистов. При добавлении N-остатка в положение R1 требуется ступень защиты (рисунок 5). Еще одна вещь, усложняющая синтез, - это получение оптически чистого R (-) энантиомера соединения. Стереохимия очень важна для активности, потому что только R (-) энантиомер способен образовывать водородные связи, необходимые для того, чтобы соответствовать сайту связывания и активировать β 2 -рецептор.
Сальбутамол обычно вдыхается в рацемических смесях (например, вентолин). Путем лечения астмы оптически чистым (R) -сальбутамолом можно минимизировать риск побочных эффектов, таких как эффекты стимуляции нервной системы и сердечная аритмия. Вот почему описано несколько способов получения оптически чистого сальбутамола, но они недостаточно эффективны для использования в фармацевтической промышленности. Наиболее эффективным способом получения чистого (R) -сальбутамола является получение рацемической смеси с последующим разделением изомеров.
Стереоселективный синтез трибуталина и сальбутамола ацеталя может быть осуществлен из O-защищенных- (R) -циангидринов. F. Effenberg и др. описать способ синтеза. Основные сложности заключаются в проведении стадии снятия защиты без рацемизации и в образовании чистой соли. Реакция Риттера может использоваться для N-третичного бутилирования. В этом эксперименте деацетилирование (R) -сальбутамола ацеталя было безуспешным, поэтому его нельзя использовать для получения чистого (R) -сальбутамола. На рисунке 6 показаны основные этапы синтеза салметерола и трибуталина.
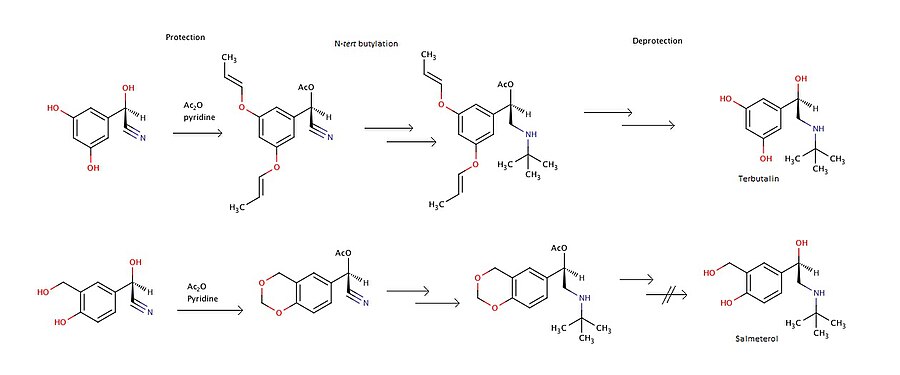 Рисунок 6: Синтез трибуталина и сальбутамола из циангидринов
Рисунок 6: Синтез трибуталина и сальбутамола из циангидринов Может быть синтезирован сальметерол β 2 -агониста длительного действия из фенэтилового спирта. Дибромгексан используется для связывания фенэтилового спирта с этиламином салицилового спирта. На рисунке 7 показаны основные этапы синтеза.
 Рисунок 7: Синтез салметерола
Рисунок 7: Синтез салметерола