
Изображение топологии пальмитоилтрансфераз семейства DHHC. Трансмембранные альфа-спирали представлены черными трубками. Домен DHHC показан в виде светло-оранжевого овала.
В молекулярной биологии домен DHHC представляет собой домен белка, который действует как фермент, который добавляет химическая группа пальмитоил к белкам, чтобы закрепить их на клеточных мембранах. Домен DHHC был открыт в 1999 году и назван в честь консервативного мотива последовательности, обнаруженного в его белковой последовательности. Рот и его коллеги показали, что дрожжевой Akr1p-белок может пальмитоилат Yck2p in vitro, и сделали вывод, что домен DHHC определяет большое семейство пальмитоилтрансфераз. У млекопитающих идентифицировано двадцать три члена этого семейства и исследованы их субстратные особенности. Некоторые члены семейства, такие как ZDHHC3, и усиливают пальмитоилирование белков, таких как PSD-95, SNAP-25, GAP43, Гэс. Другие, такие как ZDHHC9, показали специфичность только в отношении белка H-Ras. Однако недавнее исследование ставит под сомнение участие классического распознавания и специфичности фермент-субстрат в реакции пальмитоилирования. Некоторые члены семьи были замешаны в заболеваниях человека.
Содержание
- 1 Мотивы последовательности
- 2 Структура и механизм
- 3 Химические ингибиторы
- 4 При заболеваниях человека
- 5 Белки человека, содержащие этот домен
- 6 См. Также
- 7 Ссылки
- 8 Дополнительная литература
- 9 Внешние ссылки
Мотивы последовательностей
Консервативные мотивы в белковых последовательностях указывают на наиболее важные аминокислотные остатки для функции. В домене DHHC имеется тетрапептидный мотив, состоящий из аспартата - гистидина -гистидина- цистеина. Однако эта короткая последовательность встроена в более крупную область длиной около пятидесяти аминокислот, которая имеет гораздо больше консервативных аминокислот. Канонический домен DHHC может быть описан следующим мотивом последовательности:
C-x2-C-x9-HC-x2-C-x2-C-x4-DHHC-x5-C-x4-N-x3-F (x показывает область неконсервативных остатков)Однако известно много примеров доменов DHHC, которые не содержат всех этих консервативных остатков. Помимо центрального домена DHHC, у членов семейства DHHC были идентифицированы еще три мотива последовательности. Мотив DPG (аспартат- пролин - глицин ) был идентифицирован только на С-конце второй трансмембранной области. Мотив TTxE (треонин -реонин-любой- глутамат ) также был идентифицирован после четвертой трансмембранной спирали. Был идентифицирован третий мотив по направлению к С-концу многих белков, который содержит консервативную ароматическую аминокислоту, глицин и аспарагин, названный мотивом PaCCT (консервативный мотив C-конца PAlmitoiltransferase).
Структура и механизм
Было решено несколько структур домена DHHC, и известно, что он работает на линейно расположенной каталитической триаде Asp153, His154 и Cys156. Он работает по механизму пинг-понга, где цистеин атакует ацил-КоА с образованием S-ацилированного DHHC, а затем ацильная группа переносится на субстрат. Существуют ферменты DHHR, и он (как и некоторые ферменты DHHC) может вместо этого использовать механизм тройного комплекса.
Химические ингибиторы
В 2006 году пять химических классов были обнаружены небольшие молекулы, которые, как было показано, действуют против пальмитоилтрансфераз. Дальнейшие исследования в 2009 году показали, что из 5 изученных классов 2- (2-гидрокси-5-нитробензилиден) бензо [b] тиофен-3-он ведет себя аналогично и был идентифицирован как способный к ингибировать реакцию пальмитоилирования ряда белков, содержащих домен DHHC. Было обнаружено, что ингибирование 2-бромопальмитатом является необратимым, а другое, однако, в основном обратимым. Из-за роли белков домена DHHC в заболеваниях человека было высказано предположение, что химические ингибиторы конкретных белков DHHC могут быть потенциальным путем лечения заболевания.
При заболевании человека
Несколько белков, содержащих Домены DHHC участвуют в заболеваниях человека. Две миссенс-мутации в домене DHHC ZDHHC9 были идентифицированы в X-связанной умственной отсталости, связанной с марфаноидной привычкой. Возможная связь рака мочевого пузыря с раком мочевого пузыря была подтверждена открытием, что 5 из 9 исследованных образцов рака мочевого пузыря высокой степени злокачественности содержали дупликацию геномной области 5p15.33. Однако эта область содержит другой ген TPPP, который может быть причинным геном. Пальмитоилтрансфераза HIP14 отвечает за пальмитоилирование белка Huntingtin. Расширение триплетного повтора в гене хантингтона приводит к потере взаимодействия с HIP14, который, как предполагают Янаи и его коллеги, участвует в патологии болезни Хантингтона. Эксперимент с нокаутом гена у мышей-гомологов показал выпадение волос, тяжелый остеопороз и системный амилоидоз, отложения как AL, так и AA.
человеческие белки, содержащие этот домен
; ZDHHC2 ; ZDHHC3 ; ZDHHC4 ; ; ; ; ZDHHC8 ; ZDHHC9 ; ; ; ; ; ZDHHC14 ; ; ; ZDHHC17 ; ; ; ; ; ; ; ;
См. Также
Ссылки
Дополнительная литература
- Гривз Дж., Горлеку О.А., Салаун С., Чемберлен Л.Х. (август 2010). «Пальмитоилирование семейства белков SNAP25: СПЕЦИФИЧНОСТЬ И РЕГУЛИРОВАНИЕ ПЕРЕДАЧИ ПАЛМИТОИЛА DHHC». J. Biol. Chem. 285 (32): 24629–38. doi : 10.1074 / jbc.M110.119289. PMC 2915699. PMID 20519516.
- Гривз Дж., Чемберлен Л.Х. (апрель 2010 г.). «S-ацилирование белком семейства DHHC». Biochem. Soc. Пер. 38 (2): 522–4. DOI : 10.1042 / BST0380522. PMID 20298214. S2CID 2048858.
- Хайнс Р.М., Канг Р., Гойтайн А., Куамме, Джорджия (февраль 2010 г.). «Гольджи-специфический DHHC цинковый белок пальца GODZ опосредует мембранный перенос Ca2 +». J. Biol. Chem. 285 (7): 4621–8. doi : 10.1074 / jbc.M109.069849. PMC 2836067. PMID 19955568.
- Mizumaru C, Saito Y, Ishikawa T. и др. (Декабрь 2009 г.). «Подавление транспорта везикул, содержащих АРР, и продукции бета-амилоида с помощью белка AID / DHHC-12». J. Neurochem. 111 (5): 1213–24. DOI : 10.1111 / j.1471-4159.2009.06399.x. PMID 19780898.
- Норитаке Дж., Фуката Й., Иванага Т. и др. (Июль 2009 г.). «Мобильный пальмитоилирующий фермент DHHC опосредует чувствительное к активности синаптическое нацеливание PSD-95». J. Cell Biol. 186 (1): 147–60. DOI : 10.1083 / jcb.200903101. PMC 2712995. PMID 19596852.
- Хоу Х, Джон Питер А.Т., Мейрингер С., Субраманиан К., Унгерманн С. (август 2009 г.). «Анализ ацилтрансфераз DHHC предполагает перекрывающуюся субстратную специфичность и двухступенчатый механизм реакции». Движение. 10 (8): 1061–73. DOI : 10.1111 / j.1600-0854.2009.00925.x. PMID 19453970.
- Гривз Дж., Прескотт Г.Р., Фуката И., Фуката М., Салаун С., Чемберлен Л.Х. (март 2009 г.). «Гидрофобный богатый цистеином домен пар SNAP25 с нижележащими остатками для опосредования мембранных взаимодействий и распознавания пальмитоилтрансферазами DHHC». Мол. Биол. Cell. 20 (6): 1845–54. DOI : 10.1091 / mbc.E08-09-0944. PMC 2655257. PMID 19158383.
- Johswich A, Kraft B, Wuhrer M, et al. (Январь 2009 г.). «Для нацеливания Гольджи на β4GalNAcTB Drosophila melanogaster необходим белок, родственный семейству белков DHHC, в качестве пилотного». J. Cell Biol. 184 (1): 173–83. DOI : 10.1083 / jcb.200801071. PMC 2615082. PMID 19139268.
- Матакацу Х., Блэр СС (сентябрь 2008 г.). «приблизительно кодирует пальмитоилтрансферазу DHHC, которая регулирует передачу сигналов жиров, а также субклеточную локализацию и активность Dachs». Curr. Биол. 18 (18): 1390–5. DOI : 10.1016 / j.cub.2008.07.067. PMC 2597019. PMID 18804377.
- Баннан Б.А., Ван Эттен Дж., Холер Дж. А. и др. (2008). «Белок пальмитойлома Drosophila: характеристика пальмитоилтиоэстеразы и пальмитоилтрансферазы DHHC». Fly (Остин). 2 (4): 198–214. doi : 10.4161 / fly.6621. PMC 2898910. PMID 18719403.
- Dighe SA, Kozminski KG (октябрь 2008 г.). «Swf1p, член семейства пальмитоилтрансфераз DHHC-CRD, регулирует актиновый цитоскелет и поляризованную секрецию независимо от его мотива DHHC». Мол. Биол. Cell. 19 (10): 4454–68. doi : 10.1091 / mbc.E08-03-0252. PMC 2555925. PMID 18701706.
- Лам К.К., Дэйви М., Сан Б., Рот А.Ф., Дэвис Н.Г., Конибир Э. (июль 2006 г.). «Пальмитоилирование белком DHHC Pfa4 регулирует выход из ЭР Chs3». J. Cell Biol. 174 (1): 19–25. DOI : 10.1083 / jcb.200602049. PMC 2064155. PMID 16818716.
- Оно Y, Кихара А., Сано Т., Игараси Y (апрель 2006 г.). «Внутриклеточная локализация и тканеспецифическое распределение белков, содержащих богатый цистеином домен DHHC человека и дрожжей». Биохим. Биофиз. Acta. 1761 (4): 474–83. doi : 10.1016 / j.bbalip.2006.03.010. HDL : 2115/14509. PMID 16647879.
- Mitchell DA, Vasudevan A, Linder ME, Deschenes RJ (июнь 2006 г.). «Пальмитоилирование белков семейством S-ацилтрансфераз DHHC». J. Lipid Res. 47 (6): 1118–27. doi : 10.1194 / мл.R600007-JLR200. PMID 16582420.
- Hou H, Subramanian K, LaGrassa TJ, et al. (Ноябрь 2005 г.). «Белок Pfa3 DHHC влияет на связанное с вакуолью пальмитоилирование фактора слияния Vac8». Proc. Natl. Акад. Sci. США 102 (48): 17366–71. Bibcode : 2005PNAS..10217366H. doi : 10.1073 / pnas.0508885102. PMC 1297695. PMID 16301533.
- Смотрис Дж. Э., Шенфиш М. Дж., Штутц М. А., Линдер М. Е. (сентябрь 2005 г.). «Вакуолярный белок Pfa3p DHHC-CRD представляет собой протеинацилтрансферазу для Vac8p». J. Cell Biol. 170 (7): 1091–9. doi : 10.1083 / jcb.200507048. PMC 2171546. PMID 16186255.
- Глисон Э.Дж., Линдси В.К., Крофт Т.Л., Сингсон А.В., Л'эрно, SW (январь 2006 г.). «spe-10 кодирует DHHC-CRD белок мембраны цинка-пальца, необходимый для морфогенеза эндоплазматической сети / мембраны Гольджи во время сперматогенеза Caenorhabditis elegans». Генетика. 172 (1): 145–58. doi : 10.1534 / genetics.105.047340. ПМС 1456142. PMID 16143610.
- Сейдел К.Б., Гаур Д., Аравинд Л., Субраманиан Г., Миллер Л.Х. (август 2005 г.). «Plasmodium falciparum: характеристика белка Гольджи на поздней бесполой стадии, содержащего как анкирин, так и домены DHHC». Exp. Паразитол. 110 (4): 389–93. doi : 10.1016 / j.exppara.2005.03.030. PMID 15882865.
- Сайто Ф., Тиан QB, Окано А., Сакагами Х., Кондо Х., Судзуки Т. (июль 2004 г.). «NIDD, новый DHHC-содержащий белок, направляет нейрональную синтазу оксида азота (nNOS) на синаптическую мембрану посредством PDZ-зависимого взаимодействия и регулирует активность nNOS». J. Biol. Chem. 279 (28): 29461–8. doi : 10.1074 / jbc.M401471200. PMID 15105416.
- Нагая М., Инохая К., Имаи Ю., Кудо А. (декабрь 2002 г.). «Экспрессия zisp, гена цинкового пальца DHHC, в сомитах и хрусталике во время эмбриогенеза рыбок данио». Gene Expr. Узоры. 2 (3–4): 355–8. DOI : 10.1016 / S1567-133X (02) 00021-2. PMID 12617825.
- Уэмура Т., Мори Х., Мишина М. (август 2002 г.). «Выделение и характеристика специфичного для аппарата Гольджи GODZ с доменом цинкового пальца DHHC». Biochem. Биофиз. Res. Commun. 296 (2): 492–6. DOI : 10.1016 / S0006-291X (02) 00900-2. PMID 12163046.
- Li B, Cong F, Tan CP, Wang SX, Goff SP (август 2002 г.). «Apdiv class="ht", белок с мотивом zf-DHHC, взаимодействует с c-Abl и обладает проапоптотической активностью». J. Biol. Chem. 277 (32): 28870–6. doi : 10.1074 / jbc.M202388200. PMID 12021275.
Внешние ссылки
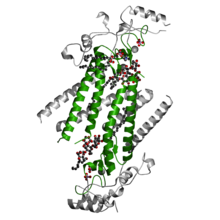 Димер белка DHHC от рыбок данио (PDB : 6BMS ), Показывая домен TM зеленым цветом. Спиральные домены вверху и внизу - это цитоплазматические домены DHHC.
Димер белка DHHC от рыбок данио (PDB : 6BMS ), Показывая домен TM зеленым цветом. Спиральные домены вверху и внизу - это цитоплазматические домены DHHC. Изображение топологии пальмитоилтрансфераз семейства DHHC. Трансмембранные альфа-спирали представлены черными трубками. Домен DHHC показан в виде светло-оранжевого овала.
Изображение топологии пальмитоилтрансфераз семейства DHHC. Трансмембранные альфа-спирали представлены черными трубками. Домен DHHC показан в виде светло-оранжевого овала.