 | |||
| |||
 | |||
| Имена | |||
|---|---|---|---|
| Название ИЮПАК Сульфаминовая кислота | |||
| Идентификаторы | |||
| Количество CAS | |||
| 3D модель ( JSmol ) | |||
| ЧЭБИ | |||
| ЧЭМБЛ | |||
| ChemSpider | |||
| ECHA InfoCard | 100.023.835 | ||
| Номер ЕС | |||
| PubChem CID | |||
| Номер RTECS | |||
| UNII | |||
| Номер ООН | 2967 | ||
| Панель управления CompTox ( EPA) | |||
ИнЧИ
| |||
Улыбки
| |||
| Характеристики | |||
| Химическая формула | H 3 NSO 3 | ||
| Молярная масса | 97,10 г / моль | ||
| Появление | белые кристаллы | ||
| Плотность | 2,15 г / см 3 | ||
| Температура плавления | 205 ° С (401 ° F, 478 К) разлагается | ||
| Растворимость в воде | Умеренный, с медленным гидролизом | ||
| Растворимость | |||
| Кислотность (p K a) | 1.0 | ||
| Опасности | |||
| Паспорт безопасности | ICSC 0328 | ||
| Классификация ЕС (DSD) (устаревшая) | Раздражающий ( Си) | ||
| R-фразы (устаревшие) | R36 / 38 R52 / 53 | ||
| S-фразы (устаревшие) | (S2) S26 S28 S61 | ||
| Родственные соединения | |||
| Другие катионы | Сульфамат аммония | ||
| Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |||
| | |||
| Ссылки на инфобоксы | |||
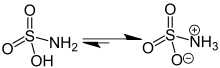
Сульфаминовая кислота, также известная как амидосульфоновая кислота, амидосерная кислота, аминосульфоновая кислота, сульфаминовая кислота и сульфамидная кислота, представляет собой молекулярное соединение с формулой H 3 NSO 3. Это бесцветное водорастворимое соединение находит множество применений. Сульфаминовой кислоты плавится при 205 ° С перед разложением при более высоких температурах в воде, триоксида серы, двуокиси серы и азота.
Сульфаминовая кислота (H 3 NSO 3) может считаться промежуточным соединением между серной кислотой (H 2 SO 4) и сульфамидом (H 4 N 2 SO 2), эффективно заменяя гидроксильную (–OH) группу амином (–NH 2) группа на каждом шагу. Эта картина не может распространяться дальше ни в одном направлении без разрушения сульфонильной (–SO 2 -) части. Сульфаматы - производные сульфаминовой кислоты.
Сульфаминовая кислота производится в промышленных масштабах путем обработки мочевины смесью триоксида серы и серной кислоты (или олеума ). Конвертация проводится в два этапа:
Таким образом, в 1995 году было произведено около 96 000 тонн.
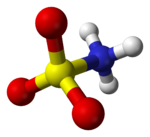 Шарообразная модель цвиттер-иона сульфаминовой кислоты в кристаллическом состоянии.
Шарообразная модель цвиттер-иона сульфаминовой кислоты в кристаллическом состоянии. Соединение хорошо описывается формулой H 3 NSO 3, а не таутомером H 2 NSO 2 (OH). Соответствующие расстояния связи составляют 1,44 Å для S = O и 1,77 Å для S – N. Большая длина S – N соответствует одинарной связи. Кроме того, нейтронографическое исследование обнаружило атомы водорода, все три из которых удалены от азота на 1,03 Å. В твердом состоянии молекула сульфаминовой кислоты хорошо описывается цвиттерионной формой.
Водные растворы сульфаминовой кислоты нестабильны и медленно гидролизуются до бисульфата аммония, но твердое кристаллическое вещество бесконечно стабильно при обычных условиях хранения. Его поведение напоминает поведение мочевины, (H 2 N) 2 CO. Обе имеют аминогруппы, связанные с электроноакцепторными центрами, которые могут участвовать в делокализованном связывании. Оба выделяют аммиак при нагревании в воде; однако сульфаминовая кислота превращается в серную кислоту вместо CO 2, который выделяет мочевина, в соответствии со следующей реакцией:
Сульфаминовая кислота является умеренно сильной кислотой, K a = 0,101 (p K a = 0,995). Поскольку твердое вещество не гигроскопично, оно используется в качестве стандарта в ацидиметрии (количественный анализ содержания кислоты).
Двойное депротонирование может быть выполнено в растворе аммиака с образованием аниона HNSO.2- 3.
С азотистой кислотой сульфаминовая кислота реагирует с образованием азота :
в то время как с азотной кислотой, она дает закись азота :
Реакция избытка гипохлорит- ионов с сульфаминовой кислотой или сульфаматной солью обратимо приводит к образованию как N- хлорсульфаматных, так и N, N- дихлорсульфамат-ионов.
Следовательно, сульфаминовая кислота используются в качестве гипохлорита акцептора при окислении альдегидов с хлоритом, такими как окисление Пинника.
При нагревании сульфаминовая кислота реагирует со спиртами с образованием соответствующих органосульфатов. Для этого он дороже других реагентов, таких как хлорсульфоновая кислота или олеум, но также значительно мягче и не сульфирует ароматические кольца. Продукты производятся в виде их солей аммония. Такие реакции могут катализироваться присутствием мочевины.
Без присутствия каких-либо катализаторов сульфаминовая кислота не будет реагировать с этанолом при температурах ниже 100 ° C.
Сульфаминовая кислота в основном является предшественником соединений со сладким вкусом. Реакция с циклогексиламином с последующим добавлением NaOH дает C 6 H 11 NHSO 3 Na, цикламат натрия. Родственные соединения также являются подсластителями, такими как ацесульфам калия.
Сульфаматы были использованы при разработке многих типов терапевтических агентов, таких как антибиотики, нуклеозид / нуклеотид вирус иммунодефицита человека (ВИЧ) ингибиторы обратной транскриптазы, ВИЧ ингибиторов протеазы (ИП), противораковые препараты ( стероидсульфатазы и карбоангидразы ингибиторов), анти эпилептического лекарства и лекарства для похудания.
Сульфаминовая кислота используется как кислотное чистящее средство и средство для удаления накипи, иногда в чистом виде или как компонент запатентованных смесей, обычно для металлов и керамики. Для целей очистки существуют разные степени очистки в зависимости от области применения, такие как GP Grade, SR Grade и TM Grade. Его часто используют для удаления ржавчины и известкового налета, заменяя более летучую и раздражающую соляную кислоту, которая дешевле. Он часто входит в состав бытового средства для удаления накипи, например, Lime-A-Way Thick Gel содержит до 8% сульфаминовой кислоты и имеет pH 2,0–2,2, или моющие средства, используемые для удаления известкового налета. По сравнению с большинством обычных сильных минеральных кислот сульфаминовая кислота обладает желательными свойствами удаления накипи с воды, низкой летучестью и низкой токсичностью. Образует водорастворимые соли кальция и трехвалентного железа.
Сульфаминовая кислота предпочтительнее соляной кислоты в быту из-за ее внутренней безопасности. При ошибочном смешивании с продуктами на основе гипохлорита, такими как отбеливатель, он не образует газообразного хлора, в отличие от большинства обычных кислот; реакция ( нейтрализация ) с аммиаком дает соль, как показано в разделе выше.
Он также находит применение при промышленной очистке молочного и пивоваренного оборудования. Хотя он считается менее коррозионным, чем соляная кислота, ингибиторы коррозии часто добавляют в коммерческие чистящие средства, в состав которых он входит. Его можно использовать как средство для удаления накипи для удаления накипи в домашних кофемашинах и кофемашинах эспрессо, а также в средствах для чистки зубных протезов.
Согласно этикетке на потребительском продукте, жидкое чистящее средство для серебра TarnX содержит тиомочевину, моющее средство и сульфаминовую кислоту.