 | |||
| |||
| Имена | |||
|---|---|---|---|
| Предпочтительное имя IUPAC Трииодметан | |||
| Другие названия Йодоформ;. Трииодид углерода | |||
| Идентификаторы | |||
| Номер CAS | |||
| 3D-модель (JSmol ) | |||
| Ссылка Beilstein | 1697010 | ||
| ChEBI | |||
| ChEMBL |
| ||
| ChemSpider | |||
| ECHA InfoCard | 100.000.795 | ||
| Номер EC |
| ||
| KEGG | |||
| MeSH | йодоформ | ||
| PubChem CID | |||
| номер RTECS |
| ||
| UNII | |||
| Панель управления CompTox (EPA ) | |||
InChI
| |||
УЛЫБКИ
| |||
| Свойства | |||
| Химическая формула | CHI 3 | ||
| Молярная масса | 393,732 г · моль | ||
| Внешний вид | Бледный, светло-желтый, непрозрачный кристаллы | ||
| Запах | Шафраноподобный | ||
| Плотность | 4,008 г см | ||
| Точка плавления | 119 ° C (246 ° F; 392 K) | ||
| Температура кипения | 218 ° C (424 ° F; 491 K) | ||
| Растворимость в воде | 100 мг л | ||
| Растворимость в диэтиловом эфире | 136 г L | ||
| Растворимость в ацетоне | 120 г L | ||
| Растворимость в этаноле | 78 г L | ||
| log P | 3,118 | ||
| Закон Генри. константа (kH) | 3,4 мкмоль Па кг | ||
| Магнитная восприимчивость (χ) | −117,1 · 10 см / моль | ||
| Структура | |||
| Кристаллическая структура | Гексагональная | ||
| Координационная геометрия | Тетрагональная | ||
| Молекулярная форма | Тетраэдр | ||
| Термохимия | |||
| Теплоемкость (C) | 157,5 ДжК моль | ||
| Стандартная энтальпия. образования (ΔfH298) | 180,1–182,1 кДж моль | ||
| Стандартная энтальпия. горения (ΔcH298) | −716,9 - −718,1 кДж моль | ||
| Фармакология | |||
| Код ATC | D09AA13 ( ВОЗ ) | ||
| Опасности | |||
| Пиктограммы GHS |  | ||
| Сигнальное слово GHS | Предупреждение | ||
| Краткие сведения об опасности GHS | H315, H319, H335 | ||
| Меры предосторожности GHS | P261, P280, P305 + 351 + 338 | ||
| NFPA 704 (огненный алмаз) |  0 2 1 0 2 1 | ||
| Вспышка пои nt | 204 ° C (399 ° F; 477 K) | ||
| Смертельная доза или концентрация (LD, LC): | |||
| LD50(средняя доза ) |
| ||
| NIOSH (пределы воздействия на здоровье в США): | |||
| PEL (допустимо) | нет | ||
| REL (рекомендуется) | 0,6 ppm (10 мг / м) | ||
| IDLH (непосредственная опасность) | ND | ||
| Родственные соединения | |||
| Родственные галоалканы | |||
| Родственные соединения | |||
| Если не указано иное, данные для материалов приведены в их стандартное состояние (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки ink | |||

Йодоформ ( также известный как трийодметан и, неточно, как трииодид углерода ), представляет собой йодорганическое соединение с формулой C H I 3. Бледно-желтое, кристаллическое, летучее вещество, оно имеет проникающий и характерный запах (в старых текстах по химии этот запах иногда упоминается как запах больниц, где это соединение до сих пор широко используется) и аналогично хлороформу, сладковатый вкус. Иногда его используют в качестве дезинфицирующего средства.
Молекула принимает тетраэдрическую молекулярную геометрию с симметрией C 3v.
Синтез йодоформа был первым описан Жоржем-Симоном Серулласом в 1822 г. реакциями паров йода с водяным паром над раскаленными углями, а также реакцией калия с этанольным йодом в присутствии воды; и почти в то же время независимо Джоном Томасом Купером. Он синтезируется в галоформной реакции реакцией йода и гидроксида натрия с любым из этих четырех видов органических соединений: метил кетон (CH 3 COR), ацетальдегид (CH 3 CHO), этанол (CH 3CH2OH) и некоторые вторичные спирты (CH 3 CHROH, где R представляет собой алкильную или арильную группу).
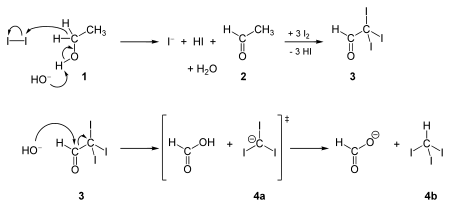
Реакция йода и основания с метил кетонами настолько надежна, что йодоформный тест (появление желтого осадка) используется для исследования наличие метилкетона. То же самое происходит при тестировании конкретных вторичных спиртов, содержащих по крайней мере одну метильную группу в альфа-положении.
. Некоторые реагенты (например, йодистый водород ) превращают йодоформ в дииодметан. Также возможно преобразование в диоксид углерода : йодоформ реагирует с водным нитратом серебра с образованием монооксида углерода. При обработке порошком элементарного серебра йодоформ восстанавливается, образуя ацетилен. При нагревании йодоформ разлагается с образованием двухатомного йода, газообразного йодистого водорода и углерода.
Гриб шляпка ангела содержит йодоформ и имеет характерный запах.
Соединение находит маломасштабное использование в качестве дезинфицирующего средства. Примерно в начале 20 века он использовался в медицине как заживляющая и антисептическая повязка на раны и язвы, хотя в настоящее время его заменяют более совершенные антисептики. Он является активным ингредиентом многих порошков для ушей собак и кошек, а также оксид цинка и пропионовая кислота, которые используются для предотвратить инфекцию и облегчить удаление волос в ушах.