 . Безводный . Безводный | |
 . Гексагидрат . Гексагидрат | |
| Имена | |
|---|---|
| Имена ИЮПАК Хром (III) хлорид. Хром трихлорид | |
| Другие названия Хромовый хлорид | |
| Идентификаторы | |
| Номер CAS |
|
| 3D-модель (JSmol ) | |
| ChEBI | |
| ChEMBL |
|
| ChemSpider | |
| DrugBank | |
| ECHA InfoCard | 100.030.023 |
| Справочник Гмелина | 1890 130477 532690 |
| PubChem CID | |
| номер RTECS |
|
| UNII | |
| CompTox Dashboard (EPA ) | |
InChI
| |
| Свойства | |
| Химическая формула | CrCl 3 |
| Молярная масса | 158,36 г / моль (безводный). 266,45 г / моль (гексагидрат) |
| Внешний вид | фиолетовый (безводный), темно-зеленый (гексагидрат) |
| Плотность | 2,87 г / см (безводный). 1,760 г / см (гексагидрат) |
| Температура плавления | 1,152 ° C (2106 ° F; 1425 K) (безводный). 83 ° C (гексагидрат) |
| Точка кипения | 1300 ° C (2370 ° F; 1570 K) разлагается |
| Растворимость в воде | малорастворимый (безводный). 585 г / л (гексагидрат) |
| Растворимость | нерастворим в этаноле. нерастворим в эфире, ацетоне |
| Кислотность ( pK a) | 2,4 (0,2М раствор) |
| Магнитная восприимчивость (χ) | + 6890,0 · 10 см / моль |
| Структура | |
| Кристаллическая структура | YCl 3 структура |
| Координационная геометрия | Октаэдрическая |
| Опасности | |
| Паспорт безопасности | ICSC 1316 (безводный). ICSC 1532 (гексагидрат) |
| Пиктограммы GHS |    |
| Сигнальное слово GHS | Опасность |
| Краткая характеристика опасности GHS | H302, H314, H318, H401, H411 |
| Меры предосторожности GHS | P260, P264, P270, P273, P280, P301 + 312, P301 + 330 + 331, P303 + 361 + 353, P304 + 340, P305 + 351 + 338, P310, P321, P3 30, P363, P391, P405, P501 |
| NFPA 704 (огненный алмаз) |  0 3 0 0 3 0 |
| Температура возгорания | Невоспламеняющийся |
| Смертельная доза или концентрация (LD, LC): | |
| LD50(средняя доза ) | 1870 мг / кг (перорально, крыса) |
| NIOSH ( Пределы воздействия на здоровье в США): | |
| PEL (Допустимо) | TWA 1 мг / м |
| REL (Рекомендуется) | TWA 0,5 мг / м |
| IDLH ( Непосредственная опасность) | 250 мг / м |
| Родственные соединения | |
| Другие анионы | Фторид хрома (III). Бромид хрома (III). Иодид хрома (III) |
| Другие катионы | хлорид молибдена (III). хлорид вольфрама (III) |
| родственные соединения | хлорид хрома (II). хлорид хрома (IV) |
| Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |
| Ссылки на информационные панели | |
Хром (III) хлорид (также называемый хлорид хрома ) описывает любое из нескольких соединений формулы CrCl 3 • x H2O, где x может быть 0, 5 и 6. Безводное соединение с формулой CrCl 3 представляет собой твердое вещество фиолетового цвета. Наиболее распространенной формой трихлорида является темно-зеленый гексагидрат CrCl 3 • 6 H2O. Хлориды хрома находят применение в качестве катализаторов и в качестве предшественников красителей для шерсти.
Безводный хлорид хрома (III) принимает Структура YCl 3, в которой Cr занимает одну треть октаэдрических пустот в чередующихся слоях псевдо- кубической плотноупакованной решетки ионов Cl. Отсутствие катионов в чередующихся слоях приводит к слабой связи между соседними слоями. По этой причине кристаллы CrCl 3легко раскалываются по плоскостям между слоями, что приводит к образованию чешуек (слюдистых ) образцов хлорида хрома (III).

Пространство- Модель заполнения кубической плотной упаковки хлорид-ионов в кристаллической структуре CrCl 3

Шаровая модель части слоя

Укладка слоев
Хлориды хрома (III) демонстрируют несколько необычное свойство присутствия в нескольких различных химических формах (изомерах), которые различаются количеством хлорид-анионов, координированных с Cr (III), и кристаллизационная вода. Различные формы существуют как в твердом виде, так и в водных растворах. Известно несколько членов ряда [CrCl 3-n (H2O)n]. Основной гексагидрат можно более точно описать как [CrCl 2(H2O)4] Cl • 2 H2O. Он состоит из транс- катиона [CrCl 2(H2O)4] и дополнительных молекул воды и хлорид-аниона в решетке. Известны два других гидрата, бледно-зеленый [CrCl (H 2O)5] Cl 2• H2O и фиолетовый [Cr (H 2O)6] Cl 3). Аналогичное поведение наблюдается с другими соединениями хрома (III).
Безводный хлорид хрома (III) может быть получен хлорированием металла хром напрямую или косвенно карботермическим методом хлорирование оксида хрома (III) при 650–800 ° C
Дегидратация триметилсилилхлоридом в ТГФ дает сольват:
Его также можно получить обработкой гексагидрата с тионилхлоридом :
Гидратированные хлориды получают обработкой хромата соляной кислотой и метанолом.
Низкие скорости реакции обычны для хрома (III) c комплексы. Низкую реакционную способность иона d Cr можно объяснить с помощью теории кристаллического поля. Одним из способов раскрытия CrCl 3 до замещения в растворе является уменьшение даже следовых количеств до CrCl 2, например, используя цинк в соляной кислоте.. Это соединение хрома (II) легко подвергается замещению, и оно может обмениваться электронами с CrCl 3 через хлорид мостик, позволяя всему CrCl 3 быстро реагировать.
Однако в присутствии некоторого количества хрома (II) твердый CrCl 3 быстро растворяется в воде. Точно так же реакции замещения лиганда в растворах [CrCl 2(H2O)4] ускоряются хромовыми (II) катализаторами.
С расплавленными хлоридами щелочных металлов, такими как хлорид калия, CrCl 3 дает соли типа M 3 CrCl 6 и K 3Cr2Cl9, который также является октаэдрическим, но в котором два хрома связаны тремя хлоридными мостиками.
CrCl 3 представляет собой кислоту Льюиса, классифицируемую как «твердую» в соответствии с жестко-мягкой кислотой. -Базовая теория. Он образует множество аддуктов типа [CrCl 3L3], где L представляет собой основание Льюиса. Например, он реагирует с пиридином (C. 5H. 5N) с образованием аддукта:
Обработка триметилсилилхлоридом в THF дает безводный комплекс THF:
Хлорид хрома (III) используется в качестве предшественника многих хроморганических соединений, например, бис (бензол) хром, аналог ферроцена :
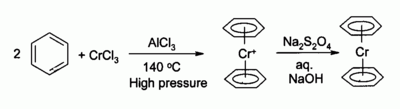
Фосфиновые комплексы, полученные из CrCl 3, катализируют тримеризацию этилена в 1-гексен.
Одним из нишевых вариантов использования CrCl 3 в органическом синтезе является получение in situ хлорид хрома (II), реагент для восстановления алкилгалогенидов и для синтеза (E) -алкенилгалогенидов. Реакцию обычно проводят с использованием двух моль CrCl 3 на моль лития а гидрид люминия, хотя, если подходят водные кислотные условия, может быть достаточно цинка и соляной кислоты.
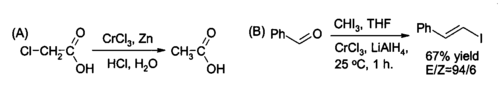
Хлорид хрома (III) также использовался в качестве кислоты Льюиса в органических реакциях, например, для катализа нитрозо реакции Дильса-Альдера.
Ряд хромсодержащих красителей используются в коммерческих целях для шерсти. Типичными красителями являются триарилметаны, состоящие из производных орто-гидроксилбензойной кислоты.
Хотя трехвалентный хром гораздо менее ядовит, чем шестивалентный, соли хрома обычно считаются токсичными.
| Викискладе есть материалы, связанные с хлоридом хрома (III). |