В органической химии, нитрование - это общий класс химических процессов для введения нитро группы в органическое соединение. Этот термин также неправильно применяется к другому процессу образования нитратных сложных эфиров между спиртами и азотной кислотой (как это происходит в синтезе нитроглицерин ). Разница между полученными молекулярными структурами нитросоединений и нитратов состоит в том, что атом азота в нитросоединениях непосредственно связан с не- атомом кислорода (обычно с углеродом или другим атомом азота), тогда как в сложных нитратных эфирах (также называемых органическими нитратами) азот связан с атомом кислорода, который в свою очередь, обычно связан с атомом углерода (нитритогруппа).
Существует множество основных промышленных применений нитрования в строгом смысле слова; наиболее важны по объему для производства нитроароматических соединений, таких как нитробензол. Реакции нитрования, в частности, используются для производства взрывчатых веществ, например, превращение гуанидина в нитрогуанидин и превращение толуола в тринитротолуол (ТНТ). Однако они имеют большое значение как химические промежуточные продукты и предшественники. Ежегодно производятся миллионы тонн нитроароматических углеводородов.
В типичных синтезах нитрования применяется так называемая «смешанная кислота», смесь концентрированной азотной кислоты и серной кислоты. Эта смесь дает ион нитрония (NO 2), который является активным веществом в ароматическом нитровании . Этот активный ингредиент, который может быть выделен в случае тетрафторбората нитрония, также обеспечивает нитрование без необходимости в смешанной кислоте. При смешанном кислотном синтезе серная кислота не расходуется и, следовательно, действует как катализатор, а также как поглотитель воды. В случае нитрования бензола реакцию проводят при теплой температуре, не превышающей 50 ° C. Этот процесс является одним из примеров электрофильного ароматического замещения, который включает атаку богатым электронами бензольным кольцом:
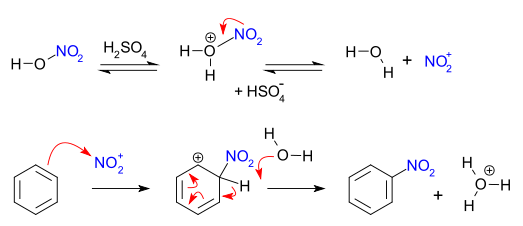
Также были предложены альтернативные механизмы, включая один, связанный с переносом одного электрона. (SET).
Селективность может быть проблемой при нитровании, потому что, как правило, может получиться более одного соединения, но желательно только одно, поэтому альтернативные продукты действуют как загрязняющие вещества или просто выбрасываются.. Соответственно, желательно разрабатывать синтезы с подходящей селективностью; например, контролируя условия реакции, флуоренон можно селективно тринитрировать или тетранитрировать.
Заместители в ароматических кольцах влияют на скорость этого электрофильного ароматического соединения. замена. Деактивирующие группы, такие как другие нитро группы, обладают эффектом акцептирования электронов. Такие группы дезактивируют (замедляют) реакцию и направляют электрофильный ион нитрония на атаку ароматического мета-положения. Дезактивирующие мета-направляющие заместители включают сульфонил, циано группы, кето, сложные эфиры и карбоксилаты. Нитрование можно ускорить с помощью активирующих групп, таких как амино, гидрокси и метил группы, а также амиды и простые эфиры с образованием пара- и орто-изомеров.
Прямое нитрование анилина с помощью азотной кислоты и серной кислоты, согласно одному источнику, приводит к смеси 50/50 пара - и изомеры мета-нитроанилина. В этой реакции быстро реагирующий и активирующий анилин (ArNH 2) находится в равновесии с более многочисленным, но менее реактивным (дезактивированным) ионом анилиния (ArNH 3), что может объяснить это распределение продуктов реакции. Согласно другому источнику, более контролируемое нитрование анилина начинается с образования ацетанилида в результате реакции с уксусным ангидридом с последующим фактическим нитрованием. Поскольку амид представляет собой обычную активирующую группу, образующиеся продукты представляют собой пара- и орто-изомеры. Нагревания реакционной смеси достаточно для обратного гидролиза амида до нитрованного анилина.
В реакции Вольфенштейна – Бетерса бензол реагирует с азотной кислотой и нитратом ртути (II) с образованием пикриновой кислоты.
С арилхлоридами трифлаты и нонафлаты ипсо-замещение также может происходить в так называемом ипсо-нитровании . Фраза была впервые использована Перрином и Скиннером в 1971 году при исследовании нитрования хлоранизола. В одном протоколе 4-хлор-н-бутилбензол реагирует с нитритом натрия в трет-бутаноле в присутствие 0,5 мол.% Pd2(dba) 3, биарилфосфинового лиганда и катализатора фазового переноса в 4-нитро-н-бутилбензол.