 | |
 | |
 | |
| Имена | |
|---|---|
| Предпочтительное название IUPAC Пропан-1,2,3-триил тринитрат | |
Другие названия * 1,2,3-Трис (нитроокси) пропан
| |
| Идентификаторы | |
| Номер CAS | |
| 3D-модель (JSmol ) | |
| Ссылка Beilstein | 1802063 |
| ChEBI | |
| ChEMBL |
|
| ChemSpider | |
| DrugBank | |
| ECHA InfoCard | 100.000.219 |
| Номер EC |
|
| Справочник Гмелина | 165859 |
| IUPHAR / BPS | |
| KEGG | |
| MeSH | Нитроглицерин |
| PubChem CID | |
| UNII | |
| Номер ООН | 0143, 0144, 1204, 3064, 3319 |
| Панель управления CompTox (EPA ) | |
InChI
| |
УЛЫБКИ
| |
| Свойства | |
| Химическая формула | C3H5N3O9 |
| Молярная масса | 227,085 г · моль |
| Внешний вид | Бесцветная жидкость |
| Плотность | 1,6 г⋅см (при 15 ° C) |
| Температура плавления | 14 ° C (57 ° F; 287 K) |
| Температура кипения | 50 ° C (122 ° F; 323 K) Взрывается |
| Растворимость в воде | Незначительно |
| Растворимость | Ацетон, эфир, бензол, спирт |
| log P | 2,154 |
| Структура | |
| Координационная геометрия |
|
| Молекулярная форма |
|
| Взрывоопасные данные | |
| Чувствительность к удару | Высокая |
| Чувствительность к трению | Высокая |
| Скорость детонации | 7700 м⋅с |
| Фактор RE | 1,50 |
| Термохимия | |
| Стандартная энтальпия образования. (ΔfH298) | −370 кДж⋅моль |
| Стандартная энтальпия. сгорание (ΔcH298) | -1,529 МДж⋅моль |
| Фармакология | |
| Код АТС | C01DA02 (ВОЗ ) C05AE01 (ВОЗ ) |
| Беременность. категория |
|
| Способы. введения | Внутривенно, перорально, под язык, местно |
| Фармакокинетика : | |
| Биодоступность | <1% |
| Метаболизм | Печень |
| Период полувыведения | 3 мин |
| Правовой статус |
|
| Опасности | |
| Основные опасности | Взрывоопасные, токсичные |
| Пиктограммы GHS |     |
| Сигнальное слово GHS | Опасно |
| Формулировки опасностей GHS | H202, H205, H241, H301, H311, H331, H370 |
| Меры предосторожности GHS | P210, P243, P250, P260, P264, P270, P271, P280, P302 + 352, P410 |
| NFPA 704 (огненный алмаз) |  2 3 4 2 3 4 |
| NIOSH (пределы воздействия на здоровье в США): | |
| PEL (допустимое) | C 0,2 ppm (2 мг / м) [кожа] |
| ссылки на инфобокс | |
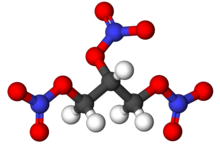
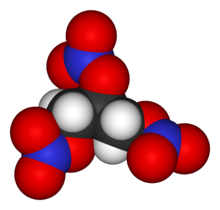
нитроглицерин (NG), также известный как нитроглицерин, тринитроглицерин (TNG ), нитро, тринитрат глицерина (GTN ) или 1,2,3-тринитроксипропан, представляет собой плотный, бесцветный, маслянистый, взрывчатое вещество жидкость, чаще всего производимая нитрованием глицерина с белым дымом азотной кислоты в условиях, подходящих для образования эфира азотной кислоты . Химически это вещество представляет собой органическое нитратное соединение, а не нитросоединение, однако традиционное название часто сохраняется. Изобретенный в 1847 году, нитроглицерин с тех пор используется в качестве активного ингредиента при производстве взрывчатых веществ, в основном динамита, и как таковой он используется в строительстве, снос и горнодобывающая промышленность. С 1880-х годов он использовался военными в качестве активного ингредиента и желатинизатора для нитроцеллюлозы, в некоторых твердых ракетных топливах, таких как кордит и баллистит.
Нитроглицерин является одним из основных компонентов бездымных порохов двойной основы, используемых в перезарядных устройствах. Сотни комбинаций пороха в сочетании с нитроцеллюлозой используются в перезарядных устройствах для винтовок, пистолетов и дробовиков.
В медицине более 130 лет нитроглицерин использовался как сильнодействующее вазодилататор (расширение сосудистой системы) для лечения заболеваний сердца, таких как стенокардия и хроническая сердечная недостаточность. Хотя ранее было известно, что эти положительные эффекты обусловлены превращением нитроглицерина в оксид азота, сильнодействующее венодилататор, ферментом для этого преобразования не было обнаружено митохондриальная альдегиддегидрогеназа (ALDH2 ) до 2002 года. Нитроглицерин доступен в сублингвальных таблетках, спреях, мазях и пластырях.
Нитроглицерин был первым произведенным взрывчатым веществом, которое было сильнее черного пороха. Впервые он был синтезирован итальянским химиком Асканио Собреро в 1847 году, работая под руководством Теофиля-Жюля Пелуза в Туринском университете. Собреро первоначально назвал свое открытие пироглицерином и решительно предостерегал от его использования в качестве взрывчатого вещества.
Нитроглицерин был позже принят в качестве коммерчески полезного взрывчатого вещества Альфредом Нобелем, который экспериментировал с более безопасными способами обращения с опасными веществами. комплекс после его младшего брата, Эмиля Оскара Нобеля, и нескольких заводских рабочих были убиты в результате взрыва на оружейном заводе Нобельса в 1864 году в Хеленеборге, Швеция.
Год спустя Нобель основал Alfred Nobel and Company в Германии и построил изолированную фабрику на Krümmel холмах Geesthacht около Гамбурга. Этот бизнес экспортировал жидкую комбинацию нитроглицерина и пороха под названием «Blasting Oil», но это было крайне нестабильно и с трудом справляться, о чем свидетельствуют многочисленные катастрофы. Здания фабрики Крюммеля были дважды разрушены.
В апреле 1866 года три ящика нитроглицерина были отправлены в Калифорнию для Центрально-Тихоокеанской железной дороги, где планировалось провести эксперимент. с его помощью в качестве взрывчатого вещества для ускорения строительства 1659 футов (506 м) Summit Tunnel через горы Сьерра-Невада. Один из ящиков взорвался, разрушив офис компании Wells Fargo в Сан-Франциско и погибли 15 человек. Это привело к полному запрету на провоз жидкого нитроглицерина в Калифорнии. Таким образом, производство нитроглицерина на месте потребовалось для оставшихся твердых пород буровзрывных работ, необходимых для завершения Первой трансконтинентальной железной дороги в Северной Америке.
в В июне 1869 года два однотонных фургона, загруженных нитроглицерином, в то время известном как Powder-Oil, взорвались на дороге в деревне Cwm-Y-Glo в Северном Уэльсе. Взрыв привел к гибели шести человек, множеству ранений и значительному ущербу для села. От двух лошадей не было обнаружено никаких следов. Правительство Великобритании было настолько встревожено нанесенным ущербом и тем, что могло произойти в городе (эти две тонны были частью более крупного груза, идущего из Германии через Ливерпуль), что вскоре они приняли Закон о нитроглицерине 1869 года. Жидкий нитроглицерин был также широко запрещен в других странах, и эти правовые ограничения привели к тому, что Альфред Нобель и его компания в 1867 году разработали динамит. Это было сделано путем смешивания нитроглицерина с диатомовой землей («Кизельгур» на немецком языке) найден на холмах Крюммель. Подобные смеси, такие как «дуалин» (1867), «литофрактер» (1869) и «гелигнит » (1875), были образованы путем смешивания нитроглицерина с другими инертными абсорбентами, и многие комбинации были опробованы другими компании в попытках обойти жестко закрепленные патенты Нобеля на динамит.
Смеси динамита, содержащие нитроцеллюлозу, которая увеличивает вязкость смеси, обычно известны как «желатины».
После открытия, что амилнитрит помогает облегчить боль в груди, врач Уильям Мюррелл экспериментировал с использованием нитроглицерина для облегчения стенокардии и уменьшения артериальное давление. Он начал лечить своих пациентов небольшими разбавленными дозами нитроглицерина в 1878 году, и это лечение вскоре стало широко использоваться после того, как Мюррелл опубликовал свои результаты в журнале The Lancet в 1879 году. За несколько месяцев до своей смерти в 1896 году. Альфреду Нобелю прописали нитроглицерин из-за этого сердечного заболевания, и он написал другу: «Разве не по иронии судьбы, что мне прописали нитроглицерин для внутреннего приема! Они называют его Тринитрин, чтобы не напугать химик и общественность ". По той же причине в медицинском учреждении также использовалось название «тринитрат глицерина».
Большие количества нитроглицерина были произведены во время Первой мировой войны и Второй мировой войны для использования в качестве военного топлива и в военно-инженерная работа. Во время Первой мировой войны завод HM, Гретна, крупнейший завод по производству топлива в Великобритании, производил около 800 тонн кордита RDB в неделю. Для этого количества требовалось не менее 336 тонн нитроглицерина в неделю (при условии отсутствия производственных потерь). Королевский флот имел собственный завод на Кордитовой фабрике Королевского флота, Холтон-Хит, Дорсет, Англия. Большой завод по производству кордита был также построен в Канаде во время Первой мировой войны. Завод по производству кордита Canadian Explosives Limited в Нобель, Онтарио был спроектирован для производства 1 500 000 фунтов (680 т) кордита на в месяц, требуя около 286 тонн нитроглицерина в месяц.
В чистом виде нитроглицерин является контактным взрывчатым веществом, которое взрывается при физическом шоке, и со временем оно разлагается до еще более нестабильных форм.. Это делает нитроглицерин очень опасным для транспортировки и использования. В неразбавленном виде это одно из самых мощных взрывчатых веществ в мире, сравнимое с недавно разработанными RDX и PETN.
. В начале своей истории было обнаружено, что жидкий нитроглицерин «десенсибилизированный "путем охлаждения примерно до 5-10 ° C (40-50 ° F). При этой температуре нитроглицерин замерзает, сжимаясь при затвердевании. Размораживание может вызвать повышенную чувствительность, особенно если присутствуют загрязнения или слишком быстрое нагревание. Химически «десенсибилизировать» нитроглицерин можно до такой степени, что он может считаться таким же «безопасным», как современные взрывчатые вещества, например, путем добавления примерно от 10 до 30% этанола, ацетон или динитротолуол (процентное содержание зависит от используемого десенсибилизирующего агента). Десенсибилизация требует дополнительных усилий для восстановления «чистого» продукта. В противном случае следует полагать, что десенсибилизированный нитроглицерин будет значительно труднее взорвать, что может сделать его бесполезным в качестве взрывчатого вещества для практического применения.
Серьезная проблема при использовании нитроглицерина связана с его высокой температурой замерзания 13 ° C (55 ° F). Твердый нитроглицерин гораздо менее чувствителен к ударам, чем жидкость, что является обычным явлением для взрывчатых веществ. В прошлом нитроглицерин часто транспортировали в замороженном состоянии, но это приводило к большому количеству несчастных случаев во время процесса оттаивания непосредственно перед его использованием. Этот недостаток преодолевается за счет использования смесей нитроглицерина с другими полинитратами. Например, смесь нитроглицерина и динитрата этиленгликоля замерзает при -29 ° C (-20 ° F).
Нитроглицерин и любые разбавители, безусловно, могут сжечь (сжечь). Взрывная сила нитроглицерина происходит от детонации : энергия начального разложения вызывает сильную волну давления, которая взрывает окружающее топливо. Это самоподдерживающаяся ударная волна, которая распространяется через взрывоопасную среду со скоростью, в 30 раз превышающей скорость звука, как почти мгновенное разложение топлива под давлением в раскаленный добела газ. При детонации нитроглицерина образуются газы, которые занимают более чем в 1200 раз исходный объем при обычной комнатной температуре и давлении. Выделяющееся тепло поднимает температуру примерно до 5000 ° C (9000 ° F). Это полностью отличается от дефлаграции, которая зависит исключительно от доступного топлива, независимо от давления или удара. Разложение приводит к гораздо более высокому отношению энергии к молям выделяемого газа по сравнению с другими взрывчатыми веществами, что делает его одним из самых горячих детонирующих бризантных взрывчатых веществ.
Нитроглицерин может быть получен путем кислотного катализа нитрования глицерин (глицерин).
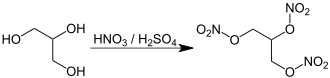 Синтез нитроглицерина:
Синтез нитроглицерина: В процессе промышленного производства часто реагирует глицерин со смесью концентрированной серной кислоты и концентрированной азотной кислоты почти 1: 1. Это может быть получено путем смешивания белой дымящей азотной кислоты - довольно дорогой чистой азотной кислоты, в которой удалены оксиды азота, в отличие от красной дымящей азотной кислоты, который содержит оксиды азота - и концентрированную серную кислоту. Чаще эту смесь получают более дешевым методом смешивания дымящей серной кислоты, также известной как олеум - серной кислоты, содержащей избыток триоксида серы - и азеотропная азотная кислота (состоящая примерно из 70% азотной кислоты, остальное - вода).
серная кислота производит протонированные азотные кислоты разновидностей, которые атакуются глицерином нуклеофильными атомы кислорода. Таким образом, нитро группа добавляется в виде сложного эфира C-O-NO 2 и образуется вода. Это отличается от реакции электрофильного ароматического замещения, в которой ионы нитрония являются электрофилом.
. Добавление глицерина приводит к экзотермической реакции ( т.е. выделяется тепло), как обычно при смешанном кислотном азотировании. Если смесь становится слишком горячей, это приводит к неуправляемой реакции, состоянию ускоренного нитрования, сопровождающемуся деструктивным окислением органических материалов горячей азотной кислотой и выделением ядовитого диоксид азота газ с высоким риском взрыва. Таким образом, смесь глицерина медленно добавляют в реакционный сосуд, содержащий смешанную кислоту (а не кислоту по отношению к глицерину). Нитратор охлаждают холодной водой или какой-либо другой охлаждающей смесью и поддерживают на протяжении всего добавления глицерина при температуре около 22 ° C (72 ° F), намного ниже которой этерификация происходит слишком медленно, чтобы ее можно было использовать. Емкость нитратора, часто сделанная из железа или свинца и обычно перемешиваемая сжатым воздухом, имеет в основании аварийный люк, который нависает над большим бассейном. очень холодной воды, в которую может быть сброшена вся реакционная смесь (называемая зарядом), чтобы предотвратить взрыв, процесс, называемый утоплением. Если температура заряда превышает примерно 30 ° C (86 ° F) (фактическое значение зависит от страны) или в вентиляционном отверстии нитратора появляются коричневые пары, то он немедленно тонет.
Основное применение нитроглицерина по тоннажу - это взрывчатые вещества, такие как динамит, и топливо.
Нитроглицерин - маслянистая жидкость, которая может взорваться при воздействии тепла, удара или пламени.
Альфред Нобель разработал использование нитроглицерина в качестве взрывчатого вещества путем смешивания нитроглицерина с инертными абсорбентами, в частности «кизельгуром» или диатомитовой землей. Он назвал это взрывчатое вещество динамит и запатентовал его в 1867 году. Оно было поставлено готовым к использованию в виде палочек, индивидуально завернутых в промасленную водонепроницаемую бумагу. Динамит и аналогичные взрывчатые вещества широко использовались для задач гражданского строительства, таких как бурение шоссе и железнодорожных туннелей, для горных работ., для очистки сельскохозяйственных угодий от пней, в разработке карьеров и в сносе зданий. Точно так же военные инженеры использовали динамит для строительных и сносных работ.
Нитроглицерин также использовался в качестве ингредиента в военном топливе для использования в огнестрельном оружии.
Нитроглицерин использовался в сочетании с гидроразрывом пласта, процессом, используемым для извлечения нефть и газ из сланцев пластов. Этот метод включает вытеснение и детонацию нитроглицерина в естественных или гидравлически индуцированных системах трещин или вытеснение и детонацию нитроглицерина в гидравлически индуцированных трещинах с последующими выстрелами из ствола скважины с использованием гранулированного TNT.
Нитроглицерин имеет преимущество перед некоторыми другими взрывчатыми веществами, которые при детонации практически не производит видимого дыма. Таким образом, он может быть использован в качестве ингредиента в составе различных видов бездымного пороха.
 в заявке на патент Альфреда Нобеля от 1864
в заявке на патент Альфреда Нобеля от 1864  , запряженной лошадьми, для нитроглицерина на Востоке. Толедо, Огайо, 1890 г.
, запряженной лошадьми, для нитроглицерина на Востоке. Толедо, Огайо, 1890 г. Его чувствительность ограничивает применимость нитроглицерина в качестве военной взрывчатки и менее чувствительных взрывчатых веществ, таких как TNT, RDX и HMX <354.>Во многом заменили его в боеприпасах. Он остается важным в военной инженерии, и саперы до сих пор используют динамит.
Альфред Нобель затем разработал баллистит, объединив нитроглицерин и пушистый хлопок. Он запатентовал его в 1887 году. Баллистит был принят на вооружение правительствами ряда европейских стран в качестве военного топлива. Италия была первой, кто его принял. Британское правительство и правительства Содружества взамен приняли кордит, который был разработан сэром Фредериком Абелем и сэром Джеймсом Дьюаром из Соединенного Королевства в 1889 году. Оригинал Кордит Mk I состоял из 58% нитроглицерина, 37% хлопка и 5,0% вазелина. И баллистит, и кордит изготавливались в виде «шнуров».
Бездымный порох изначально был разработан с использованием нитроцеллюлозы в качестве единственного взрывчатого ингредиента. Поэтому они были известны как одноосновное топливо. Также был разработан ряд бездымных порохов, которые содержат как нитроцеллюлозу, так и нитроглицерин, известные как двухосновные пропелленты. Изначально бездымные пороха поставлялись только для использования в военных целях, но вскоре они были разработаны и для гражданского использования, и их быстро применили в спорте. Некоторые из них известны как спортивные порошки. Пропелленты на тройной основе содержат нитроцеллюлозу, нитроглицерин и нитрогуанидин, но предназначены в основном для боеприпасов сверхбольшого калибра, таких как те, которые используются в танковых пушках и морской артиллерии. Желатин для взрывных работ, также известный как гелигнит, был изобретен компанией Nobel в 1875 году с использованием нитроглицерина, древесной массы и натрия или нитрата калия. Это было раннее, дешевое, гибкое взрывное устройство.
Нитроглицерин относится к группе препаратов, называемых нитратами, в которую входят многие другие нитраты, такие как динитрат изосорбида (Изордил) и мононитрат изосорбида (Имдур, Исмо, Монокет). Все эти агенты проявляют свой эффект, превращаясь в оксид азота в организме митохондриальной альдегиддегидрогеназой (ALDH2 ), а оксид азота является мощным естественным сосудорасширяющим средством.
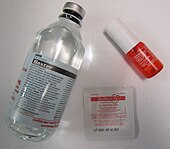 Нитроглицерин в трех различных формах: внутривенный, сублингвальный спрей и нитроглицериновый пластырь.
Нитроглицерин в трех различных формах: внутривенный, сублингвальный спрей и нитроглицериновый пластырь. В медицине нитроглицерин используется при стенокардии, болезненном симптоме ишемическая болезнь сердца, вызванная недостаточным притоком крови и кислорода к сердцу и являющаяся мощным антигипертензивным средством. Нитроглицерин корректирует дисбаланс между потоком кислорода и крови к сердцу. В низких дозах нитроглицерин расширяет вены больше, чем артерии, тем самым уменьшая преднагрузку (объем крови в сердце после наполнения); это считается его основным механизмом действия. Снижая предварительную нагрузку, сердце перекачивает меньше крови, что снижает потребность в кислороде, поскольку сердцу не приходится работать так тяжело. Кроме того, меньшая преднагрузка снижает трансмуральное давление желудочков (давление, оказываемое на стенки сердца), что снижает компрессию сердечных артерий, позволяя большему количеству крови проходить через сердце. В более высоких дозах он также расширяет артерии, тем самым уменьшая постнагрузку (уменьшая давление, против которого должно работать сердце). Повышение потребности миокарда в кислороде по сравнению с соотношением доставки кислорода приводит к следующим терапевтическим эффектам во время приступов стенокардии: уменьшение боли в груди, снижение артериального давления, увеличение частоты сердечных сокращений и ортостатическая гипотензия. Пациенты, страдающие стенокардией при выполнении определенных физических нагрузок, часто могут предотвратить симптомы, приняв нитроглицерин за 5-10 минут до активности. Передозировка может вызвать метгемоглобинемию.
. Нитроглицерин доступен в виде таблеток, мази, раствора для внутривенного использования, трансдермальных пластырей или спреев, вводимых сублингвально. Некоторые формы нитроглицерина сохраняются в организме намного дольше, чем другие. Было показано, что постоянное воздействие нитратов приводит к тому, что организм перестает нормально реагировать на это лекарство. Специалисты рекомендуют снимать пластыри на ночь, позволяя организму через несколько часов восстановить свою чувствительность к нитратам. Препараты нитроглицерина короткого действия можно использовать несколько раз в день с меньшим риском развития толерантности. Впервые нитроглицерин был использован Уильямом Мюрреллом для лечения приступов стенокардии в 1878 году, и в том же году было опубликовано открытие.
Редкое воздействие высоких доз нитроглицерина может вызывают сильную головную боль, известную как «н.г. голова» или «удар головой». Эти головные боли могут быть достаточно сильными, чтобы вывести из строя некоторых людей; однако у людей развиваются толерантность и зависимость от нитроглицерина после длительного воздействия. Отмена может быть фатальной, хотя и редко. Симптомы отмены включают боль в груди и другие проблемы с сердцем. Эти симптомы могут быть облегчены повторным воздействием нитроглицерина или других подходящих органических нитратов.
Для рабочих на предприятиях по производству нитроглицерина (NTG) последствия отмены иногда включают «воскресные сердечные приступы» у тех, кто регулярно подвергается воздействию нитроглицерина. на рабочем месте, что приводит к развитию толерантности к венодилатирующим эффектам. В выходные рабочие теряют толерантность, и когда они снова подвергаются воздействию в понедельник, резкое расширение сосудов вызывает учащенное сердцебиение, головокружение и головную боль, это называется как «болезнь понедельника».
Люди могут подвергнуться воздействию нитроглицерина на рабочем месте, вдыхая его, впитывая в кожу, проглатывая его или контактируя с глазами. Управление по охране труда установило юридический предел (допустимый предел воздействия ) для воздействия нитроглицерина на рабочем месте, равный 0,2 ppm (2 мг / м 2) воздействия на кожу в течение 8 часов. рабочий день. Национальный институт охраны труда установил рекомендуемый предел воздействия 0,1 мг / м3 воздействия на кожу в течение 8-часового рабочего дня. При уровне 75 мг / м3 нитроглицерин немедленно опасен для жизни и здоровья.