 | |
 | |
| Имена | |
|---|---|
| Название IUPAC Формиат аммония | |
| Идентификаторы | |
| Номер CAS | |
| 3D-модель (JSmol ) | |
| ChemSpider | |
| ECHA InfoCard | 100.007.959 |
| PubChem CID | |
| Номер RTECS |
|
| UNII | |
| Панель управления CompTox (EPA ) | |
InChI
| |
УЛЫБКИ
| |
| Свойства | |
| Химическая формула | CH5NO2 |
| Молярная масса | 63,056 г · моль |
| Внешний вид | Белые моноклинные кристаллы, расплывающиеся на воздухе |
| Запах | Слегка аммиачный |
| Плотность | 1,26 г / см |
| Температура плавления | 116 ° C (241 ° F; 389 K) |
| Точка кипения | 180 ° C (356 ° F; 453 K). разлагается |
| Растворимость в воде | (граммы на 100 г воды) 102 г (0 ° C). 142,7 г (20 ° C). 202,4 г (40 ° C). 516 г (80 ° C) |
| Растворимость в других растворителях | Растворим в жидкости аммиак, спирт, диэтиловый эфир |
| Термохимия | |
| Стандартная энтальпия образования. (ΔfH298) | -556,18 кДж / моль |
| Опасности | |
| Паспорт безопасности | JT Baker MSDS |
| Пиктограммы GHS |  |
| Сигнальное слово GHS | Предупреждение |
| Предупреждения об опасности GHS | H315, H319, H335 |
| Меры предосторожности GHS | P261, P305 + 351 + 338 |
| NFPA 704 (огненный алмаз) |  1 2 1 1 2 1 |
| Смертельная доза или концентрация (LD, LC) : | |
| LD50(средняя доза ) | 410 мг / кг (мыши, внутривенно) |
| Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F ], 100 кПа). | |
| Ссылки в ink | |
Формиат аммония, NH 4 HCO 2, это аммоний соль муравьиной кислоты. Это бесцветное, гигроскопичное, кристаллическое твердое вещество.
Ацетон может быть преобразован в изопропиламин следующим образом:
Чистый формиат аммония при нагревании разлагается на формамид и воду, и это его основное применение в промышленности. Муравьиная кислота также может быть получена путем реакции формиата аммония с разбавленной кислотой, и, поскольку формиат аммония также производится из муравьиной кислоты, он может служить способом хранения муравьиной кислоты.
Формиат аммония также может быть использован для восстановления функциональных групп палладием на углероде (Pd / C). В присутствии Pd / C формиат аммония разлагается до водорода, углекислый газ и боеприпасы ния. Этот газообразный водород адсорбируется на поверхности металла палладий, где он может реагировать с различными функциональными группами. Например, алкены могут быть восстановлены до алканов или формальдегида до метанола. Активированные одинарные связи с гетероатомами также могут быть заменены атомами водорода (гидрогенолиз ).
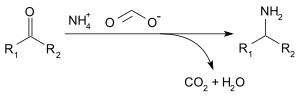
Формиат аммония можно использовать для восстановительного аминирования альдегидов и кетонов (реакция Лейкарта ) следующим образом реакция:
Формиат аммония может использоваться в качестве буфера в высокоэффективной жидкостной хроматографии (HPLC) и подходит для использования с жидкостной хроматографией-масс-спектрометрией (LC / MS).. Значения pKa для муравьиной кислоты и иона аммония составляют 3,8 и 9,2 соответственно.
При нагревании формиат аммония удаляет воду, образуя формамид. При дальнейшем нагревании он образует цианистый водород (HCN) и воду. Побочной реакцией при этом является разложение формамида до монооксида углерода (CO) и аммиака.
![]() СМИ, относящиеся к формиату аммония на Wikimedia Commons
СМИ, относящиеся к формиату аммония на Wikimedia Commons