 | |||
| |||
 | |||
| Имена | |||
|---|---|---|---|
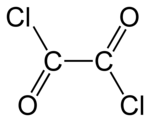
| Предпочтительное название IUPAC Оксалил дихлорид | |||
| Систематическое название ИЮПАК Этандиоил дихлорид | |||
| Другие названия Хлорид щавелевой кислоты Дихлорид щавелевой кислоты Дихлорид щавелевой кислоты Оксалоилхлорид | |||
| Идентификаторы | |||
| Количество CAS | |||
| 3D модель ( JSmol ) | |||
| ChemSpider | |||
| ECHA InfoCard | 100.001.092 | ||
| Номер ЕС | |||
| PubChem CID | |||
| Номер RTECS | |||
| UNII | |||
| Панель управления CompTox ( EPA) | |||
ИнЧИ
| |||
Улыбки
| |||
| Характеристики | |||
| Химическая формула | С 2 О 2 Cl 2 | ||
| Молярная масса | 126,93 г / моль | ||
| Появление | Бесцветная жидкость | ||
| Плотность | 1,4785 г / мл | ||
| Температура плавления | -16 ° С (3 ° F, 257 К) | ||
| Точка кипения | От 63 до 64 ° C (от 145 до 147 ° F; от 336 до 337 K) при 1,017 бар | ||
| Растворимость в воде | Реагирует | ||
| Показатель преломления ( n D) | 1,429 | ||
| Опасности | |||
| Основные опасности | Токсичный, едкий, слезоточивый | ||
| Паспорт безопасности | Внешний паспорт безопасности материала | ||
| Пиктограммы GHS |   | ||
| Сигнальное слово GHS | Опасность | ||
| Положения об опасности GHS | H314, H331 | ||
| Меры предосторожности GHS | P261, P280, P305 + 351 + 338, P310 | ||
| NFPA 704 (огненный алмаз) |  3 1 2 3 1 2 | ||
| Родственные соединения | |||
| Родственные ацилхлориды | Малонил хлорид сукцинил хлорида фосгена | ||
| Родственные соединения | Щавелевая кислота диэтилоксалата оксамидом оксалилхлорид гидразид Cuprizon 1 | ||
| Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |||
| | |||
| Ссылки на инфобоксы | |||
Оксалилхлорид - это химическое соединение с формулой (COCl) 2. Это бесцветное, острый пахнущие жидкости, ди - ацил хлорид из щавелевой кислоты, является полезным реагентом в органическом синтезе.
Оксалилхлорид был впервые получен в 1892 году французским химиком Адрианом Фоконье, который вступил в реакцию диэтилоксалата с пентахлоридом фосфора. Она также может быть получена путем обработки щавелевой кислоты с пентахлоридом фосфора.
Оксалилхлорид коммерчески производится из этиленкарбоната. Фотохлорирование дает тетрахлорид, который впоследствии разлагается:
Оксалилхлорид реагирует с водой с выделением только газообразных продуктов: хлористого водорода (HCl), диоксида углерода (CO 2) и монооксида углерода (CO).
В этом он сильно отличается от других ацилхлоридов, которые гидролизуются с образованием хлористого водорода и исходной карбоновой кислоты.
Раствор, содержащий ДМСО и оксалилхлорид, с последующим гашением триэтиламином превращает спирты в соответствующие альдегиды и кетоны посредством процесса, известного как окисление по Сверну.
Оксалилхлорид в основном используется вместе с N, N- диметилформамидным катализатором в органическом синтезе для получения ацилхлоридов из соответствующих карбоновых кислот. Как и тионилхлорид, в этом случае реагент разлагается на летучие побочные продукты, что упрощает обработку. Одним из второстепенных побочных продуктов реакции, катализируемой N, N- диметилформамидом, является мощный канцероген, возникающий при разложении N, N- диметилформамида. По сравнению с тионилхлоридом оксалилхлорид является более мягким и селективным реагентом. Кроме того, он дороже, чем тионилхлорид, поэтому его обычно используют в меньших масштабах.

Эта реакция включает превращение ДМФ в производное имидоилхлорида (Me 2 N = CHCl +), как и первая стадия реакции Вильсмайера – Хаака. Имидоилхлорид является активным хлорирующим агентом.
Оксалилхлорид реагирует с ароматическими соединениями в присутствии хлорида алюминия с образованием соответствующего ацилхлорида в процессе, известном как ацилирование Фриделя-Крафтса. Полученный ацилхлорид можно гидролизовать с образованием соответствующей карбоновой кислоты.
Как и другие ацилхлориды, оксалилхлорид реагирует со спиртами с образованием сложных эфиров:
Обычно такие реакции проводят в присутствии основания, такого как пиридин. Диэфир, полученный из фенола, фенилоксалатного эфира, представляет собой Cyalume, активный ингредиент светящихся палочек.
Сообщается, что оксалилхлорид был использован в первом синтезе диоксантетракетона (C 4 O 6), оксида углерода.
В марте 2000 года самолет Airbus A330 -300 Malaysia Airlines был поврежден и не подлежал ремонту после того, как в грузовой отсек просочился груз запрещенного оксалилхлорида (ложно заявленного как гидроксихинолин). Он токсичен при вдыхании, хотя он более чем на порядок менее токсичен, чем родственный фосген.