| |||
| Имена | |||
|---|---|---|---|
| Название IUPAC 1-бром- 2,5-пирролидиндион | |||
| Другие названия N-бромсукцинимид; NBS | |||
| Идентификаторы | |||
| Номер CAS | |||
| 3D-модель (JSmol ) | |||
| Ссылка Beilstein | 113916 | ||
| ChEBI | |||
| ChemSpider | |||
| ECHA InfoCard | 100.004.435 | ||
| Номер ЕС |
| ||
| Справочник Гмелина | 26634 | ||
| PubChem CID | |||
| UNII | |||
| Панель управления CompTox (EPA ) | |||
InChI
| |||
УЛЫБКА
| |||
| Свойства | |||
| Химическая формула | C4H4BrNO 2 | ||
| Молярная масса | 177,985 г · моль | ||
| Внешний вид | Белое твердое вещество | ||
| Плотность | 2,098 г / см (твердое вещество) | ||
| Температура плавления | 175 до 178 ° C (от 347 до 352 ° F; от 448 до 451 K) | ||
| Точка кипения | 339 ° C (642 ° F, 612 K) | ||
| Растворимость в воде | 14,7 г / л (25 ° C) | ||
| Растворимость в CCl 4 | Нерастворим (25 ° C) | ||
| Опасности | |||
| Основные опасности | Раздражающий | ||
| Паспорт безопасности | [1] | ||
| Если не указано иное, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа). | |||
| Ссылки в ink | |||
N-бромсукцинимид или NBS - это химический реагент используется в реакциях радикального замещения, электрофильного присоединения и электрофильного замещения в органической химии. NBS может быть удобным источником Br, радикала брома.
NBS имеется в продаже. Его также можно синтезировать в лаборатории. Для этого гидроксид натрия и бром добавляют к раствору сукцинимида в воде со льдом. Продукт NBS выпадает в осадок и может быть собран фильтрованием.
Неочищенный NBS дает лучший выход в реакции Воля-Циглера. В других случаях нечистый NBS (слегка желтого цвета) может дать ненадежные результаты. Его можно очистить перекристаллизацией из воды 90–95 ° C (10 г NBS на 100 мл воды).
NBS будет реагировать с алкенами 1 в водных растворителях с получением бромгидринов 2. Предпочтительными условиями являются порционное добавление NBS к раствору алкена в 50% водном ДМСО, ДМЭ, ТГФ или трет-бутаноле. при 0 ° C. Образование иона бромония и немедленная атака водой дает сильное марковниковское присоединение и антистереохимическую селективность.

Побочные реакции включают образование α-бромкетонов и дибромосоединений. Их можно свести к минимуму за счет использования свежеперекристаллизованного NBS.
С добавлением нуклеофилов вместо воды можно синтезировать различные бифункциональные алканы.

Стандартные условия для использования NBS в аллильном и / или бензильном бромировании включает кипячение раствора NBS в безводном CCl 4 с радикальным инициатором - обычно азобисизобутиронитрилом (AIBN ) или пероксид бензоила, облучение или то и другое для воздействия радикала инициирования. Аллильные и бензильные промежуточные радикалы, образующиеся во время этой реакции, более стабильны, чем другие углеродные радикалы, и основными продуктами являются аллильные и бензильные бромиды. Это также называется реакцией Воля – Циглера.

четыреххлористый углерод должен оставаться безводным на протяжении всей реакции, поскольку присутствие воды может гидролизоваться желаемый продукт. Карбонат бария часто добавляют для поддержания безводных и бескислотных условий.
В указанной выше реакции, хотя возможна смесь изомерных аллильных бромидных продуктов, создается только одна смесь из-за большей стабильности радикала в 4-м положении по сравнению с метилцентрированным радикалом.
NBS может α-бромировать карбонильные производные либо радикальным путем (как указано выше), либо посредством кислотного катализа. Например, гексаноилхлорид 1 может быть бромирован в альфа-положении с помощью NBS с использованием кислотного катализа.

Реакция енолятов, простых эфиров енолов или с NBS является предпочтительным методом α-бромирования, поскольку он высокопродуктивен с небольшим количеством побочных продуктов.
богатых электронами ароматических соединений, таких как фенолы, анилины и различные ароматические гетероциклы могут быть бромированы с использованием NBS. Использование ДМФ в качестве растворителя дает высокие уровни пара-селективности.
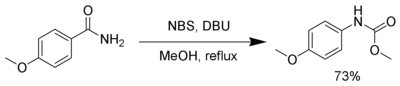
NBS в присутствии сильного основания, такого как DBU, реагирует с первичными амидами с образованием карбамата посредством перегруппировки Хофмана.
Это редко, но возможно для NBS для окисления спиртов. Э. Дж. Кори и др. обнаружили, что можно избирательно окислять вторичные спирты в присутствии первичных спиртов с использованием NBS в водном диметоксиэтане (DME).

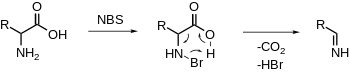
NBS электрофильно бромирует амин, за которым следует декарбоксилирование и высвобождение имина. Дальнейший гидролиз даст альдегид и аммиак. (ср. неокислительное декарбоксилирование, зависимое от PLP)
Хотя NBS проще и безопаснее в обращении, чем бром, следует соблюдать меры предосторожности, чтобы избежать вдыхания. НБС следует хранить в холодильнике. NBS со временем разлагается с выделением брома. Чистый NBS имеет белый цвет, но часто бывает, что он не совсем белый или коричневый из-за брома.
Обычно реакции с участием NBS являются экзотермическими. Поэтому при крупномасштабном использовании следует принимать дополнительные меры предосторожности.