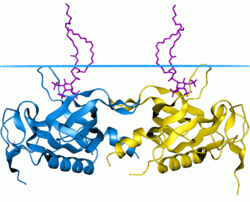
 PH-домен тирозинкиназы BTK PH-домен тирозинкиназы BTK | |||||||||
| Идентификаторы | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Символ | PH | ||||||||
| Pfam | PF00169 | ||||||||
| Pfam клан | CL0266 | ||||||||
| InterPro | IPR001849 | ||||||||
| SMART | PH | ||||||||
| PROSITE | PDOC50003 | ||||||||
| SCOPe | 1dyn / SUPFAM | ||||||||
| OPM белок суперсемейства | 49 | ||||||||
| OPM | 1pls | ||||||||
| CDD | cd00821 | ||||||||
| |||||||||
домен гомологии плекстрина (домен PH ) или (PHIP ) является доменом белка из примерно 120 аминокислот, которые встречаются в широком спектре белков, участвующих во внутриклеточной передаче сигналов, или в качестве компонентов цитоскелета.
Этот домен может связывать фосфатидилинозитол липиды внутри биологические мембраны (такие как фосфатидилинозитол (3,4,5) -трисфосфат и фосфатидилинозитол (4,5) -бисфосфат ) и белки, такие как βγ-субъединицы гетеротримерного G белки и протеинкиназа C. Благодаря этим взаимодействиям, домены PH играют роль в привлечении белков к различным мембранам, направляя их таким образом в соответствующие клеточные компартменты или позволяя им взаимодействовать с другими компонентами передачи сигнала. пути.
Отдельные домены PH обладают специфичностью в отношении фосфоинозитидов, фосфорилированных по различным сайтам внутри кольца инозитола, например, некоторые связывают фосфатидилинозит (4,5) - бисфосфат, но не фосфатидилинозитол (3,4,5) -трисфосфат или фосфатидилинозитол (3,4) -бисфосфат, тогда как другие могут обладать необходимой аффинностью. Это важно, потому что это делает привлечение различных белков, содержащих домен PH, чувствительными к активности ферментов, которые либо фосфорилируют, либо дефосфорилируют эти сайты на инозитоловом кольце, таких как фосфоинозитид-3-киназа или PTEN соответственно. Таким образом, такие ферменты частично влияют на функцию клеток, модулируя локализацию нижестоящих сигнальных белков, которые обладают доменами PH, способными связывать их фосфолипидные продукты.
Определена трехмерная структура нескольких PH-доменов. Все известные случаи имеют общую структуру, состоящую из двух перпендикулярных антипараллельных бета-листов, за которыми следует C-концевая амфипатическая спираль. Петли, соединяющие бета-нити, сильно различаются по длине, что делает домен PH относительно трудным для обнаружения, обеспечивая источник специфичности домена. Единственным консервативным остатком среди PH-доменов является единственный триптофан, расположенный внутри альфа-спирали, который служит ядром ядра домена.
домены PH, могут быть обнаружены во многих различных белках, таких как или ARF. Вербовка в Гольджи в этом случае зависит как от PtdIns, так и от ARF. Большое количество PH-доменов имеют низкое сродство к фосфоинозитидам и, как предполагается, функционируют как белковые связывающие домены. Полногеномный анализ Saccharomyces cerevisiae показал, что большинство из 33 дрожжевых PH-доменов действительно беспорядочно связываются с фосфоинозитидами, в то время как только один (Num1-PH) ведет себя высокоспецифично. Белки, содержащие домены PH, принадлежат к следующим семействам:
Кодирование генов человека белки, содержащие этот домен, включают: