| Нейроиммунная система | |
|---|---|
 На этой диаграмме показаны нейроиммунные механизмы, которые опосредуют индуцированную метамфетамином нейродегенерацию в мозге человека. Опосредованный NF-κB нейроиммунный ответ на употребление метамфетамина, который приводит к повышенной проницаемости гематоэнцефалического барьера, возникает из-за его связывания и активации рецепторов сигма-1, повышенное производство активных форм кислорода (ROS), активных форм азота (RNS) и молекул молекулярных структур, связанных с повреждениями (DAMPs), нарушение регуляции транспортеров глутамата (в частности, EAAT1 и EAAT2 ) и метаболизма глюкозы, а также избыточный приток кальция в глиальный клетки и дофамин нейроны. На этой диаграмме показаны нейроиммунные механизмы, которые опосредуют индуцированную метамфетамином нейродегенерацию в мозге человека. Опосредованный NF-κB нейроиммунный ответ на употребление метамфетамина, который приводит к повышенной проницаемости гематоэнцефалического барьера, возникает из-за его связывания и активации рецепторов сигма-1, повышенное производство активных форм кислорода (ROS), активных форм азота (RNS) и молекул молекулярных структур, связанных с повреждениями (DAMPs), нарушение регуляции транспортеров глутамата (в частности, EAAT1 и EAAT2 ) и метаболизма глюкозы, а также избыточный приток кальция в глиальный клетки и дофамин нейроны. | |
| Детали | |
| Система | Нейроиммунные |
| Идентификаторы | |
| MeSH | D015213 |
| Анатомическая терминология [редактировать в Викиданных ] | |
нейроиммунная система - это система структур и процессов, включающая биохимические и электрофизиологические взаимодействия между нервной системой и иммунной системой которые защищают нейроны от возбудители. Он служит для защиты нейронов от болезней путем поддержания избирательно проницаемых барьеров (например, гематоэнцефалический барьер и гематоэнцефалический барьер ), опосредуя нейровоспаление и заживление ран в поврежденных нейронах и мобилизация защиты хозяина от патогенов.
Нейроиммунная система и периферическая иммунная система структурно различаются. В отличие от периферической системы, нейроиммунная система состоит в основном из глиальных клеток ; Среди всех гемопоэтических клеток иммунной системы только тучные клетки обычно присутствуют в нейроиммунной системе. Однако во время нейроиммунного ответа определенные периферические иммунные клетки способны преодолевать различные барьеры между кровью или жидкостью и мозгом, чтобы реагировать на патогены, проникшие в мозг. Например, есть доказательства того, что после повреждения макрофаги и Т-клетки иммунной системы мигрируют в спинной мозг. Также было зарегистрировано, что продукция иммунных клеток системы комплемента создается непосредственно в центральной нервной системе.
Ключевыми клеточными компонентами нейроиммунной системы являются глиальные клетки, включая астроцитов, микроглии и олигодендроцитов. В отличие от других гемопоэтических клеток периферической иммунной системы, тучные клетки естественным образом встречаются в головном мозге, где они опосредуют взаимодействия между кишечными микробами, иммунной системой и центральной нервной системой как часть ось микробиота-кишечник-мозг.
рецепторы, связанные с G-белком, которые присутствуют как в ЦНС, так и в типах иммунных клеток и которые отвечают за нейроиммунный сигнальный процесс, включают:
Нейроиммунная система и ее изучение включают понимание иммунной и неврологической систем и перекрестное регулирующее влияние их функций. Цитокины регулируют иммунные ответы, возможно, за счет активации оси гипоталамус-гипофиз-надпочечники (HPA). Цитокины также участвуют в координации между нервной и иммунной системами. Были задокументированы случаи связывания цитокинов с нервными рецепторами между высвобождающими цитокины иммунными клетками IL-1β и нервным рецептором IL-1R. Это связывание приводит к электрическому импульсу, который вызывает ощущение боли. Все больше данных свидетельствует о том, что аутоиммунные Т-клетки участвуют в нейрогенезе. Исследования показали, что во время адаптивного ответа иммунной системы нейрогенез гиппокампа увеличивается, и, наоборот, аутоиммунные Т-клетки и микроглия важны для нейрогенеза (и, следовательно, памяти и обучения) у здоровых взрослых.
нейроиммунная система использует дополнительные процессы как сенсорных нейронов, так и иммунных клеток для обнаружения и реагирования на вредные или вредные стимулы. Например, вторгшиеся бактерии могут одновременно активировать инфламмасомы, которые обрабатывают интерлейкины (IL-1 β ), и деполяризовать сенсорные нейроны посредством секреции гемолизинов.. Гемолизины создают поры, вызывая деполяризующее высвобождение ионов калия изнутри эукариотической клетки и приток ионов кальция. Вместе это приводит к потенциалу действия в сенсорных нейронах и активации инфламмасом.
Травма и некроз также вызывают нейроиммунный ответ. Высвобождение аденозинтрифосфата (АТФ) из поврежденных клеток связывается с рецепторами P2X7 на макрофагах иммунной системы и активирует их как P2X3, так и P2X3 рецепторы ноцицепторов нервной системы. Это вызывает комбинированный ответ как результирующего потенциала действия из-за деполяризации, создаваемой притоком ионов кальция и калия, так и активации инфламмасом. Производимый потенциал действия также отвечает за ощущение боли, и иммунная система вырабатывает IL-1β в результате связывания рецептора АТФ P2X7.
Хотя воспаление обычно считается иммунным ответом, это сочетание нервных процессов, связанных с воспалительным процессом иммунной системы. После травмы или инфекции возникает каскад воспалительных реакций, таких как секреция циоткинов и хемокинов, которые сочетаются с секрецией нейропептидов (например, вещество P ) и нейротрансмиттеры (такие как серотонин ). Вместе этот связанный нейроиммунный ответ оказывает усиливающее действие на воспаление.
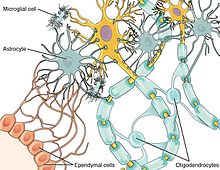 Различные типы глиальных клеток, включая микроглию, астроглию и олигодендроциты.
Различные типы глиальных клеток, включая микроглию, астроглию и олигодендроциты. Нейроны и глиальные клетки работают вместе, чтобы бороться с вторжением патогенов и травмами. Хемокины играют важную роль в качестве посредника между нейронно-глиальными клетками, поскольку оба типа клеток экспрессируют хемокиновые рецепторы. Например, хемокин фракталкин участвует в связи между нейронами микроглии и ганглия дорсального корешка (DRG) в спинном мозге. Фракталкин был связан с повышенной чувствительностью к боли при введении in vivo, и было обнаружено, что он активирует молекулы, опосредующие воспаление. Глиальные клетки могут эффективно распознавать патогены как в центральной нервной системе, так и в периферических тканях. Когда глиальные клетки распознают чужеродные патогены с помощью передачи сигналов цитокинов и хемокинов, они могут передавать эту информацию в ЦНС. Результат - усиление депрессивных симптомов. Однако хроническая активация глиальных клеток приводит к нейродегенерации и нейровоспалению.
Клетки микроглии являются наиболее заметными типами глиальных клеток в головном мозге. Одна из их основных функций - фагоцитоз клеточного дебриса после апоптоза нейронов. После апоптоза мертвые нейроны выделяют химические сигналы, которые связываются с микроглиальными клетками и заставляют их поглощать вредный мусор из окружающей нервной ткани. Микроглия и система комплемента также связаны с сокращением синапсов, так как их секреция цитокинов, факторов роста и других комплементов способствует удалению устаревших синапсов.
Астроциты - еще один тип глиальных клеток. которые, помимо других функций, модулируют проникновение иммунных клеток в ЦНС через гематоэнцефалический барьер (BBB). Астроциты также выделяют различные цитокины и нейротрофины, которые позволяют иммунным клеткам проникать в ЦНС; эти задействованные иммунные клетки нацелены как на патогены, так и на поврежденную нервную ткань.
 Рефлекс отмены
Рефлекс отмены рефлекс отмены - это рефлекс, который защищает организм от вредных раздражителей. Этот рефлекс возникает, когда ядовитые стимулы активируют ноцицепторы, которые посылают потенциал действия к нервам в позвоночнике, которые затем иннервируют эффекторные мышцы и вызывают внезапный толчок для перемещения позвоночника. организм вдали от опасных раздражителей. Рефлекс отмены затрагивает как нервную, так и иммунную системы. Когда потенциал действия распространяется обратно по сети спинномозговых нервов, другой импульс перемещается к периферическим сенсорным нейронам, которые секретируют аминокислоты и нейропептиды, такие как пептид, связанный с геном кальцитонина (CGRP) и Вещество Р. Эти химические вещества действуют, усиливая покраснение, отек поврежденных тканей и прикрепляя иммунные клетки к эндотелиальной ткани, тем самым увеличивая проницаемость иммунных клеток через капилляры.
Нейроиммунные взаимодействия также возникают, когда патогены, аллергены или токсины проникают в организм. блуждающий нерв соединяется с кишечником и дыхательными путями и вызывает нервные импульсы в ствол мозга в ответ на обнаружение токсинов и патогенов. Этот электрический импульс, который идет вниз от ствола головного мозга, достигает слизистых клеток и стимулирует секрецию слизи; этот импульс также может вызвать выброс токсина из-за мышечных сокращений, вызывающих рвоту или диарею.
Нейроиммунная система участвует в рефлексах, связанных с паразитарным вторжением в организм хозяина. Ноцицепторы также связаны с рефлексами организма на патогены, поскольку они находятся в стратегически важных местах, таких как дыхательные пути и ткани кишечника, и вызывают сокращения мышц, вызывающие расчесывание, рвоту и кашель. Все эти рефлексы предназначены для изгнания болезнетворных микроорганизмов из организма. Например, расчесывание вызывается зудящими генами, которые стимулируют ноцицепторы на эпидермальных тканях. Эти пруритогены, такие как гистамин, также заставляют другие иммунные клетки секретировать дополнительные пруритогены, чтобы вызвать больший зуд, чтобы физически удалить паразитарных захватчиков. Что касается кишечных и бронхиальных паразитов, то рвота, кашель и диарея также могут быть вызваны стимуляцией ноцицепторов в инфицированных тканях и нервными импульсами, исходящими от ствола мозга, которые иннервируют соответствующие гладкие мышцы.
Эозинофилы в ответ на капсаицин могут запускать дополнительную сенсибилизацию к молекуле. У пациентов с хроническим кашлем также наблюдается усиленный кашлевой рефлекс на патогенные микроорганизмы, даже если возбудитель был изгнан. В обоих случаях высвобождение эозинофилов и других иммунных молекул вызывает гиперчувствительность сенсорных нейронов в бронхиальных дыхательных путях, что вызывает усиление симптомов. Также сообщалось, что повышенная секреция нейротрофинов иммунными клетками в ответ на загрязнители и раздражители может реструктурировать периферическую сеть нервов в дыхательных путях, чтобы обеспечить более примированное состояние для сенсорных нейронов.
Было продемонстрировано, что длительный психологический стресс может быть связан с повышенным риском заражения вирусными респираторными инфекциями. Исследования на животных показывают, что психологический стресс повышает уровень глюкокортикоидов и, в конечном итоге, повышает восприимчивость к стрептококковым кожным инфекциям.
Нейроиммунная система играет роль в болезни Альцгеймера. В частности, микроглия может быть защитной, способствуя фагоцитозу и удалению отложений амилоида-β (Aβ), но также становится дисфункциональной по мере прогрессирования заболевания, вырабатывая нейротоксины, прекращение удаления отложений Aβ и выработка цитокинов, которые дополнительно способствуют отложению Aβ. Было показано, что при болезни Альцгеймера амилоид-β напрямую активирует микроглию и другие моноциты с образованием нейротоксинов..
Астроциты также участвуют в рассеянном склерозе (MS). Астроциты ответственны за демиелинизацию и разрушение олигодендроцитов, связанное с заболеванием. Этот демиелинизирующий эффект является результатом секреции цитокинов и матриксных металлопротеиназ (ММП) из активированных клеток астроцитов на соседние нейроны. Астроциты, которые остаются в активированном состоянии, образуют глиальные рубцы, которые также предотвращают повторную миелинизацию нейронов, поскольку они являются физическим препятствием для клеток-предшественников олигодендроцитов (OPCs).
Нейроиммунная система также участвует в астме и хроническом кашле, поскольку оба являются результатом сверхчувствительного состояния сенсорных нейронов из-за высвобождения иммунных молекул и механизмов положительной обратной связи.
Доклинические и клинические исследования показали, что клеточные (микроглия / макрофаги, лейкоциты, астроциты, тучные клетки и т. Д.) И молекулярные нейроиммунные реакции способствуют вторичному повреждению мозга после внутримозгового кровоизлияния.